Синдром нечувствительности к андрогенам
Из Википедии, свободной энциклопедии
Синдро́м нечувстви́тельности к андроге́нам (синдро́м резисте́нтности к андроге́нам, синдром Морриса, синдром тестикуля́рной феминиза́ции[2]; англ. Androgen insensitivity syndrome — AIS) — врожденные эндокринные вариации полового развития, вызванные мутацией гена, отвечающего за андрогеновый рецептор. Подобные синдромы варьируются в зависимости от структуры и чувствительности аномального рецептора. Клинические фенотипы находятся в диапазоне от номинального мужского телосложения с мягким синдромом сперматогенеза до крайне феминного телосложения, в дополнение к наличию Y-хромосомы[3][4][5].
Нечувствительность к андрогенам является клинически значимой только для людей с Y-хромосомой, или, более конкретно, с геном SRY [3].
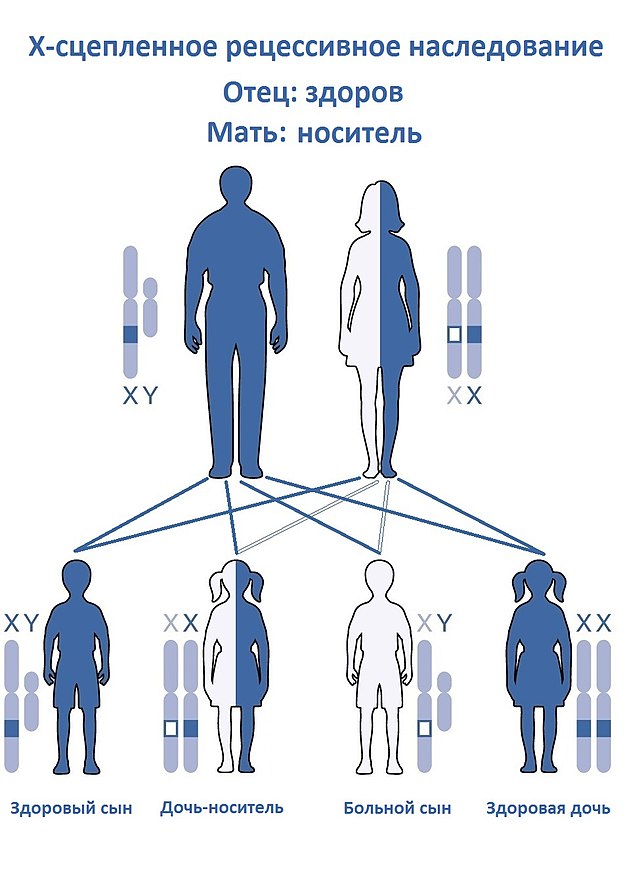
Для синдрома характерно X-сцепленное рецессивное наследование.
Синдром нечувствительности к андрогенам делится на три типа, которые различаются по степени маскулинизации гениталий: синдром полной нечувствительности к андрогенам (когда наружные гениталии имеют женский фенотип); синдром лёгкой нечувствительности к андрогенам (когда наружные гениталии имеют мужской фенотип) и синдром частичной нечувствительности к андрогенам (когда наружные гениталии частично, но не полностью, маскулинизированы)[6][7][8][9][10][11][12][13][14]. Синдром нечувствительности к андрогенам это наиболее частая причина гениталий неопределённого типа у людей с кариотипом 46.XY[15].
Помощь пациентам с данным состоянием на текущий момент проводится симптоматически; в настоящее время не существует метода для коррекции неправильно функционирующих рецепторов белков к андрогенам, происходящих из-за мутаций гена AR. Области в которых оказывается медицинская помощь включают в себя генитопластику (по желанию пациента), гонадэктомию (в случаях развития риска опухолей), заместительную гормональную терапию, генетическое консультирование и психологическую помощь.
Генетика
Суммиров вкратце
Перспектива
Рецептор андрогена человека (AR) представляет собой белок, кодируемый геном, расположенным на проксимальном длинном плече Х-хромосомы (локус Xq11-Xq12)[16]. Область, кодирующая белок, состоит из приблизительно 2757 нуклеотидов (919 кодонов), охватывающих восемь экзонов, обозначенных 1-8 или A-H[3][17]. Интроны различаются по размеру от 0,7 до 26 кб[17]. Как и другие ядерные рецепторы, белок AR состоит из нескольких функциональных доменов: домена трансактивации (также называемого доменом регуляции транскрипции или амино / NH2-терминальным доменом), ДНК-связывающего домена, шарнирной области и стероид-связывающего домен (также называемый карбоксильным лиганд-связывающим доменом)[3][7][17][14]. Домен трансактивации кодируется экзоном 1 и составляет более половины белка AR[17]. Экзоны 2 и 3 кодируют ДНК-связывающий домен, тогда как 5'-часть экзона 4 кодирует шарнирную область[17]. Остальная часть экзонов с 4 по 8 кодирует лиганд-связывающий домен[17].

Мутации в гене AR
По состоянию на 2010г. в базе данных мутаций AR зарегистрировано более 400 разновидностей мутаций этого гена, и их число продолжает расти[7]. Наследование обычно происходит по материнской линии путём X-сцепленного рецессивного наследования[3][18]. Примерно в 30% случаев мутация гена AR имеет спонтанный характер и не наследуется[11]. Такие мутации de novo являются результатом мутации гоноцита или мозаицизма в гоноците в гонаде одного из родителей или мутаций в самой оплодотворенной яйцеклетке[19]. В одном исследовании[20] три из восьми мутаций de novo произошли на постзиготически[3]. Не каждая мутация гена AR приводит к нечувствительности к андрогенам; одна конкретная мутация встречается у 8–14% генетических мужчин[21][22][23][24], и, как полагают, отрицательно влияет на небольшое количество особей при наличии других генетических факторов[25].
Другие причины
У некоторых людей с полной или частичной нечувствительностью нет мутаций гена AR, несмотря на клинические, гормональные и гистологические особенности, необходимые для установления диагноза синдром нечувствительности к андрогенам; до 5% женщин с полной нечувствительностью к андрогенам не имеют мутации гена AR[7], а также от 27[9][26] до 72%[27] людей с частичной нечувствительностью к андрогенам.
У одного пациента основной причиной предполагаемой частичной нечувствительности к андрогенам была мутация белка стероидогенного фактора-1 (SF-1)[28]. У другого пациента полная нечувствительность к андрогенам была результатом дефицита в передаче трансактивирующего сигнала от N-концевой области нормального рецептора андрогена к основному механизму транскрипции клетки[29].
XY кариотип
В зависимости от мутации, человек с кариотипом 46,XY и нечувствительностью к андрогенам может иметь мужской или женский фенотип[30] или могут иметь гениталии промежуточного типа[31]. У таких людей гонады являются яичками независимо от фенотипа из-за наличия Y-хромосомы[32][33]. Человек 46,XY, таким образом, может не иметь яичников или матки, внешне не отличаясь при этом от женщины с кариотипом 46,XX[34].
Было опубликовано несколько тематических исследований фертильных мужчин с кариотипом 46,XY и нечувствительностью к андрогенам[35][36][37][38][39], хотя эта группа считается малочисленной[14]. Кроме того, некоторые бесплодные мужчины с легкой формой нечувствительности к андрогенам смогли зачать детей после увеличения количества сперматозоидов с помощью дополнительного тестостерона[3][40]. Генетический мужчина, зачатый мужчиной с нечувствительностью к андрогенам, не получит Х-хромосому своего отца и, следовательно, не наследует и не несет ген синдрома. Генетическая женщина, зачатая таким образом, получит Х-хромосому своего отца, следовательно, станет носителем.
ХХ кариотип
Генетические женщины (кариотип 46,ХХ) имеют две Х-хромосомы, поэтому имеют два гена AR. Мутация в одном (но не в обоих) приводит минимальным проявлениям. Эти женщины фертильны и являются носителями мутации. Было отмечено, что у некоторых носителей слегка уменьшено количество волос на теле, наблюдаются задержки полового созревание и/или наблюдается высокий рост, вероятно, из-за искаженной инактивации Х-хромосомы[17][35]. Женщина-носитель будет передавать мутировавший ген AR своим детям в 50% случаев. Если ребенок, получивший мутацию - генетически женщина, то она тоже будет носителем мутации. Если ребенок, получивший мутацию - генетически мужчина, то у него будет нечувствительность к андрогенам.
Генетическая женщина с мутациями в обоих генах AR теоретически может возникнуть в результате объединения фертильного мужчины с нечувствительностью к андрогенам и женщиной-носителя гена с мутацией или в результате мутации de novo. Однако, учитывая малое количество фертильных мужчин с нечувствительностью к андрогенам и низкий уровень мутации гена AR, шансы на это невелики. Фенотип такого человека является предметом спекуляций; по состоянию на 2010 год, не было зарегистрировано таких случаев.
Патофизиология
Суммиров вкратце
Перспектива


Андрогены в развитии плода
Эмбрионы человека развиваются одинаково в течение первых шести недель, независимо от генетического пола (46,XX или 46,XY); единственный способ определить разницу между 46,XX или 46,XY эмбрионами в этот период времени — это поиск телец Барра или Y-хромосомы[42]. Гонады изначально представляют собой выпуклости ткани, называемые генитальным бугорком. К пятой неделе генитальный бугорок превращается в индифферентные гонады[42]. К шестой неделе индифферентные гонады начинают дифференцироваться в зависимости от генетического пола. Если кариотип 46,XY, яички развиваются из-за влияния гена SRY Y-хромосомы[33][32]. Этот процесс не требует присутствия андрогена или функционального рецептора андрогена[32][33].
Примерно до седьмой недели развития зародыш имеет индифферентные протоки, которые состоят из двух пар протоков: мюллеровых и вольфовых[42]. Примерно в это время клетки Сертоли в яичках выделяют антимюллеров гормон, чтобы подавить развитие мюллеровых протоков и вызвать их дегенерацию[42]. Если этого не происходит, то мюллеровы протоки развиваются в женские половые органы (матка, шейка матки, фаллопиевы трубы и верхняя часть влагалища)[42]. В отличие от мюллеровых протоков, вольфовы протоки не будут развиваться по умолчанию[43]. При наличии тестостерона и функциональных андрогенных рецепторов протоки Вольфа превращаются в эпидидимис, семявыносящие протоки и семенные пузырьки[42]. Если яички не способны секретировать тестостерон или андрогенные рецепторы не функционируют должным образом, протоки Вольфа вырождаются[44].
Маскулинизация мужских половых органов зависит как от тестостерона, так и от дигидротестостерона[41].
Маскулинизация мужских наружных половых органов, а также предстательной железы, зависит от андрогенного дигидротестостерона[45][46][47][48]. Тестостерон превращается в дигидротестостерон с помощью фермента 5-альфа-редуктазы[49]. Если этот фермент отсутствует или его мало, то дигидротестостерон не генерируется, и внешние мужские гениталии не развиваются должным образом[45][46][47][48][49]. Как и в случае с внутренними мужскими органами, для дигидротестостерона необходим функциональный рецептор андрогена, чтобы регулировать транскрипцию генов-мишеней, участвующих в развитии[50].
Патогенез нечувствительности к андрогенам
Мутации в гене рецептора андрогена могут вызывать проблемы на любом из этапов андрогенизации, начиная с синтеза самого белка рецептора андрогена и заканчивая транскрипционной способностью димеризованного комплекса андроген-АР[17]. Нечувствительность к андрогенам может привести к значительному нарушению хотя бы одного из этих этапов, поскольку каждый шаг необходим андрогенам для успешной активации AR и регуляции экспрессии генов[17]. То, какие именно этапы будут мешать конкретной мутации, можно до некоторой степени предсказать, идентифицируя область AR, в которой находится мутация. Эта прогнозирующая способность в основном имеет ретроспективный характер; различные функциональные домены гена AR были выяснены путем анализа эффектов специфических мутаций в различных областях AR[17]. Например, известно, что мутации в стероидсвязывающем домене влияют на сродство или удержание андроген-связывающего вещества, известно, что мутации в шарнирной области влияют на транслокацию ядер, известно, что мутации в ДНК-связывающем домене влияют на димеризацию и связывание с мишенью. Известно, что ДНК и мутации в домене трансактивации влияют на регуляцию транскрипции гена-мишени[17][43]. Даже когда пораженный функциональный домен известен, предсказать фенотипические последствия конкретной мутации сложно.
Некоторые мутации могут отрицательно повлиять на более чем один функциональный домен. Например, мутация в одном функциональном домене может оказывать вредное влияние на другой, изменяя способ взаимодействия доменов[43]. Одиночная мутация может повлиять на все нижестоящие функциональные домены, если результатом является преждевременный стоп-кодон или ошибка кадрирования; такая мутация может привести к совершенно непригодному (или несинтезируемому) белку рецептора андрогена[17]. Стероидсвязывающий домен особенно чувствителен к эффектам преждевременного стоп-кодона или ошибочному кадрированию, поскольку он возникает в конце гена, и поэтому его информация, скорее всего, будет усечена или неверно истолкована, чем другие функциональные домены[17].
Другие, более сложные отношения наблюдались как следствие мутированного AR; некоторые мутации, связанные с мужскими фенотипами, были связаны с мужским раком молочной железы, раком простаты или, в случае спинальной и бульбарной мышечной атрофии, заболеванием центральной нервной системы[51][52][53][54][55]. Форма рака молочной железы, наблюдаемая у некоторых мужчин с частичной нечувствительностью к андрогенам, вызвана мутацией в ДНК-связывающем домене AR[53][55]. Считается, что эта мутация вызывает нарушение взаимодействия гена-мишени AR, что позволяет ему действовать на определенных дополнительных мишенях, возможно, в сочетании с белком рецептора эстрогена, вызывая рост раковых клеток[17]. Патогенез спинальной и бульбарной мышечной атрофии показывает, что даже сам мутантный белок AR может привести к патологии. Расширение тринуклеотидного повтора полиглатаминового тракта гена AR, связанного с этой атрофией, приводит к синтезу неправильно свернутого белка AR, который клетка не может протеолизовать должным образом[56]. Эти неправильно свернутые AR-белки образуют агрегаты в цитоплазме и ядре клетки[56]. В течение 30-50 лет эти агрегаты накапливаются и оказывают цитотоксическое действие, что в конечном итоге приводит к нейродегенеративным симптомам, связанным с атрофией[56].
Диагностика
Суммиров вкратце
Перспектива

Варианты фенотипа, возникающие из-за нечувствительности к андрогенам, не являются уникальными для этого состояния, поэтому диагностика требует полного исключения других причин[15][57]. Клинические признаки, указывающие на нечувствительность к андрогенам, включают наличие слепого влагалища[58] или недостаточную маскулинизацию гениталий[3][59][45], частичную или полную регрессию мюллеровых протоков[60], двусторонние недиспластические яички[61], и нарушение сперматогенеза и/или вирилизацию[3][5][9][51], кариотип 46,XY[7] и нормальный или повышенный уровень постпубертатного тестостерона, лютеинизирующего гормона и эстрадиола[7][15]. Андроген-связывающая активность фибробластов кожи гениталий, как правило, снижается[17][62], хотя сообщалось об исключениях[63]. Преобразование тестостерона в дигидротестостерон может быть нарушено[17]. Диагноз подтверждается, если секвенирование гена рецептора андрогена обнаруживает мутацию, хотя не у всех людей с нечувствительностью к андрогенам (особенно с частичной нечувствительностью) присутствует мутация гена AR[7][9][26][27].
Каждый из трех типов состояния (полная, частичная и легкая нечувствительность к андрогенам) имеет свой список дифференциальных диагнозов[3]. В зависимости от формы подозреваемого состояния, список может включать[33][32][64][65][66]:
- Хромосомные аберрации:
- Синдром Клайнфелтера (кариотип 47,XXY)
- Синдром Шерешевского — Тёрнера (кариотип 45, ХО)
- Смешанная дисгенезия гонад (кариотип 45, XO / 46, XY)
- Тетрагаметический химеризм (кариотип 46, XX / 46, XY)
- Андрогенная биосинтетическая дисфункция у лиц с кариотипом 46,XY:
- Мутации рецепторов лютеинизирующего гормона (ЛГ)
- Синдром Смита – Лемли – Опица (связанный с умственной отсталостью)
- Липоидная врождённая гиперплазия надпочечников
- ВГКН вследствие недостаточности 3-бета-гидроксистероиддегидрогеназы
- ВГКН вследствие недостаточности 17-альфа-гидроксилазы
- 17,20 lyase deficiency
- Дефицит 17β-гидроксистероиддегидрогеназы III
- Дефицит 5-альфа-редуктазы
- Избыток андрогена у 46, XX человек:
- ВГКН вследствие недостаточности 21-гидроксилазы
- ВГКН вследствие недостаточности 3-бета-гидроксистероиддегидрогеназы
- Дефицит цитохрома P450 оксидоредуктазы
- ВГКН вследствие недостаточности 11-бета-гидроксилазы
- Дефицит ароматазы
- Мутации глюкокортикоидных рецепторов
- Материнская вирилизирующая опухоль (например, лютеома)
- Повышенное воздействие андрогенов в утробе матери, не указано иное (например, андрогенные препараты)
- Связанные с развитием
- Синдром Майера — Рокитанского — Кустера — Хаузера (кариотип 46,ХХ)
- Синдром Свайера (кариотип 46,ХY)
- XX дисгенезия гонад (46, XX кариотип)
- Гипоплазия клеток Лейдига
- Анорхизм
- Овотестикулярное НФП
- НФП яичка
- Тератогенные причины (например, эстрогены, антиэстрогены)
- Другое:
- Синдром Фрейзера (связанный с прогрессирующей гломерулопатией)
- Синдром Дениса-Драш (связанный с нефропатией и опухолью Вильмса)
- Синдром WAGR (связан с опухолью Вильмса и аниридиями)
- Синдром Мак-Кьюсика-Кауфмана (связанный с постаксиальной полидактилией)
- Синдром Робинова (связанный с карликовостью)
- Синдром Аарскога – Скотта (связанный с аномалиями лица)
- Hand-foot-genital syndrome (связан с пороками развития конечностей)
- Синдром подколенного птеригиума (связан с обширными перепонками за коленями)
- Синдром Каллмана (часто связанный с аносмией)
- Гипоспадия, не указанная иным образом
- Крипторхизм не указано иное
- Атрезия влагалища, не указанная иным образом
Эпидемиология
Оценки встречаемости нечувствительности к андрогенам основаны на относительно небольших выборках, поэтому неточны[3]. По оценкам, полная нечувствительность к андрогенам случается с вероятностью 1 на 20 400 родившихся людей с кариотипом 46,XY[67]. Общенациональный опрос в Нидерландах, основанный на пациентах с генетическим подтверждением диагноза, показывает, что минимальная частота полной нечувствительности составляет один на 99 000[68]. Встречаемость частичной нечувствительности к андрогенам оценивается как 1 из 130 000[69]. Из-за своего тонкого проявления легкая нечувствительность к андрогенам обычно не исследуется, за исключением случаев бесплодия у мужчин[45], поэтому его истинная распространенность неизвестна[7].
История
Суммиров вкратце
Перспектива
Ранее для обозначения нарушения использовался термин синдром тестикулярной феминизации (англ. testicular feminisation syndrom), который отражает исторически ошибочное понимание причины заболевания. В 1953 году американский гинеколог Джон Моррис дал первое полное описание синдрома на основе 82 случаев, собранных из медицинской литературы, в том числе двух своих пациентов[3][17]. Термин testicular feminisation syndrom был выбран для того, чтоб отразить представление Морриса о том, что яички у пациентов производят гормон, обладающий феминизирующим воздействием на организм. В настоящее время причину заболевания связывают с бездействием андрогенов и последующим превращением тестостерона в эстроген[3]. За несколько лет до Морриса Лоусон Уилкинс на собственных экспериментах показал, что невосприимчивость клеток-мишеней к андрогенным гормонам была причиной «мужского псевдогермафродитизма»[57][70]. Опыты Уилкинса наглядно продемонстрировали отсутствие терапевтического эффекта, когда женщин с генотипом 46XY лечили андрогенами. Понимание причины заболевания повлекло постепенный переход в номенклатуре от термина «testicular feminisation syndrom» к «androgen resistance»[71].
Хронология основных вех
- 1950: Лоусон Уилкинс[англ.] прописывает метилтестостерон пациентке с кариотипом 46,XY, у которой нет признаков вирилизации. Его эксперимент — первая задокументированная попытка лечения нечувствительности к андрогенам[57][72].
- 1970: Мэри Ф. Лайон и Сьюзен Хоукс сообщили, что ген на Х-хромосоме вызывал полную нечувствительность к андрогенам у мышей[73][74].
- 1981: Барбара Мигеон с коллегами сузили локус гена рецептора андрогена у человека (или фактора, контролирующего ген рецептора андрогена) где-то между Xq11 и Xq13[75][76].
- 1988: Ген рецептора андрогенов у человека впервые клонируется и частично анализируется[77][78]. Терри Браун с коллегами сообщили о первых найденных мутациях, доказано вызывающих нечувствительность к андрогенам[7][76].
- 1989: Терри Браун с коллегами сообщили о нахождении точного локуса гена AR (Xq11-Xq12)[16]; Деннис Любан с коллегами опубликовал его экзон-интрон границы[79].
- 1994: Создана база данных мутаций генов рецепторов андрогенов, для ведения полного списка мутаций, опубликованных в медицинских журналах и материалах конференций[80].
Ранняя терминология
Первые описания эффектов нечувствительности к андрогенам появились в медицинской литературе как отдельные случаи или как часть всестороннего описания физических свойств интерсексов. В 1839 году шотландский акушер сэр Джеймс Янг Симпсон опубликовал одно такое описание[81] в исчерпывающем исследовании интерсекс-состояний[82]. Система таксономии Симпсона, однако, была далеко не первой; таксономии или описания для классификации интерсекс-вариаций были разработаны итальянским врачом и физиком Фортуне Аффайтати в 1549 году[83][84], французским хирургом Амбруазом Паре в 1573 году[82][85], французским врачом и пионером сексологии Николя Венетт в 1687 году (под псевдоним Vénitien Salocini)[86][87], и французским зоологом Исидор Жоффруа Сен-Илер в 1832 году[88]. Все пять этих авторов использовали разговорный термин «гермафродит» в качестве основы своих таксономий, хотя сам Симпсон поставил под сомнение правильность этого слова в своей публикации[81]. Использование слова «гермафродит» в медицинской литературе сохранилось до наших дней[89][90], хотя его обоснованность все еще остается под вопросом. Недавно была предложена альтернативная система номенклатуры[91], но предмет того, какое именно слово или слова следует использовать вместо него, все еще вызывает много споров[65][92][93][94][95].
Псевдогермафродитизм
Термин «псевдогермафродитизм» до недавнего времени[91] использовался в медицинской литературе для описания состояния индивидуума, у которого гонады и кариотип не совпадают с внешними гениталиями. Например, лица с кариотипом 46.XY имеют женский фенотип, и вместе с тем яички вместо яичников. Группа, включающая всех людей с полной нечувствительностью к андрогенам, а также ряд лиц с частичной нечувствительностью к андрогенам классифицируются как имеющие мужской «псевдогермафродитизм», в то время как люди у которых есть яичник и яичко (или, по крайней мере, один яичник) классифицируются как имеющие «истинный гермафродитизм»[90][91]. Использование этого слова в медицинской литературе предшествует открытию хромосомы, поэтому при его использовании не учитывается кариотип при определении пола индивидуума. Предыдущие определения «псевдогермафродитизма» основывались на предполагаемых несоответствиях между внутренними и внешними органами; «истинный» пол индивида определялся внутренними органами, а внешние органы определяли «воспринимаемый» пол индивида[81][88].
Немецко-швейцарский патолог Эдвин Клебс иногда упоминается за использование слова «псевдогермафродитизм» в его таксономии интерсекс-состояний в 1876 году[96], хотя это слово явно не является его изобретением, как иногда сообщается; История слова «псевдогермафродит» и соответствующее желание отделить «истинных» гермафродитов от «ложных» или «псевдо» гермафродитов датируются как минимум 1709 годом, когда голландский анатом Фредерик Рюйш использовал его в описание субъекта с яичками и преимущественно женским фенотипом[97]. «Псевдогермафродит» также появился в Acta Eruditorum позже в том же году, в обзоре работы Рюйша[98]. Также некоторые данные указывают на то, что слово уже использовалось медицинским сообществом Германии и Франции задолго до того, как Клебс использовал его; Немецкий физиолог Йоханнес Петер Мюллер приравнивал «псевдогермафродитизм» к подклассу гермафродитизма из таксономии Сен-Илера в публикации от 1834 года[99], а к 1840-м годам «псевдогермафродитизм» появлялся в нескольких французских и немецких публикациях, включая словари[14][100][101][102].
Тестикулярная феминизация
В 1953 году американский гинеколог Джон Моррис дал первое полное описание того, что он назвал «тестикулярной феминизацией», основываясь на 82 случаях, собранных из медицинской литературы, в том числе двух его собственных пациентов[3][17][103]. Термин «тестикулярная феминизация» был придуман, чтобы отразить наблюдение Морриса о том, что яички у этих пациентов продуцируют гормон, который оказывает феминизирующее действие на организм, явление, которое, как теперь понимают, связано с бездействием андрогенов и последующей ароматизацией тестостерона в эстрогены[3]. За несколько лет до того, как Моррис опубликовал свою знаменательную статью, Лоусон Уилкинс в ходе эксперимента показал, что невосприимчивость клетки-мишени к действию андрогенных гормонов является причиной "мужского псевдогермафродитизма"[57][70]. Работа Уилкинса, которая ясно продемонстрировала отсутствие терапевтического эффекта, когда женщины с кариотипом 46.XY получали андрогены, вызвала постепенный сдвиг в номенклатуре от термина «тестикулярная феминизация» к термину «резистентность к андрогенам»[71].
Другие названия
Отдельное название было дано многим различным проявлениям нечувствительности к андрогенам, например, синдром Рейфенштейна (1947)[104], синдром Голдберга-Максвелла (1948)[105], синдром Морриса (1953)[103], синдром Гилберта-Дрейфуса (1957)[106], синдром Луба (1959)[107], «неполная тестикулярная феминизация» (1963)[108], синдром Розуотера (1965)[109], и синдром Аймана (1979)[110]. Поскольку не было понятно, что все эти различные проявления были вызваны одним и тем же набором мутаций в гене рецептора андрогена, каждому новому сочетанию симптомов было присвоено уникальное имя, что привело к сложному разделению на, казалось бы, не сопоставимые состояний[57][111].
За последние 60 лет, поскольку сообщения о поразительно различных фенотипах, как сообщалось, имели место даже среди членов одной семьи, и поскольку был достигнут устойчивый прогресс в понимании основного молекулярного патогенеза нечувствительности к андрогенам, было обнаружено, что эти состояния являются различными фенотипическими выражениями. одного и того же, вызванного молекулярными дефектами в гене рецептора андрогена[3][14][57][111].
В настоящее время нечувствительность к андрогенам является общепринятым названием для состояний, возникающих в результате невосприимчивости клеток-мишеней к действию андрогенных гормонов. Полная нечувствительность к андрогенам включает в себя фенотипы, ранее описанные как «тестикулярная феминизация», «синдром Морриса» и «синдром Голдберга-Максвелла»[3][112]; Частичная нечувствительность к андрогенам включает в себя «синдром Рейфенштейна», «синдром Гилберта-Дрейфуса, «синдром Луба», «неполную тестикулярную феминизацию» и «синдром Розуотера»[111][113][114]. Легкая нечувствительность к андрогенам включает «синдром Аймана»[115].
Более вирилизированные фенотипы нечувствительности к андрогенам иногда описывались как «синдром недовиризованного мужчины», «синдром бесплодного мужчины» и т.д. До того, как появились данные о том, что эти состояния были вызваны мутациями в гене AR[38], эти диагнозы были использованы для описания различных легких дефектов вирилизации; в результате фенотипы некоторых мужчин, которым был поставлен диагноз, лучше описываются частичной нечувствительностью (например, микропенис, гипоспадия и неопущенные яички), в то время как другие лучше описываются легкой нечувствительностью (например, изолированное мужское бесплодие или гинекомастия)[3][38][39][114][116][117].
В культуре
- В документальном фильме «Орхидеи: Мои интерсексуальные приключения» обе героини, Фиби Харт и Бонни Харт имеют данный синдром[118].
- В 13-й серии 2-го сезона сериала «Доктор Хаус» «Внешность обманчива» (англ. Skin Deep) главному пациенту серии ставят диагноз полная нечувствительность к андрогенам.
- В книге «None of the Above» у главной героини нечувствительность к андрогенам[119].
- В автобиографической книге «XOXY, A Memoir: Intersex Woman, Mother, Activist» Кимберли Зизельман описывает свой опыт жизни с данным состоянием[120].
Примечания
Ссылки
Wikiwand - on
Seamless Wikipedia browsing. On steroids.

