Европий
химический элемент с порядковым номером 63 Из Википедии, свободной энциклопедии
Евро́пий (химический символ — Eu, от лат. Europium) — химический элемент 3-й группы (по устаревшей классификации — побочной подгруппы третьей группы, IIIB) шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 63.
| Европий | ||||
|---|---|---|---|---|
| ← Самарий | Гадолиний → | ||||
| ||||
| Внешний вид простого вещества | ||||
 Очищенный европий (~300 г, чистота 99,998%) |
||||
| Свойства атома | ||||
| Название, символ, номер | Европий / Europium (Eu), 63 | |||
| Группа, период, блок |
3 (устар. IIIB), 6, f-элемент |
|||
| Атомная масса (молярная масса) |
151,964(1)[1] а. е. м. (г/моль) | |||
| Электронная конфигурация | [Xe] 6s24f7 | |||
| Радиус атома | 199 пм | |||
| Химические свойства | ||||
| Ковалентный радиус | 185 пм | |||
| Радиус иона | (+3e) 95 (+2e) 109 пм | |||
| Электроотрицательность | 1,2 (шкала Полинга) | |||
| Электродный потенциал |
Eu←Eu3+ -1,99 В Eu←Eu2+ -2,80 В |
|||
| Степени окисления | +2, +3 | |||
| Энергия ионизации (первый электрон) |
546,9 (5,67) кДж/моль (эВ) | |||
| Термодинамические свойства простого вещества | ||||
| Плотность (при н. у.) | 5,243 г/см³ | |||
| Температура плавления | 1099 К (826 °C) | |||
| Температура кипения | 1802 K (1529 °C) | |||
| Мол. теплота плавления | 9,21 кДж/моль | |||
| Мол. теплота испарения | 176 кДж/моль | |||
| Молярная теплоёмкость | 27,656[2] Дж/(K·моль) | |||
| Молярный объём | 28,9 см³/моль | |||
| Кристаллическая решётка простого вещества | ||||
| Структура решётки |
Кубическая объёмноцентрированая |
|||
| Параметры решётки | 4,581 Å | |||
| Прочие характеристики | ||||
| Теплопроводность | (300 K) 13,9 Вт/(м·К) | |||
| Номер CAS | 7440-53-1 | |||
| 63 | Европий |
| 4f76s2 | |
Относится к семейству лантаноидов.
Простое вещество европий — это мягкий редкоземельный металл серебристо-белого цвета, легко окисляющийся на воздухе.
История
Первыми спектральные линии, отнесённые впоследствии к европию, наблюдали Крукс (1886) и Лекок де Буабодран (1892). Демарсе обнаружил полосу спектра элемента в самариевой земле в 1896 году, а в 1901 году смог выделить элемент, описал его и дал ему название в честь Европы[3].
Нахождение в природе
Месторождения
Европий входит в состав лантаноидов, которые часто встречаются в России, Казахстанe, США, Австралии, Бразилии, Индии, Скандинавии. Крупнейшее в мире месторождение европия находится в Кении[4]. Значительны запасы в глубоководном месторождении редкоземельных минералов у тихоокеанского острова Минамитори в исключительной экономической зоне Японии[5].
Физические свойства
Суммиров вкратце
Перспектива
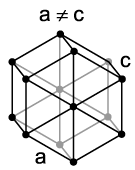
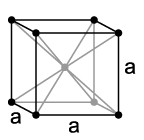
Полная электронная конфигурация атома европия: 1s22s22p63s23p64s23d104p65s24d105p66s24f7.
Европий (в чистом виде) представляет собой мягкий серебристо-белый металл. Он имеет необычно низкую плотность (5,243 г/см³), температуру плавления (826 °C) и температуру кипения (1440 °C) по сравнению со своими соседями по периодической системе элементов гадолинием и самарием. Эти величины противоречат явлению лантаноидного сжатия из-за влияния электронной конфигурации атома европия [Xe]4f76s2 на его свойства. Так как электронная оболочка f атома европия заполнена наполовину, для образования металлической связи предоставлены только два электрона, притяжение которых к ядру ослаблено и приводит к существенному увеличению радиуса атома. Аналогичное явление наблюдается также у атома иттербия. При нормальных условиях европий имеет кубическую объёмно-центрированную кристаллическую решетку с постоянной решетки 4,581 Å. При кристаллизации под высоким давлением европий образует ещё две модификации кристаллической решетки. При этом последовательность модификаций при возрастании давления отличается от такой последовательности у других лантаноидов, что наблюдается также и у иттербия. Первый фазовый переход происходит при давлении свыше 12,5 ГПа, при этом европий образует гексагональную кристаллическую решетку с параметрами a = 2,41 Å и c = 5,45 Å. При давлении свыше 18 ГПа европий образует аналогичную гексагональную кристаллическую решетку с более плотной упаковкой. Ионы европия, встроенные в кристаллическую решетку некоторых соединений, способны вызывать интенсивную флуоресценцию, причем длина волны излучаемого света зависит от степени окисления ионов европия. Eu3+ практически независимо от того вещества, в кристаллическую решетку которого он встроен, испускает свет с длиной волны 613 и 618 нм, что соответствует интенсивному красному цвету. Напротив, максимальная эмиссия Eu2+ сильно зависит от строения кристаллической решетки вещества-хозяина и, например, в случае алюмината бария-магния длина волны испускаемого света составляет 447 нм и находится в синей части спектра, а в случае алюмината стронция (SrAl2O4:Eu2+) длина волны составляет 520 нм и находится в зелёной части спектра видимого света. При давлении 80 ГПа[6] и температуре 1,8 К европий приобретает сверхпроводящие свойства.
Изотопы
Природный европий состоит из двух изотопов, 151Eu и 153Eu, в соотношении примерно 1:1. Европий-153 имеет природную распространённость 52,2 %, он стабилен. Изотоп европий-151 составляет 47,8 % природного европия. Недавно была обнаружена[7] его слабая альфа-радиоактивность с периодом полураспада около 5×1018 лет, что соответствует примерно 1 распаду за 2 минуты в килограмме природного европия. Кроме этого природного радиоизотопа, созданы и исследованы 35 искусственных радиоизотопов европия, среди которых наиболее устойчивы 150Eu (период полураспада 36,9 года), 152Eu (13,516 года) и 154Eu (8,593 года). Обнаружены также 8 метастабильных возбуждённых состояний, среди которых наиболее стабилен 150mEu (12,8 часа), 152m1Eu (9,3116 часа) и 152m2Eu (96 минут)[8].
Химические свойства
Суммиров вкратце
Перспектива
Европий является типичным активным металлом и вступает в реакции с большинством неметаллов. Европий в группе лантаноидов имеет максимальную реакционную способность. На воздухе быстро окисляется, на поверхности металла всегда есть оксидная плёнка. Хранят в банках или ампулах под слоем жидкого парафина или в керосине. При нагревании на воздухе до температуры 180 °C воспламеняется и горит с образованием оксида европия(III).
Очень активен, может вытеснять из растворов солей почти все металлы, кроме щелочных и щелочноземельных. В соединениях, как и большинство РЗЭ, проявляет преимущественно степень окисления +3, при определённых условиях (например, электрохимическим восстановлением, восстановлением амальгамой цинка и др.) можно получить степень окисления +2. Также при изменении окислительно-восстановительных условий возможно получение степени окисления +2 и +3, что соответствует оксиду с химической формулой Eu3O4. С водородом европий образует нестехиометрические фазы, в которых атомы водорода находятся в промежутках кристаллической решетки между атомами европия. Европий растворяется в аммиаке с образованием раствора синего цвета, что обусловлено, как и в подобных растворах щелочных металлов, образованием сольватированных электронов.
Получение
Металлический европий получают восстановлением Eu2O3 в вакууме лантаном или углеродом, а также электролизом расплава EuCl3.
Применение
Суммиров вкратце
Перспектива
Ядерная энергетика
Европий используется в ядерной энергетике в качестве поглотителя нейтронов (в основном окись европия, гексаборид и борат европия) в атомных реакторах, но окись постепенно «выгорает», и по срокам эксплуатации уступает карбиду бора в 1,5 раза (хотя имеет преимущество в почти полном отсутствии газовыделения и распухания в мощном потоке нейтронов, например, реактор БН-600). Сечение захвата тепловых нейтронов европием (природной смесью изотопов) составляет около 4500 барн, самым активным в отношении захвата нейтронов является европий-151 (9200 барн).
Атомно-водородная энергетика
Оксид европия применяется при термохимическом разложении воды в атомно-водородной энергетике (европий-стронций-йодидный цикл).
Лазерные материалы
Ионы европия служат для генерации лазерного излучения в видимой области спектра с длиной волны 0,61 мкм (оранжевые лучи), поэтому оксид европия используется для создания твердотельных, и менее распространённых жидкостных лазеров.
Электроника
Европий является легирующей примесью в моносульфиде самария (термоэлектрогенераторы), а также как легирующий компонент для синтеза алмазоподобного (сверхтвердого) нитрида углерода.
Силицид европия в виде тонких плёнок находит применение в интегральной микроэлектронике.
Моноокись европия, а также сплав моноокиси европия и моноокиси самария применяются в виде тонких плёнок в качестве магнитных полупроводниковых материалов для функциональной электроники и, в частности, МДП-электроники.
Люминофоры
- Европий — непременная составляющая люминофоров, используемых в электронно-лучевых и плазменных цветных экранах.
- Купюры евро защищены от подделок люминофорами на основе европия.
- Вольфрамат европия — люминофор, используемый в микроэлектронике.
- Легированный европием борат стронция используется как люминофор в лампах чёрного света.
Медицина
Катионы европия используются в медицинской диагностике в качестве флуоресцентных зондов. Радиоактивные изотопы европия применяются при лечении некоторых форм рака.
Другие сферы применения
- Интенсивно изучаются светочувствительные соединения европия с бромом, хлором и иодом.
- Европий-154 обладает большой мощностью тепловыделения при радиоактивном распаде и предложен в качестве источника в радиоизотопных источниках энергии.
Влияние на качество воды
В реакциях с водой европий химически ведёт себя как кальций. При уровнях рН ниже 6 европий способен мигрировать в воде в ионном виде. При более высоких уровнях рН европий образует плохо растворимые и, соответственно, менее подвижные гидроксиды. При контакте с кислородом воздуха происходит дальнейшее окисление до Eu2O3. Максимально наблюдаемые концентрации европия в природных маломинерализованных водах составляют менее 1 мкг/л (в морской воде — 1,1⋅10−6 мг/л). Влияние на качество воды при таких концентрациях представляется незначительным. Предельно допустимая концентрация (ПДК) в воде нормируется только российскими нормами и равна (для питьевой воды) 0,3 мг/л.
Пути поступления в организм
Вероятность попадания европия в организм человека представляется незначительной. Возможно поступление европия в организм с водой в микроскопических количествах. Нельзя исключать вероятности и других путей попадания в организм у людей, сталкивающихся с соединениями европия на производстве.
Потенциальная опасность для здоровья
Европий относится к малотоксичным элементам. Нет какой-либо информации о последствиях воздействия европия на организм человека.
Физиологическое значение
На данный момент нет данных о какой-либо биологической роли европия в организме человека или животных.
Цены
Европий является одним из самых дорогих лантаноидов[9]. В 2014 году цена металлического европия ЕВМ-1 составляла от 800 до 2000 долларов США за кг, а оксида европия чистотой 99,9 % — около 500 долларов за кг.
Примечания
Ссылки
Wikiwand - on
Seamless Wikipedia browsing. On steroids.


