
Monoxid de azot
compus chimic / From Wikipedia, the free encyclopedia
Monoxidul de azot este un gaz incolor cu formula chimică NO.
| Monoxid de azot | |
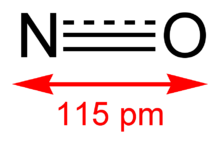 Formula structurală | |
 | |
| Denumiri | |
|---|---|
| Identificare | |
| Număr CAS | 10102-43-9 |
| ChEMBL | CHEMBL1200689 |
| PubChem CID | 145068 |
| Informații generale | |
| Formulă chimică | NO |
| Aspect | gaz incolor |
| Masă molară | 30,01 g/mol |
| Proprietăți | |
| Densitate | 1,25 kg/m3 |
| Starea de agregare | gazoasă |
| Punct de topire | −164 °C |
| Punct de fierbere | −152 °C |
| Solubilitate | în apă (60 mg/l) |
| Presiune de vapori | 34 atm[2] |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
În aer, fiind un radical liber instabil, monoxidul de azot se transformă în dioxid de azot (NO2, o noxă). Folosirea masivă în ultimul secol și ceva a motoarelor cu ardere internă, alături de arderea de combustibili fosili pentru generarea de electricitate, crește contribuția antropică (48 milioane de tone anual) la concentrația atmosferică totală a monoxidului de azot la aproximativ 5% din total.[3].
Natural, monoxidul de azot este produs prin acțiunea bacteriană în sol (responsabilă de emisia atmosferică a 990 milioane de tone anual) și datorită descărcărilor electrice în atmosferă (fulgere).
Concentrația atmosferică a monoxidului de azot este rezultatul unui echilibru dinamic datorat unor serii de reacții în care este implicat oxigenul molecular (O2) și ozonul (O3, din straturile inferioare ale atmosferei) prin care mono- și di-oxidul de azot se transformă reciproc unul în celălalt.
Activitatea chimică a moleculei de monoxid de azot este și mai evidentă decât în aer în soluțiile apoase, timpul de înjumătățire al acestei molecule fiind în sânge (un exemplu de soluție apoasă, unde molecula de monoxid îndeplinește importante funcții fiziologice) de doar câteva secunde.