
Carboran
From Wikipedia, the free encyclopedia
Carboranul este un compus de tip cluster a borului cu carbonul: Face parte din clasa boranilor avînd ca și aceștia structură poliedrică fiind similar clasificați în closo-, nido-, arachno-, hipho-, etc. în funcție de repezentarea unui poliedru complet(closo-) sau a unuia căruia îi lipsesc una (nido-), două (arachno-), sau mai multe vertexuri. Unul dintre cei mai cercetat carboran este un compus extrem de stabil cu simetrie icosaedrică closo-carboranul.[1]
| Acest articol (sau secțiunea de mai jos) conține greșeli de ortografie sau de punctuație. Puteți consulta manualul de stil și contribui prin corectarea greșelilor. |

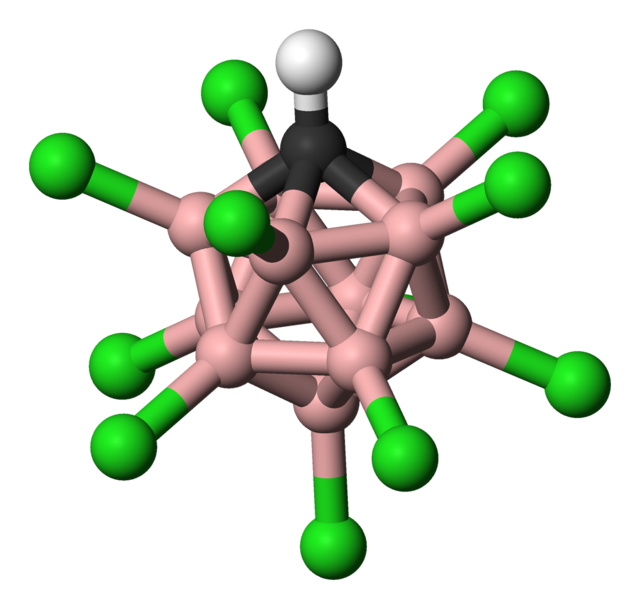
Legendă:
hidrogen − alb,
clor − verde,
bor − roz,
carbon − negru.
Un alt exemplu este cel al C2B10H12 sau o-carboran compus neutru din punct de vedere electric, carboran utilizat în cele mai diverse domenii de la polimeri termorezistenți pînă la domeniul medical. O-carboranul este denumit compus superaromatic deoarece se supune regulii lui Huckel, având o stabilitate termică mare.la fel ca și arenele carboranii suferă reacții de substituție electrofilă.
Un carboran puternic electronegativ este CHB11H12−, utilizat în sinteza superacizilor.
Carboran superacid H(CHB11Cl11)[2] este de circa 1 milion de ori mai puternic decât acidul sulfuric fumans.Această aciditate extrem de puternică este dată de anionul acid CHB11Cl11−, extrem de stabil și care poate fi substituit cu substituenți electronegativi. H(CHB11Cl11) este uncil acid cunoscut care poate protona C60 fulerenă fără a le descompune.[3][4]. De asemenea este unicul anion capabil să formeze o sare stabilă cu benzenul protonat C6H7+.
