compus chimic From Wikipedia, the free encyclopedia
Amoniacul este un compus chimic format dintr-un atom de azot și trei atomi de hidrogen. Denumirea provine de la clorura de amoniu, care a fost pentru prima dată descoperită în „Oaza lui Ammon” azi „Oaza Siwa”, Egipt. Starea de agregare a amoniacului fiind gazoasă, având proprietățile chimice unei baze, toxice cu miros înțepător, mai ușor ca aerul.
| Acest articol sau această secțiune are bibliografia incompletă sau inexistentă. Puteți contribui prin adăugarea de referințe în vederea susținerii bibliografice a afirmațiilor pe care le conține. |
| Amoniac | |
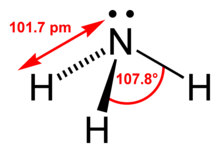 Structura moleculei de amoniac | |
 | |
| Denumiri | |
|---|---|
| Alte denumiri | Soluție de amoniac |
| Identificare | |
| Număr CAS | 7664-41-7 |
| ChEMBL | CHEMBL1160819 |
| PubChem CID | 222 |
| Informații generale | |
| Formulă chimică | NH3 |
| Aspect | gaz incolor |
| Masă molară | 17 g/mol |
| Proprietăți | |
| Densitate | 0,7198 kg/m3 |
| Starea de agregare | gaz |
| Punct de topire | -77,73 |
| Punct de fierbere | -33,5 |
| Solubilitate | 541 g/l |
| Anion | Azot |
| Cation | Hidrogen |
| Duritate (Scara Mohs) | - |
| Presiune de vapori | 8,5 atm[2] |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Amoniacul are un important rol, fiind precursor sau constituent al multor compuși organici, printre care se numără: aminele, amidele, aminoacizii (și de aici peptide, proteine) etc.
Amoniacul este ușor solubil în apă la temperatura de 0 °C, se dizolvă 90,7 g amoniac în 100 ml de apă, soluție cu un miros înțepător și cu o reacție alcalină.
Amoniacul lichid dizolvă metale alcaline, alcalino-pământoase și aluminiu.
Amoniacul sub formă de gaz într-un amestec între 15,5 - 30 % cu aerul este exploziv. La contactul cu suprafețe cu o temperatură de peste 630 °C se descompune în apă și azot, reacție de descompunere care este catalizată prin prezența unui metal, care coboară temperatura de descompunere de la 630 °C la 300 °C.
Amoniacul gaz are acțiune caustică în contact cu suprafețele umede, fiind iritant al pielii, mucoaselor căilor respiratorii, digestive sau ochilor. O concentrație de amoniac de 0,5% în aerul inspirat produce în timp de 30-60 de minute moartea.
Molecula de amoniac are o structură piramidal-trigonală, având suprafețe tetraedrice, care au în colț un atom de azot cu o pereche liberă de electroni. Amoniacul are un caracter amfoter, formează baze prin acceptare de protoni dând naștere la ioni a sărurilor de amoniu, sau are proprietăți acide prin pierdere de protoni în prezența bazelor tari formând ioni de amide:
Producerea pe scară industrială a amoniacului este realizată într-un procent de 90 % din azot și hidrogen (în raport de 1:3) după procedeul Haber-Bosch, procedeu descoperit de chimiștii germani Fritz Haber (1868–1934) și Carl Bosch (1874–1940).
Acest procedeu obține amoniacul dintr-un amestec gazos de hidrogen și azot, în prezența unui catalizator de oxid de fier Fe3O4, K2O, CaO, Al2O3 și bioxid de siliciu SiO2 supus la o presiune de 300 bari și o temperatură de 450 °C.
Amoniacul este unul din produsele principale ale industriei chimice. În prezent producția mondială de amoniac ajunge la cca. 125 milioane tone, pentru această producție fiind necesară 3% din energia mondială.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.