
Kalmodulina
Z Wikipedii, wolnej encyclopedia
Kalmodulina (ang. calcium-modulated protein, CaM, "białko modulowane przez wapń") – małe (16,7 kDa) białko modulatorowe, powszechnie występujące w organizmach eukariotycznych[1], o konserwatywnej ewolucyjnie strukturze: składa się z jednego łańcucha polipeptydowego o długości 148 reszt aminokwasowych. Odkryte w 1970 r. równocześnie przez dwa zespoły badaczy, zyskało stosowaną dziś nazwę w 1979[2].
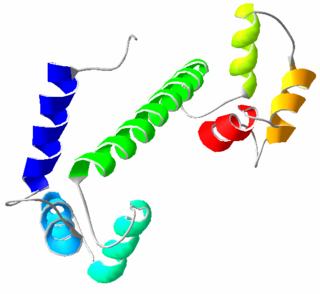

Uczestniczy w indukcji różnych szlaków sygnalizacji wewnątrzkomórkowej, odgrywając przez to rolę w podstawowych procesach fizjologicznych komórki takich jak wzrost, podział, różnicowanie i ruchliwość[3].
Wiązanie czterech jonów wapnia (Ca2+), po dwa w dwóch domenach typu dłonie EF (ang. EF hands) powoduje zmianę jej konformacji tym samym odsłaniając rejony hydrofobowe białka, co umożliwia jego interakcję z innymi białkami docelowymi[4]. Są nimi zarówno enzymy (np. dehydrogenaza chinianowa i kinaza II, która następnie fosforyluje inne białka)[1], jak i białka nieenzymatyczne, m.in. związane z reorganizacją cytoszkieletu (spektryna, kaldesmon), stablilnością mikrotubul (MAP 2, Tau)[2], czy w neuronach białka związane z błoną komórkową (neurogranina, neuromodulina). Wpływa też na pompy błonowo-jonowe[1]. Kalmodulina bierze udział w wygaszaniu sygnału wapniowego po rozpoczęciu kaskady sygnalizacji, aktywując Ca2+-ATPazy oraz pompy wapniowe SERCA[5]. Może również modulować cykl komórkowy, wywołując jego zatrzymanie w fazie G1, poprzez oddziaływanie z p21cip1 zależne od różnych czynników zewnątrzkomórkowych[6].
Rejony N- i C-końcowe białka wiążą Ca2+ ze zróżnicowanym powinowactwem (Kd odpowiednio 10-6 i 10-7) , a wartości te pokrywają się z typowym stężeniem jonów wapnia w komórce. Różnica ta sprawia, że w komórkach pobudliwych CaM może oddziaływać z różnymi białkami w stanie spoczynku komórki, gdy stężenie Ca2+ jest niskie[7].