sebatian kimia, komponen baja dan bahan letupan From Wikipedia, the free encyclopedia
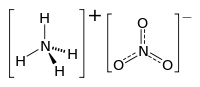
Ammonium nitrat ialah sebatian kimia dengan formula kimia NH4NO3 yang berwarna putih serta sangat larut dalam air. Sebatian ini terdiri daripada kation ammonium dan anion nitrat.
 | |
 | |
 | |
| Nama | |
|---|---|
| Nama IUPAC
Ammonium nitrat | |
| Pengecam | |
Imej model 3D Jmol |
|
| ChemSpider | |
| ECHA InfoCard | 100.026.680 |
| Nombor EC |
|
PubChem CID |
|
| Nombor RTECS |
|
| UNII | |
| Nombor PBB | 0222 – dengan > 0.2% bahan mudah terbakar 1942 – dengan <= 0.2% bahan mudah terbakar 2067 – baja 2426 – cecair |
CompTox Dashboard (EPA) |
|
| |
| |
| Sifat | |
| NH4NO3 | |
| Jisim molar | 80.043 g/mol |
| Rupa bentuk | Pepejal putih atau kelabu |
| Ketumpatan | 1.725 g/cm3 (20 °C) |
| Takat lebur | 169.6 °C (337.3 °F; 442.8 K) |
| Takat didih | anggaran 210 °C (410 °F; 483 K) Terurai |
| Endotermik 118 g/100 ml (0 °C) 150 g/100 ml (20 °C) 297 g/100 ml (40 °C) 410 g/100 ml (60 °C) 576 g/100 ml (80 °C) 1024 g/100 ml (100 °C)[1] | |
| -33.6·10−6 cm3/mol | |
| Struktur | |
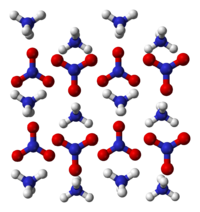
| Struktur kristal | Trigonal |
| Data bahan letupan | |
| Kepekaan kejutan | Amat rendah |
| Kepekaan geseran | Amat rendah |
| Detonation velocity | 2500 m/s |
| Bahaya | |
| Bahaya-bahaya utama | Bahan letupan, pengoksidaan |
| Piktogram GHS |    |
| Perkataan isyarat GHS | Danger |
Penyata bahaya GHS |
H201, H271, H319 |
Penyata pencegahan GHS |
P220, P221, P271, P280, P264, P372 |
| NFPA 704 (berlian api) | |
| Dos maut (LD) atau kepekatan dos maut (LC) | |
LD50 (median dos) |
2085–5300 mg/kg (tikus, oral)[2] |
| Sebatian berkaitan | |
Anion lain |
Ammonium nitrit |
Kation lain |
Natrium nitrat Kalium nitrat Hidroksilammonium nitrat |
Sebatian berkaitan |
Ammonium perklorat |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Sebatian ini biasanya digunakan dalam bidang pertanian sebagai baja nitrogen.[4] Tambahan pula, sebatian ini juga digunakan sebagai bahan letupan dalam bidang pelombongan dan pembinaan awam.
Ammonium nitrat dihasilkan dalam industri melalui tindak balas asid dan bes, yakni antara ammonia dan asid nitrik.[5]
Ammonium nitrat bertindak balas dengan hidroksida logam untuk menghasilkan ammonia dan nitrat logam alkali. Dalam persamaan di bawah, M mewakili logam alkali seperti natrium dan kalium.
Ammonium nitrat akan terurai menjadi nitrus oksida dan air apabila dipanaskan.
Walau bagaimanapun, dalam letupan atau pembakaran pantas, ammonium nitrat akan terurai menjadi gas nitrogen, gas oksigen dan air.
Ammonium nitrat terurai menjadi nitrus oksida dan wap air apabila dipanaskan, tetapi boleh terurai secara letupan. Sifat ammonium oksida sebagai pengoksida boleh memarakkan letupan dengan mudah, menjadikan ammonium nitrat memiliki risiko kebakaran yang besar.
Letupan kecil yang melibatkan ammonium hidroksida adalah agak lazim, tetapi beberapa bencana besar pernah direkodkan seperti:
Sesetengah daripada letupan ini direkodkan sebagai salah satu letupan bukan nuklear terbesar yang pernah dicatat.
Ammonium nitrat tidak berbahaya kepada kesihatan dan biasanya digunakan dalam produk baja. [10] [11] [12]
Ammonium nitrat mempunyai LD 50 bagi setiap 2217 mg/kg, [13] yang mana sebagai perbandingan adalah kira-kira dua pertiga daripada garam meja sahaja.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.