From Wikipedia, the free encyclopedia
ദൃശ്യ മണ്ഡലത്തിൻ്റെ അതായത് വിഷ്വൽ ഫീൽഡിന്റെ മധ്യഭാഗത്തെ കാഴ്ച നഷ്ടപ്പെടുന്ന ഒരു മെഡിക്കൽ അവസ്ഥയാണ് മാക്യുലാർ ഡീജനറേഷൻ. ഇത് പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലാർ ഡീജനറേഷൻ (എഎംഡി /എആർഎംഡി) എന്നും അറിയപ്പെടുന്നു.[1] ഈ അസുഖത്തിന് തുടക്കത്തിൽ പലപ്പോഴും ലക്ഷണങ്ങളൊന്നും ഉണ്ടാകില്ല. എന്നാൽ കാലക്രമേണ, ഒരു കണ്ണിലെയോ രണ്ട് കണ്ണിലെയോ കാഴ്ച കുറഞ്ഞു വരുന്നു. ഇത് സാധാരണയായി പൂർണ്ണമായ അന്ധതയ്ക്ക് കാരണമാകുന്ന രോഗം അല്ലെങ്കിലും, കേന്ദ്ര കാഴ്ച നഷ്ടപ്പെടുന്നത് മൂലം മുഖങ്ങൾ തിരിച്ചറിയാനോ, ഡ്രൈവ് ചെയ്യാനോ, വായിക്കാനോ, ദൈനംദിന ജീവിതത്തിലെ മറ്റ് പ്രവർത്തനങ്ങൾ നടത്തുന്നതിനോ ഒക്കെ പ്രയാസം ഉണ്ടാക്കിയേക്കാം. മാക്യുലർ ഡീജനറേഷൻ വന്നവരിൽ ചിലപ്പോൾ വിഷ്വൽ ഹാലൂസിനേഷൻ സംഭവിക്കാം, പക്ഷേ ഇവ ഒരു മാനസികരോഗത്തെ പ്രതിനിധീകരിക്കുന്നില്ല.
| മാക്യുലാർ ഡീജനറേഷൻ | |
|---|---|
| മറ്റ് പേരുകൾ | പ്രായവുമായിബന്ധപ്പെട്ട മാക്യുലാർ ഡീജനറേഷൻ |
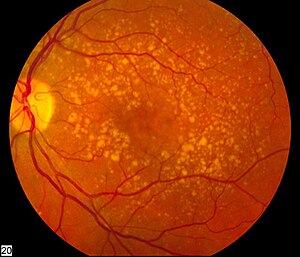 | |
| ഇന്റർമീഡിയറ്റ് മാക്യുലാർ ഡീജനറേഷൻ കാണിക്കുന്ന റെറ്റിന ചിത്രം | |
| സ്പെഷ്യാലിറ്റി | നേത്ര വിജ്ഞാനം |
| ലക്ഷണങ്ങൾ | കാഴ്ച മണ്ഡലത്തിന്റെ മധ്യ ഭാഗത്തുള്ള മങ്ങിയ കാഴ്ച or കാഴ്ച നഷ്ടം[1] |
| സങ്കീർണത | വിഷ്വൽ ഹാലൂസിനേഷൻ[1] |
| സാധാരണ തുടക്കം | പ്രായാധിക്യം[1] |
| തരങ്ങൾ | ഏർളി, ഇന്റർമീഡിയറ്റ്, ലേറ്റ്[1] |
| കാരണങ്ങൾ | റെറ്റിനയിലെ മാക്യുലയ്ക്ക് ഉണ്ടാകുന്ന തകരാറ്[1] |
| അപകടസാധ്യത ഘടകങ്ങൾ | ജനിതകം, പുകവലി[1] |
| ഡയഗ്നോസ്റ്റിക് രീതി | നേത്ര പരിശോധന[1] |
| പ്രതിരോധം | വ്യായാമം, ആരോഗ്യകരമായ ഭക്ഷണ ശീലങ്ങൾ, പുകവലി ഒഴിവാക്കുക[1] |
| Treatment | കണ്ണിലേക്ക് കുത്തിവെക്കുന്നആന്റി വിഇജി എഫ് മരുന്നുകൾ, ലേസർ കൊയാഗുലേഷൻ, ഫോട്ടോഡൈനാമിക് തെറാപ്പി[1] |
| ആവൃത്തി | 6.2 മില്യൺ (2015)[2] |
പ്രായമായവരിൽ ആണ് മാക്യുലർ ഡീജനറേഷൻ സാധാരണ സംഭവിക്കാറുള്ളത്.[1] ജനിതക ഘടകങ്ങളും, പുകവലിയും ഇതിൽ ഒരു പങ്കു വഹിക്കുന്നു. റെറ്റിനയുടെ മാക്യുലയ്ക്ക് കേടുപാടുകൾ സംഭവിക്കുന്നതാണ് ഇതിന് കാരണം. പൂർണ്ണമായ നേത്ര പരിശോധനയിലൂടെ രോഗനിർണ്ണയം സാധ്യമാണ്. തീവ്രതയ്ക്കനുസരിച്ച് ഈ രോഗം 'ഏർളി', 'ഇന്റർമീഡിയറ്റ്', 'ലേറ്റ്' എന്നിങ്ങനെ മൂന്നായി തരം തിരിച്ചിരിക്കുന്നു. ലേറ്റ് മാക്യുലർ ഡീജനറേഷൻ "ഡ്രൈ", "വെറ്റ്" രൂപങ്ങളായി വീണ്ടും വിഭജിക്കപ്പെട്ടിട്ടുണ്ട്. ഡ്രൈ വിഭാഗത്തിൽ ആണ് 90% കേസുകളും ഉൾപ്പെടുന്നത്.[3]
വ്യായാമം, പോഷക സമൃദ്ധമായ ഭക്ഷണം കഴിക്കുക, പുകവലി ഒഴിവാക്കുക എന്നിങ്ങനെയുള്ള കാര്യങ്ങൾ ഈ രോഗത്തെ പ്രതിരോധിക്കാറുണ്ട്.[1] പക്ഷെ ഇതു മൂലം നഷ്ടപ്പെട്ട കാഴ്ചയെ തിരികെ നൽകുന്ന ഒരു ചികിത്സ നിലവിൽ ഇല്ല. വെറ്റ് രോഗാവസ്ഥയിൽ, കണ്ണിലേക്ക് കുത്തിവയ്ക്കുന്ന ആന്റി-വിഇജിഎഫ് മരുന്നുകൾ അല്ലെങ്കിൽ ലേസർ കൊയാഗ്യുലേഷൻ, ഫോട്ടോഡൈനാമിക് തെറാപ്പി എന്നീ ചികിൽസാരീതികൾ കാഴ്ച വീണ്ടും മോശമാകുന്ന തോത് മന്ദഗതിയിലാക്കാം. ആന്റിഓക്സിഡൻ്റുകളും, വിറ്റാമിനുകളും, ധാതുക്കളും രോഗ പ്രതിരോധത്തിന് ഉപയോഗപ്രദമാണെന്ന് പറയുന്നില്ല.[4] എന്നിരുന്നാലും, ഡയറ്ററി സപ്ലിമെൻറുകൾ ഇതിനകം രോഗം ഉള്ളവരിൽ രോഗ പുരോഗതിയെ മന്ദഗതിയിലാക്കിയേക്കാം. [5]
2015 ൽ ഇത് ആഗോളതലത്തിൽ 6.2 ദശലക്ഷം ആളുകളെ ബാധിച്ചു എന്നാണ് കണക്കായിരിക്കുന്നത്.[2] 2013 ലെ കണക്ക് പ്രകാരം തിമിരം, മാസം തികയാതെയുള്ള ജനനം, ഗ്ലോക്കോമ എന്നിവയ്ക്ക് ശേഷമുള്ള അന്ധതയുടെ ഏറ്റവും സാധാരണമായ നാലാമത്തെ കാരണമാണ് ഇത്.[6] ഇത് സാധാരണയായി അമ്പത് വയസ്സിനു മുകളിലുള്ളവരെയാണ് ബാധിക്കുന്നത്, അമേരിക്കയിൽ ഈ പ്രായത്തിലുള്ളവരിലെ കാഴ്ച നഷ്ടത്തിൻറെ ഏറ്റവും സാധാരണ കാരണം ഇതാണ്.[1] [3] 50 നും 60 നും ഇടയിൽ പ്രായമുള്ളവരിൽ 0.4% പേർക്ക് ഈ രോഗം ഉണ്ട്, അതേസമയം 60 മുതൽ 70 വരെ ആളുകളിൽ 0.7%, ആളുകൾക്ക് 70 നും 80 നും ഇടയിൽ 2.3% ആളുകൾക്ക്, 80 വയസ്സിനു മുകളിലുള്ള വരിൽ 12% എന്നിങ്ങനെ ഇത് സംഭവിക്കുന്നു.


മാക്യുലർ ഡീജനറേഷന്റെ ലക്ഷണങ്ങളും അടയാളങ്ങളും താഴെ പറയുന്നവയാണ്:
മാക്യുലർ ഡീജനറേഷൻ പൂർണ്ണമായ അന്ധതയിലേക്ക് നയിക്കില്ല. ശരിക്കും പറഞ്ഞാൽ കാഴ്ച വൈകല്യമുള്ള വളരെ കുറച്ച് ആളുകൾ മാത്രമാണ് പൂർണ്ണമായും അന്ധർ. മിക്കവാറും എല്ലാവരിലും എല്ലാ സാഹചര്യങ്ങളിലും, ചില കാഴ്ച (പ്രധാനമായും പെരിഫറൽ കാഴ്ച) അവശേഷിക്കുന്നുണ്ടാവാം. ഗ്ലോക്കോമ പോലെയുള്ള സങ്കീർണ്ണമായ മറ്റ് അവസ്ഥകൾ പൂർണ്ണമായ അന്ധതയ്ക്ക് കാരണമാവാം, എന്നാൽ മാക്യുലർ ഡീജനറേഷൻ രോഗികൾക്ക് പൂർണ്ണമായി കാഴ്ചശക്തി നഷ്ടപ്പെടുന്നത് അപൂർവ്വമാണ്.[8]
മാക്കുലയുടെ വിസ്തീർണ്ണം റെറ്റിനയുടെ ആകെ വിസ്തീർണ്ണത്തിൻറെ 2.1% മാത്രമേയുള്ളൂ, ശേഷിക്കുന്ന 97.9% (പെരിഫറൽ ഫീൽഡ്) ഈ രോഗത്തെ ബാധിക്കുന്നില്ല. വിഷ്വൽ ഫീൽഡിന്റെ വളരെ ചെറിയ ഭാഗം മാത്രമാണ് മാക്യുലയ്ക്കുള്ളത് എങ്കിലും, വിഷ്വൽ കോർട്ടെക്സിന്റെ പകുതിയോളം ഭാഗം മാക്യുലർ വിവരങ്ങൾ പ്രോസസ്സ് ചെയ്യുന്നതിനായി നീക്കിവച്ചിരിക്കുന്നു.[9]
കേന്ദ്ര കാഴ്ച നഷ്ടപ്പെടുന്നത് വിഷ്വൽ പ്രവർത്തനത്തെ സാരമായി തന്നെ ബാധിക്കുന്നു. കേന്ദ്ര കാഴ്ചയില്ലാതെ പുസ്തകങ്ങളും മറ്റും വായിക്കുന്നത് തികച്ചും ബുദ്ധിമുട്ടാണ്. മാക്യുലർ ഡീജനറേഷന്റെ കേന്ദ്ര കാഴ്ച നഷ്ടത്തെ ഒരു കറുത്ത പുള്ളി ഉപയോഗിച്ച് കാണിക്കാൻ ശ്രമിക്കുന്ന ചിത്രങ്ങൾ (മുകളിൽ കോടുത്തര് പോലെ) യഥാർഥത്തിൽ ശരിക്കുള്ള വിഷ്വൽ നഷ്ടത്തിന്റെ വിനാശകരമായ സ്വഭാവത്തോട് നീതി പുലർത്തുന്നില്ല. ഒരു കടലാസിൽ അച്ചടിച്ച ആറ് ഇഞ്ച് ഉയരമുള്ള അക്ഷരങ്ങൾ, കണ്ണി നേരെ മുന്നിൽ പേപ്പർ ചരിച്ച് പിടിച്ച് വായിക്കാൻ ശ്രമിക്കുന്നതിലൂടെ ഇത് ഏകദേശം മനസ്സിക്കാം. മിക്ക ആളുകൾക്കും ഇത് ചെയ്യാൻ ബുദ്ധിമുട്ടാണ്.
കൂടാതെ, ഡ്രൈ മാക്യുലർ ഡീജനറേഷൻ ഉള്ള ആളുകൾക്ക് പലപ്പോഴും രോഗലക്ഷണങ്ങൾ അനുഭവപ്പെടില്ല, പക്ഷേ ഒന്നോ രണ്ടോ കണ്ണുകളിൽ മങ്ങിയ കാഴ്ചയുടെ ക്രമേണയുള്ള തുടക്കം അനുഭവപ്പെടാം.[10] [11] വെറ്റ് മാക്യുലർ ഡീജനറേഷൻ ഉള്ള ആളുകൾക്ക് തീവ്രമായ വിഷ്വൽ ലക്ഷണങ്ങൾ അനുഭവപ്പെടാം.
ബാധിത വ്യക്തിയുടെ സഹോദരങ്ങൾക്കുള്ള ആവർത്തന അനുപാതം സാധാരണ ജനസംഖ്യയേക്കാൾ മൂന്ന് മുതൽ ആറ് മടങ്ങ് വരെ കൂടുതലാണ്. [22] ജനിതക ലിങ്കേജ് വിശകലനത്തിലൂടെ വ്യത്യസ്ത ക്രോമസോമുകളിൽ (1, 6, 10) മൂന്ന് സ്ഥലങ്ങളിൽ 5 സെറ്റ് ജീൻ വകഭേദങ്ങൾ കണ്ടെത്തി, ഇത് കുറഞ്ഞത് 50% അപകടസാധ്യത വിശദീകരിക്കുന്നു. ഈ ജീനുകൾക്ക് രോഗപ്രതിരോധ പ്രതികരണം, കോശജ്വലന പ്രക്രിയകൾ, റെറ്റിനയുടെ ഹോമിയോസ്റ്റാസിസ് എന്നിവ നിയന്ത്രിക്കുന്ന റോളുകളുണ്ട്. ഈ ജീനുകളുടെ വകഭേദങ്ങൾ ഈ പ്രക്രിയകളിൽ പലതരം അപര്യാപ്തതകൾക്ക് കാരണമാകുന്നു. കാലക്രമേണ, ഇത് മൂലം ഇൻട്രാ സെല്ലുലാർ, എക്സ്ട്രാ സെല്ലുലാർ മെറ്റബോളിക് അവശിഷ്ടങ്ങൾ അടിഞ്ഞു കൂടുന്നു. ഇത് റെറ്റിനയിൽ പാടുകൾ ഉണ്ടാക്കുകയോ വാസ്കുലറൈസേഷന്റെ തകർച്ചയ്ക്ക് കാരണമാകുകയോ ചെയ്യും.
ഈ ജീൻ വ്യതിയാനങ്ങളിൽ ചിലത് തിരിച്ചറിയാൻ ജനിതക പരിശോധനകൾ ലഭ്യമാണ്. എന്നിരുന്നാലും, ജനിതകശാസ്ത്രം, പരിസ്ഥിതി, ജീവിതശൈലി എന്നിവ തമ്മിലുള്ള സങ്കീർണ്ണമായ ഇടപെടലാണ് മാക്യുലർ ഡീജനറേഷന്റെ രോഗകാരി, അതിനാൽ തന്നെ അനുകൂലമല്ലാത്ത ജനിതക ഘടകങ്ങളുടെ സാന്നിധ്യം കൊണ്ട് മാത്രം രോഗത്തിൻറെ പുരോഗതി പ്രവചിക്കാൻ സാധ്യമല്ല. തിരിച്ചറിഞ്ഞ ജീൻ വകഭേദങ്ങൾ കണ്ടെത്തിയ മൂന്ന് ലോക്കികൾ ഇനിപ്പറയുന്നവയാണ്::
മേൽ പറഞ്ഞത് MT-ND2 തന്മാത്രയിൽ ഉണ്ടെങ്കിൽ വെറ്റ് എഎംഡിക്ക് സാധ്യതയുണ്ട്.[30]

ഓക്സിഡേറ്റീവ് സ്ട്രെസ്, മൈറ്റോകോണ്ട്രിയൽ ഡിസ്ഫംഗ്ഷൻ, കോശജ്വലന പ്രക്രിയകൾ എന്നിവയുൾപ്പെടെ ചില സിദ്ധാന്തങ്ങൾ മുന്നോട്ട് വച്ചിട്ടുണ്ടെങ്കിലും പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷന്റെ രോഗകാരിയെക്കുറിച്ച് കൂടുതൽ അറിവില്ല.
കേടായ സെല്ലുലാർ ഘടകങ്ങളുടെ ഉൽപാദനവും അധപതനവും തമ്മിലുള്ള അസന്തുലിതാവസ്ഥ, ഇൻട്രാ സെല്ലുലാർ ലിപ്പോഫുസ്സിൻ, എക്സ്ട്രാ സെല്ലുലാർ ഡ്രുസെൻ പോലെയുള്ള ദോഷകരമായ ഉൽപ്പന്നങ്ങളുടെ ശേഖരണത്തിലേക്ക് നയിക്കുന്നു. എഎംഡിയുടെ പ്രാരംഭ ഘട്ടത്തിൽ ജോഗ്രഫിക്കൽ അട്രോഫിക്ക് മുമ്പുള്ള റെറ്റിനൽ പിഗ്മെൻറ് എപ്പിത്തീലിയം (ആർപിഇ) കനം കുറയൽ അല്ലെങ്കിൽ ഡിപിഗ്മെൻറേഷൻ മേഖലകളാണ് ഇൻസിപിയന്റ് അട്രോഫി എന്ന് വിളിക്കുന്നത്. എഎംഡിയുടെ വിപുലമായ ഘട്ടങ്ങളിൽ, ആർപിഇയുടെ അട്രോഫി (ജിയോഗ്രാഫിക് അട്രോഫി) കൂടാതെ / അല്ലെങ്കിൽ പുതിയ രക്തക്കുഴലുകളുടെ വളർച്ച (നിയോവാസ്കുലറൈസേഷൻ) എന്നിവയുടെ ഫലമായി ഫോട്ടോറിസെപ്റ്ററുകളുടെ മരണത്തിനും കേന്ദ്ര കാഴ്ച നഷ്ടത്തിനും കാരണമാകുന്നു.
ഡ്രൈ (നോൺ എക്സുഡേറ്റീവ്) രൂപത്തിൽ, ഡ്രൂസെൻ എന്നറിയപ്പെടുന്ന സെല്ലുലാർ അവശിഷ്ടങ്ങൾ റെറ്റിനയ്ക്കും കോറോയിഡിനുമിടയിൽ അടിഞ്ഞു കൂടുന്നു, ഇത് റെറ്റിനയിൽ അട്രോഫിയും പാടുകളും ഉണ്ടാക്കുന്നു. കൂടുതൽ കഠിനമായ വെറ്റ് (എക്സുഡേറ്റീവ്) രൂപത്തിൽ, റെറ്റിനയുടെ പിന്നിലുള്ള കോറോയിഡിൽ നിന്ന് രക്തക്കുഴലുകൾ വളരുന്നു (നിയോവാസ്കുലറൈസേഷൻ) , ഇത് എക്സുഡേറ്റും ദ്രാവകവും ചോർന്ന് രക്തസ്രാവത്തിനും കാരണമാകുന്നു.
ഇമ്മ്യൂൺ മീഡിയേറ്ററുകളുടെ ഒരു കൂട്ടം ഡ്രൂസനിൽ ധാരാളം ഉണ്ടെന്ന് ആദ്യകാല പ്രവർത്തനങ്ങൾ തെളിയിച്ചിട്ടുണ്ട്.[31] കോംപ്ലിമെന്റ് ഫാക്ടർ എച്ച് (സിഎഫ്എച്ച്) ഈ കോശജ്വലന കാസ്കേഡിന്റെ ഒരു പ്രധാന തടസ്സമാണ്, കൂടാതെ സിഎഫ്എച്ച് ജീനിലെ രോഗവുമായി ബന്ധപ്പെട്ട പോളിമോർഫിസം എഎംഡിയുമായി ശക്തമായി ബന്ധപ്പെട്ടിരിക്കുന്നു.[32] [33] [34] [35] [36] അങ്ങനെ ക്രോണിക് ലോ ഗ്രേഡ് കോംപ്ലിമെന്റ് ആക്റ്റിവേഷന്റെയും മാക്യുലയിലെ വീക്കത്തിന്റെയും എഎംഡി പാത്തോഫിസിയോളജിക്കൽ മോഡൽ വികസിപ്പിച്ചെടുത്തു.[37] [38] കോംപ്ലിമെന്റ് ഘടകം 3 (സി 3) ഉൾപ്പെടെയുള്ള കോംപ്ലിമെന്റ് കാസ്കേഡിന്റെ മറ്റ് ഘടകങ്ങളിൽ രോഗവുമായി ബന്ധപ്പെട്ട ജനിതക പോളിമോർഫിസങ്ങൾ കണ്ടെത്തിയതാണ് ഇതിന് വിശ്വാസ്യത നൽകുന്നത്.[39]
എഎംഡിയുടെ ശക്തമായ പ്രവചനം എൽഒസി 387715 ൽ ക്രോമസോം 10q26 ൽ കണ്ടെത്തി. ഈ സൈറ്റിലെ ഉൾപ്പെടുത്തൽ / ഇല്ലാതാക്കൽ പോളിമോർഫിസം ARMS2 ജീനിന്റെ ആവിഷ്കാരത്തെ കുറയ്ക്കുന്നു, പക്ഷേ പോളിഅഡൈനിലേഷൻ സിഗ്നൽ ഇല്ലാതാക്കുന്നതിലൂടെ അതിന്റെ എംആർഎൻഎയെ അസ്ഥിരപ്പെടുത്തുന്നു.[40] ARMS2 പ്രോട്ടീൻ മൈറ്റോകോൺഡ്രിയയിലേക്ക് പ്രാദേശികവൽക്കരിക്കപ്പെടുകയും ഊർജ്ജ രാസവിനിമയത്തിൽ പങ്കാളികളാകുകയും ചെയ്യാം, എന്നിരുന്നാലും അതിന്റെ പ്രവർത്തനത്തെക്കുറിച്ച് ഇനിയും വളരെയധികം കണ്ടെത്താനുണ്ട്.
എഎംഡി പുരോഗതിയിൽ എക്സ്ട്രാ സെല്ലുലാർ മാട്രിക്സ് മെറ്റബോളിസത്തിന് ഒരു പങ്ക് നിർദ്ദേശിക്കുന്ന മെറ്റലോപ്രോട്ടിനേസ് 3 ( ടിഎംപി 3) ന്റെ ടിഷ്യു ഇൻഹിബിറ്റർ പുരോഗതി അപകടസാധ്യതയുടെ മറ്റ് ജീൻ മാർക്കറുകളിൽ ഉൾപ്പെടുന്നു.[41] കൊളസ്ട്രോൾ മെറ്റബോളിസിംഗ് ജീനുകളായ ഹെപ്പാറ്റിക് ലിപേസ്, കൊളസ്ട്രോൾ ഈസ്റ്റർ ട്രാൻസ്ഫേറസ്, ലിപ്പോപ്രോട്ടീൻ ലിപേസ്, എടിപി-ബൈൻഡിംഗ് കാസറ്റ് എ 1 എന്നിവ രോഗത്തിന്റെ പുരോഗതിയുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. രോഗത്തിന്റെ ആദ്യകാല ലക്ഷണമായ ഡ്രൂസെൻ കൊളസ്ട്രോൾ കൊണ്ട് സമ്പന്നമാണ്, ഇത് ജീനോം-വൈഡ് അസോസിയേഷൻ പഠനങ്ങളുടെ ഫലങ്ങൾക്ക് സാധുത നൽകുന്നു.[42]
എഎംഡിയിൽ റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിനും അന്തർലീനമായ കോറോയിഡിനുമിടയിൽ, മാക്യുലയിൽ (റെറ്റിനയുടെ ഒരു ഭാഗം) ഡ്രൂസെൻ (എക്സ്ട്രാ സെല്ലുലാർ പ്രോട്ടീനുകളുടെയും ലിപിഡുകളുടെയും നിർമ്മാണം) എന്ന സ്വഭാവ സവിശേഷതകളുള്ള മഞ്ഞ നിക്ഷേപങ്ങൾ പുരോഗമിക്കുന്നു. ഈ ശേഖരണം കാലക്രമേണ റെറ്റിനയെ തകരാറിലാക്കുമെന്ന് വിശ്വസിക്കപ്പെടുന്നു. എഎംഡിയിൽ അടിഞ്ഞുകൂടുന്ന പ്രോട്ടീനുകളിലൊന്നാണ് അൽഷിമേഴ്സ് രോഗത്തിൽ തലച്ചോറിൽ വളരുന്ന അമിലോയിഡ് ബീറ്റ, ഇത് കാരണം എഎംഡിയെ ചിലപ്പോൾ "കണ്ണിന്റെ അൽഷിമേഴ്സ്" അല്ലെങ്കിൽ "റെറ്റിനയുടെ അൽഷിമേഴ്സ്" എന്ന് വിളിക്കുന്നു.[43] ഡ്രൂസന്റെ വ്യാപ്തിയെ (വലുപ്പവും എണ്ണവും) ഭാഗികമായി അടിസ്ഥാനമാക്കി എഎംഡിയെ, ഏർളി, ഇന്റർമീഡിയറ്റ്, ലേറ്റ് എന്നിങ്ങനെ 3 ഘട്ടങ്ങളായി തിരിക്കാം. [1]
റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിനും അന്തർലീനമായ കോറോയിഡിനുമിടയിൽ മാക്യുലയിലെെ ചെറിയ മഞ്ഞ നിക്ഷേപങ്ങളിൽ (ഡ്രൂസെൻ) എഎംഡി പത്തോളജി ആരംഭിക്കുന്നു. ഈ ആദ്യകാല മാറ്റങ്ങളുള്ള മിക്ക ആളുകൾക്കും നല്ല കാഴ്ചയുണ്ടാവും. ഡ്രൂസെൻ ഉള്ള ആളുകൾക്ക് മാക്യുലർ ഡീജനറേഷൻ ഉണ്ടാവാനും ഉണ്ടാവാതിരിക്കാനും സാധ്യതയുണ്ട്. വാസ്തവത്തിൽ, 60 വയസ്സിനു മുകളിലുള്ള ഭൂരിഭാഗം ആളുകളും പ്രതികൂല ഫലങ്ങളില്ലാതെ മദ്യപിക്കുന്നു. ഡ്രൂസൻ വലുതും കൂടുതലും ആണെങ്കിൽ ലക്ഷണങ്ങൾ ഉണ്ടാകാനുള്ള സാധ്യത കൂടുതലാണ്, ഇത് മാക്കുലയ്ക്ക് കീഴിലുള്ള പിഗ്മെന്റ് സെൽ പാളിയിലെ അസ്വസ്ഥതയുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. വലുതും മൃദുവായതുമായ ഡ്രൂസൻ ഉയർന്ന കൊളസ്ട്രോൾ നിക്ഷേപവുമായി ബന്ധപ്പെട്ടതാണെന്ന് കരുതപ്പെടുന്നു.
ഒരു ശരാശരി മനുഷ്യ മുടിയുടെ വീതിയോളമുള്ള ഇടത്തരം വലിപ്പമുള്ള ഡ്രൂസന്റെ സാന്നിധ്യം അടിസ്ഥാനമാക്കിയാണ് ആദ്യകാല എഎംഡി നിർണ്ണയിക്കുന്നത്. ആദ്യകാല എഎംഡിക്ക് സാധാരണയായി ലക്ഷണങ്ങളില്ല.[1]
വലിയ ഡ്രൂസൻ കൂടാതെ/അല്ലെങ്കിൽ ഏതെങ്കിലും റെറ്റിന പിഗ്മെന്റ് അസാധാരണതകൾ ഇവ ഒരുമിച്ചു വന്നാലാണ് ഇന്റർമീഡിയറ്റ് എഎംഡി എന്ന് പറയുന്നത്. ഇന്റർമീഡിയറ്റ് എഎംഡി മൂഒലം കുറച്ച് കാഴ്ച നഷ്ടപ്പെടാൻ കാരണമായേക്കാം, എന്നാലും ആദ്യകാല എഎംഡി പോലെ, ഇത് സാധാരണയായി അധികം ലക്ഷണങ്ങളില്ലാത്തതാണ്.[1] [44]
എഎംഡിയുടെ അവസാനത്തിൽ, മതിയായ റെറ്റിന കേടുപാടുകൾ സംഭവിക്കുന്നു, ഡ്രൂസന് പുറമേ, ആളുകൾക്ക് രോഗലക്ഷണമായ കേന്ദ്ര കാഴ്ച നഷ്ടം അനുഭവപ്പെടാൻ തുടങ്ങും. കാഴ്ച നഷ്ടത്തിന് കാരണം ഒന്നുകിൽ അട്രോഫിയുടെ വികസനം അല്ലെങ്കിൽ നിയോവാസ്കുലർ രോഗത്തിന്റെ ആരംഭം എന്നിവ ആകാം. നാശനഷ്ടങ്ങളെ അടിസ്ഥാനമാക്കി എഎംഡിയെ രണ്ട് ഉപവിഭാഗങ്ങളായി തിരിച്ചിരിക്കുന്നു: ജിയോഗ്രാഫിക് അട്രോഫി, വെറ്റ് എഎംഡി (നിയോവാസ്കുലർ എഎംഡി എന്നും ഇതിനെ വിളിക്കുന്നു). [44] [1]
നിയോവാസ്കുലർ (വെറ്റ് എഎംഡി) അല്ലാത്ത എല്ലാത്തരം എഎംഡികളെയും ഉൾക്കൊള്ളുന്ന വിശാലമായ പദവിയാണ് ഡ്രൈ എഎംഡി (നോൺഎക്സുഡേറ്റീവ് എഎംഡി എന്നും അറിയപ്പെടുന്നു). എഎംഡിയുടെ ആദ്യകാല, ഇന്റർമീഡിയറ്റ് രൂപങ്ങളും ജിയോഗ്രാഫിക് അട്രോഫി എന്നറിയപ്പെടുന്ന വരണ്ട എഎംഡിയുടെ വിപുലമായ രൂപവും ഇതിൽ ഉൾപ്പെടുന്നു. ഡ്രൈ എഎംഡി രോഗികൾക്ക് ആദ്യഘട്ടത്തിൽ കുറഞ്ഞ ലക്ഷണങ്ങളുണ്ടാകും; ഈ അവസ്ഥ ജോഗ്രഫിക്കൽ അട്രോഫിയിലേക്ക് മുന്നേറുകയാണെങ്കിൽ വിഷ്വൽ ഫംഗ്ഷൻ നഷ്ടം പലപ്പോഴും സംഭവിക്കാറുണ്ട്. ഡ്രൈ എഎംഡി 80-90% കേസുകൾക്ക് കാരണമാവുകയും സാവധാനത്തിൽ പുരോഗമിക്കുകയും ചെയ്യുന്നു. 10-20% ആളുകളിൽ, വരണ്ട എഎംഡി നനഞ്ഞ തരത്തിലേക്ക് പുരോഗമിക്കുന്നു.
ജിയോഗ്രാഫിക് അട്രോഫി (എട്രോഫിക് എഎംഡി എന്നും അറിയപ്പെടുന്നു) എഎംഡിയുടെ ഒരു നൂതന രൂപമാണ്, അതിൽ റെറ്റിന കോശങ്ങളുടെ സ്ഥായിയായ നഷ്ടം വിഷ്വൽ ഫംഗ്ഷൻ നഷ്ടപ്പെടുന്നതിലേക്ക് നയിക്കുന്നു. റെറ്റിനയെ നിർമ്മിക്കുന്ന ഒന്നിലധികം പാളികളുണ്ട്, ജിയോഗ്രഫിക്ക് അട്രോഫിയിൽ, അട്രോഫിക്ക് വിധേയമാകുന്ന മൂന്ന് നിർദ്ദിഷ്ട പാളികളുണ്ട്: കൊറിയോകാപിലറിസ്, റെറ്റിനൽ പിഗ്മെൻറ് എപ്പിത്തീലിയംം, ഫോട്ടോറിസെപ്റ്ററുകൾ എന്നിവയാണ് അത്.
ജിയോഗ്രഫിക്ക് അട്രോഫിയിൽ അട്രോഫിക്ക് വിധേയമാകുന്ന മൂന്ന് പാളികൾ എല്ലാം പരസ്പരം ചേർന്നാണ്. ഫോട്ടോറിസെപ്റ്ററുകൾ ഏറ്റവും പുറമേയുള്ളതാണ്, അവ പുറം ലോകത്തിൽ നിന്നുള്ള പ്രകാശത്തിൽ നിന്ന് ഊർജ്ജത്തെ തലച്ചോറിലേക്ക് അയയ്ക്കുന്നതിനുള്ള ഒരു വൈദ്യുത സിഗ്നലാക്കി മാറ്റാൻ കാരണമാകുന്ന കോശങ്ങളാണ്. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന്റെ നിരവധി പ്രവർത്തനങ്ങൾ ഉണ്ട്. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന്റെ പ്രധാന പ്രവർത്തനങ്ങളിലൊന്ന് ഓക്സിഡേറ്റീവ് സ്ട്രെസ് കുറയ്ക്കുക എന്നതാണ്. പ്രകാശം ആഗിരണം ചെയ്തുകൊണ്ട് അത് അങ്ങനെ ചെയ്യുന്നു, അങ്ങനെ അത് അടിസ്ഥാന പാളികളിലേക്ക് എത്തുന്നത് തടയുന്നു. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന് കീഴിലുള്ള പാളികൾ വളരെ വാസ്കുലറൈസ് ചെയ്തതിനാൽ അവയ്ക്ക് ഉയർന്ന ഓക്സിജൻ ടെൻഷനുണ്ട്. അതിനാൽ, പ്രകാശം ആ പാളികളിലേക്ക് എത്തുകയാണെങ്കിൽ, നിരവധി ഫ്രീ റാഡിക്കലുകൾ രൂപപ്പെടുകയും സമീപത്തുള്ള ടിഷ്യൂകൾക്ക് നാശമുണ്ടാക്കുകയും ചെയ്യും. ജിയോഗ്രഫിക്ക് അട്രോഫിയിൽ അട്രോഫിക്ക് വിധേയമാകുന്ന ഏറ്റവും ആഴത്തിലുള്ള പാളിയെ കൊറിയോകാപ്പിലറിസ് എന്ന് വിളിക്കുന്നു. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന് പോഷകങ്ങൾ നൽകുന്ന ഒരു കാപ്പിലറി നെറ്റ്വർക്കാണ് ഇത്.
ജിയോഗ്രഫിക്ക് അട്രോഫിയുടെ പാത്തോഫിസിയോളജി ഇപ്പോഴും അനിശ്ചിതത്വത്തിലാണ്. റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയം കുറവായതിനാലാണോ ഓക്സിഡേറ്റീവ് സ്ട്രെസ് വർദ്ധിക്കുന്നതെന്ന് ചില പഠനങ്ങൾ ചോദ്യം ചെയ്യുന്നു.[45] മറ്റ് പഠനങ്ങൾ നാശനഷ്ടങ്ങളുടെ ഇൻഫ്ലമേറ്ററി കാരണങ്ങൾ ആണ് അന്വേഷിച്ചത്. [46] ഇതുവരെ, മെഡിക്കൽ സമൂഹം ഈ വിഷയത്തിൽ കൃത്യമായ തീർപ്പിലെത്തിയിട്ടില്ല. സമീപകാല പഠനങ്ങൾ ഓരോ ലെയറുകളെയും വ്യക്തിഗതമായി കാണാൻ തുടങ്ങി. കൊറിയോകാപിലറികളിലെ രക്തയോട്ടം കുറയുന്നത് റെറ്റിന പിഗ്മെന്റ് എപിത്തീലിയത്തിന്റെയും ഫോട്ടോറിസെപ്റ്ററുകളുടെയും അട്രോഫിക്ക് മുന്നേസംഭവിക്കുന്നുവെന്ന് കണ്ടെത്തിയിട്ടുണ്ട്.[47] കൊറിയോകാപിലറി ഒരു വാസ്കുലർ ലെയറായതിനാൽ, രക്തയോട്ടം കുറയുന്നതുമൂലം ജിയോഗ്രഫിക്ക് അട്രോഫി വരാനുള്ള കാരണമായി ഇത് കണക്കാക്കാം.
നൂതന എഎംഡിയുടെ "വെറ്റ്" രൂപമായ നിയോവാസ്കുലർ അല്ലെങ്കിൽ എക്സുഡേറ്റീവ് എഎംഡിയിൽ, ബ്രച്സ് മെംബ്രേൻ വഴി കോറിയോകാപില്ലാരിസിലെ അസാധാരണമായ രക്തക്കുഴലുകളുടെ വളർച്ച (കോറോയ്ഡൽ നിയോവാസ്കുലറൈസേഷൻ) മൂലം കാഴ്ച നഷ്ടപ്പെടാൻ കാരണമാകുന്നു. ഇത് സാധാരണയായി എഎംഡിയുടെ ഡ്രൈ രൂപത്തിന് മുമ്പാണ് കാണുന്നത്, പക്ഷേ എല്ലായ്പ്പോഴും അങ്ങനെ ആവണമെന്നില്ല. റെറ്റിനയിലെ അസാധാരണമായ രക്തക്കുഴലുകളുടെ വ്യാപനം വാസ്കുലർ എൻഡോതെലിയൽ ഗ്രോത്ത് ഫാക്ടർ (വിഇജിഎഫ്) ഉത്തേജിപ്പിക്കുന്നു. ഈ രക്തക്കുഴലുകൾ അസാധാരണമായതിനാൽ ഇവ സാധാരണ രക്തക്കുഴലുകളേക്കാൾ ദുർബലമാണ്, ഇത് മാക്യുലയ്ക്ക് താഴെയുള്ള രക്തത്തിലേക്കും പ്രോട്ടീൻ ചോർച്ചയിലേക്കും നയിക്കുന്നു. ഈ രക്തക്കുഴലുകളിൽ നിന്നുള്ള രക്തസ്രാവം, ചോർച്ച, പാടുകൾ എന്നിവ ഒടുവിൽ ഫോട്ടോറിസെപ്റ്ററുകൾക്ക് മാറ്റാനാവാത്ത തകരാറുണ്ടാക്കുകയും ചികിത്സിച്ചില്ലെങ്കിൽ കാഴ്ചശക്തി കുറയുകയും ചെയ്യും.
റെറ്റിനൽ പിഗ്മെന്റ് എപിത്തീലിയത്തിലെ (ആർപിഇ) ലൈസോസോമുകൾക്കുള്ളിലെ കുറഞ്ഞ തന്മാത്രാ-ഭാരം, ഫോട്ടോടോക്സിക്, പ്രോ-ഓക്സിഡൻറ് മെലാനിൻ ഒലിഗോമറുകൾ എന്നിവയുടെ പ്രായവുമായി ബന്ധപ്പെട്ട ശേഖരണം ആർപിഇ - ഓട്ടോഫാഗി വഴി ഫോട്ടോറെസെപ്റ്റർ ഔറ്റർ റോഡ് സെഗ്മെന്റുകളുടെ (പിഒഎസ്) ദഹനനിരക്ക് കുറയ്ക്കുന്നതിന് കാരണമാകാം. പിഒഎസിന്റെ ദഹനനിരക്കിന്റെ കുറവ് ലിപോഫുസ്സിൻ രൂപീകരണവുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു - ഇത് എഎംഡിയുമായി ബന്ധപ്പെട്ട ഒരു ക്ലാസിക് അടയാളമാണ്.[48]
പുകവലിക്കാരിലും അൾട്രാവയലറ്റ് വികിരണത്തിന് വിധേയരായവരിലും രോഗത്തിന്റെ വർദ്ധിച്ച നിരക്ക്, എഎംഡിയുടെ കാരണത്തിൽ റെറ്റിനൽ ഓക്സിഡേറ്റീവ് സ്ട്രെസിന്റെ പങ്ക് സൂചിപ്പിക്കുന്നു.[13] [49] [50]
മൈറ്റോകോൺഡ്രിയൽ ഡിസ്ഫങ്ഷനും ഇതിൽ ഒരു പങ്കുണ്ടാകാം.[51]

പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ രോഗ നിർണ്ണയം കാഴ്ച പരിശോധനയേക്കാളുപരി മാക്യുലയിലെ ലക്ഷണങ്ങളുടെ പരിശോധനയാണ്. വെറ്റ് എഎംഡി സാധാരണയായി ഡ്രൈ എഎംഡിയുടെ വിപുലമായ പുരോഗതിയാണ്, അതിൻറെ പരിശോധനയ്ക്ക് അധിക ഡയഗ്നോസ്റ്റിക് ഉപകരണങ്ങൾ ആവശ്യമാണ്. വെറ്റ് എഎംഡിയുടെ ആദ്യകാല രോഗനിർണയം കാഴ്ചശക്തി വീണ്ടും കുറയാതിരിക്കാനും കാഴ്ച മെച്ചപ്പെടുത്തുന്നതിനും സഹായിക്കുന്നു.[52]
ഡ്രൈ (അല്ലെങ്കിൽ പ്രാരംഭ ഘട്ടത്തിൽ) എഎംഡി രോഗനിർണയത്തിൽ ഇനിപ്പറയുന്ന ക്ലിനിക്കൽ പരിശോധനകളും നടപടിക്രമങ്ങളും പരിശോധനകളും ഉൾപ്പെടാം:
വെറ്റ് (അല്ലെങ്കിൽ അവസാന ഘട്ടത്തിൽ) എഎംഡിയുടെ രോഗനിർണയത്തിൽ മുകളിൽ പറഞ്ഞ പരിശോധനകൾക്ക് പുറമേ ഇനിപ്പറയുന്നവ കൂടി ഉൾപ്പെടാം:
2017 ലെ കോക്രൺ അവലോകനത്തിൽ വിറ്റാമിൻ, മിനറൽ സപ്ലിമെന്റുകൾ ഒറ്റയ്ക്കോ കൂട്ടായോ ഉപയോഗിക്കുന്നത് സാധാരണ ജനങ്ങൾക്ക് എഎംഡി ഉണ്ടോ ഇല്ലയോ എന്നതിനെ ബാധിക്കുന്നില്ലെന്ന് കണ്ടെത്തി.[4]
രോഗത്തിന്റെ തരത്തെ ആശ്രയിച്ച് എഎംഡിയുടെ ചികിത്സ വ്യത്യാസപ്പെടുന്നു. പൊതുവേ, എഎംഡിയുടെ പുരോഗതി മന്ദഗതിയിലാക്കുകയാണ് ചികിത്സയുടെ പ്രധാന ലക്ഷ്യം.[55] 2018 ലെ കണക്കനുസരിച്ച്, എഎംഡിയുടെ ഫലങ്ങൾ മാറ്റുന്നതിനുള്ള ചികിത്സകളൊന്നുമില്ല. അറിയപ്പെടുന്ന അപകടസാധ്യത ഘടകങ്ങളായ പുകവലി, രക്തപ്രവാഹത്തിന് മാറ്റം വരുത്തുക, ഭക്ഷണത്തിൽ മാറ്റങ്ങൾ വരുത്തുക എന്നിവയിലൂടെയാണ് ആദ്യഘട്ടവും ഇന്റർമീഡിയറ്റ്-സ്റ്റേജ് എഎംഡിയും നിയന്ത്രിക്കുന്നത്. ഇന്റർമീഡിയറ്റ്-സ്റ്റേജ് എഎംഡി മാനേജ്മെൻറിൽ ആന്റിഓക്സിഡന്റും മിനറൽ സപ്ലിമെന്റേഷനും ഉൾപ്പെടുന്നു.[56] കോറോയിഡൽ നിയോവാസ്കുലറൈസേഷന്റെ (സിഎൻവി) സാന്നിധ്യം അടിസ്ഥാനമാക്കിയാണ് അഡ്വാൻസ്ഡ്-സ്റ്റേജ് എഎംഡി കൈകാര്യം ചെയ്യുന്നത്: ഡ്രൈ എഎംഡി (സിഎൻവി നിലവിലില്ല) അല്ലെങ്കിൽ വെറ്റ് എഎംഡി (സിഎൻവി നിലവിലുണ്ട്). ഡ്രൈ എഎംഡിക്ക് ഫലപ്രദമായ ചികിത്സകളൊന്നും നിലവിലില്ല. വെറ്റ് എഎംഡിയിലുള്ള സിഎൻവി നിയന്ത്രിക്കുന്നത് വാസ്കുലർ എൻഡോ തീലിയൽ ഗ്രോത്ത് ഫാക്ടർ (വിഇജിഎഫ്) ഇൻഹിബിറ്ററുകളാണ്.[57] [58]
ഈ അവസ്ഥയ്ക്ക് മെഡിക്കൽ അല്ലെങ്കിൽ ശസ്ത്രക്രിയാ ചികിത്സ ലഭ്യമല്ല.
വെറ്റ് എഎംഡിയിലെ സിഎൻവി ചികിത്സയ്ക്കായി റാനിബിസുമാബ്, അഫ്ലിബെർസെപ്റ്റ്, ബ്രോലുസിസുമാബ് എന്നീ വിഇജിഎഫ് ഇൻഹിബിറ്ററുകൾ അംഗീകരിച്ചിട്ടുണ്ട്.[57] [59] മൂന്ന് മരുന്നുകളും ഇൻട്രാവിട്രിയൽ കുത്തിവയ്പ്പിലൂടെയാണ് നൽകുന്നത്, അതായത് അവ നേരിട്ട് കണ്ണിലേക്ക് കുത്തിവയ്ക്കുന്നു. മുമ്പത്തെ രണ്ട് മരുന്നുകളുടേതിന് സമാനമായ ഫലപ്രാപ്തിയും സുരക്ഷയും ഉണ്ടെന്ന് തെളിയിക്കപ്പെട്ടിട്ടുള്ള മറ്റൊരു വിഇജിഎഫ് ഇൻഹിബിറ്ററാണ് ബെവാസിസുമാബ്, എന്നിരുന്നാലും ഇത് നിലവിൽ എഎംഡിക്ക് സൂചിപ്പിച്ചിട്ടില്ല. [58] ലേസർ കോയാഗ്യുലേഷൻ തെറാപ്പി ഉപയോഗിച്ചും എഎംഡി ചികിത്സിക്കാം.[60]
ക്രമരഹിതമായ ഒരു നിയന്ത്രിത ട്രയലിൽ ബെവാസിസുമാബിനും റാണിബിസുമാബിനും സമാനമായ ഫലപ്രാപ്തി ഉണ്ടെന്ന് കണ്ടെത്തി.[61] ഗ്യാസ്ട്രോഇന്റസ്റ്റൈനൽ ഡിസോർഡേഴ്സ് ഒഴികെ നിയോവാസ്കുലർ എഎംഡി ചികിത്സിക്കാൻ ഉപയോഗിക്കുമ്പോൾ ബെവാസിസുമാബിന്റെയും റാണിബിസുമാബിന്റെയും വ്യവസ്ഥാപരമായ സുരക്ഷ സമാനമാണെന്ന് 2014 ലെ ഒരു കോക്രൺ അവലോകനത്തിൽ കണ്ടെത്തി.[62] എന്നിരുന്നാലും മാക്യുലർ ഡീജനറേഷൻ ചികിത്സയ്ക്കായി ബെവാസിസുമാബ് എഫ്ഡിഎ അംഗീകരിച്ചിട്ടില്ല. അംഗീകൃതവും എന്നാൽ ചെലവേറിയതുമായ റാണിബിസുമാബിനെക്കാൾ വിലകുറഞ്ഞ ബെവാസിസുമാബിന്റെ ഓഫ്-ലേബൽ ഉപയോഗം യുകെയിലെ ഒരു വിവാദത്തിൽ ഉൾപ്പെടുന്നു. കണ്ണ് കുത്തിവയ്പ്പുകൾക്കായി പ്രത്യേകം രൂപകൽപ്പന ചെയ്ത പാരന്റ് ബെവാസിസുമാബ് തന്മാത്രയുടെ ഫാബ് ശകലമാണ് റാണിബിസുമാബ്. നിയോ വാസ്കുലർ എഎംഡിയുടെ ചികിത്സയ്ക്കായി അംഗീകരിച്ച മറ്റ് ആൻറി ആൻജിയോജനിക് മരുന്നുകളിൽ പെഗപ്റ്റാനിബ്[63], അഫ്ലിബെർസെപ്റ്റ് എന്നിവ ഉൾപ്പെടുന്നു.
അമേരിക്കൻ അക്കാദമി ഓഫ് ഒഫ്താൽമോളജി പ്രാക്ടീസ് മാർഗ്ഗനിർദ്ദേശങ്ങൾ മാക്യുലർ ഡീജനറേഷനായി ലേസർ കോയാഗ്യുലേഷൻ തെറാപ്പി ശുപാർശ ചെയ്യുന്നില്ല, പക്ഷേ മരുന്ന് ചികിത്സയോട് പ്രതികരിക്കാത്ത, ഫോവിയയ്ക്ക് പുറത്തുള്ള കോറോയിഡിൽ പുതിയ രക്തക്കുഴലുകളുള്ള ആളുകൾക്ക് ഇത് ഉപയോഗപ്രദമാകുമെന്ന് പ്രസ്താവിക്കുന്നു.[64] [65] ലേസർ കൊയാഗുലേഷൻ ഡ്രൂസൻ മാഞ്ഞുപോകുന്നതിന് കാരണമാകുമെന്നതിന് ശക്തമായ തെളിവുകളുണ്ട്, പക്ഷേ ഇത് കോറോയ്ഡൽ നിയോവാസ്കുലറൈസേഷനെ ബാധിക്കില്ല.[66] 2007 ലെ കോക്രൺ അവലോകനത്തിൽ, ഫൊവിയയ്ക്ക് പുറത്തുള്ള കോറോയിഡിലെ പുതിയ രക്തക്കുഴലുകളുടെ ലേസർ ഫോട്ടോകോയാഗുലേഷൻ ഫലപ്രദവും സാമ്പത്തികവുമായ രീതിയാണെന്ന് കണ്ടെത്തി, പക്ഷേ ഇത് ഫോവിയയ്ക്ക് അടുത്തോ താഴെയോ ഉള്ള രക്തകുഴലുകൾക്ക് മാത്രമായി പരിമിതപ്പെടുത്തിയിരിക്കുന്നു.[67]
വെറ്റ് എഎംഡിയെ ചികിത്സിക്കാൻ ഫോട്ടോഡൈനാമിക് തെറാപ്പിയും ഉപയോഗിച്ചുവരുന്നുണ്ട്.[68] മരുന്ന് വെർട്ടെപോർഫിൻ ഞരമ്പിലൂടെയാണ് നൽകുന്നത്; അതിനുശേഷം ഒരു പ്രത്യേക തരംഗദൈർഘ്യത്തിന്റെ പ്രകാശം അസാധാരണ രക്തക്കുഴലുകളിൽ പ്രയോഗിക്കുന്നു. ഇത് വെർട്ടെപോർഫിൻ സജീവമാക്കി രക്തകുഴലുകളെ നശിപ്പിക്കുന്നു.
തിമിര ശസ്ത്രക്രിയ എഎംഡിയുള്ള ആളുകൾക്ക് വിഷ്വൽ ഫലങ്ങൾ മെച്ചപ്പെടുത്താൻ കഴിയും, എഎംഡിയുടെ പുരോഗതി വർദ്ധിപ്പിക്കുന്ന ശസ്ത്രക്രിയയെക്കുറിച്ച് ആശങ്കകളുണ്ടെങ്കിലും. ക്രമരഹിതമായ നിയന്ത്രിത ട്രയലിൽ, തിമിര ശസ്ത്രക്രിയയ്ക്ക് വിധേയരായ ആളുകൾക്ക് (രണ്ടാഴ്ചയ്ക്കുള്ളിൽ) വൈകിയ തിമിര ശസ്ത്രക്രിയയ്ക്ക് വിധേയരായവരേക്കാൾ (6 മാസം) കാഴ്ചശക്തിയും ജീവിത ഫലങ്ങളുടെ ഗുണനിലവാരവും മെച്ചപ്പെട്ടതായി കണ്ടെത്തിയിട്ടുണ്ട്.[69]

പെരിഫറൽ കാഴ്ചയെ ബാധിക്കാത്തതിനാൽ, മാക്യുലർ ഡീജനറേഷൻ ഉള്ള ആളുകൾക്ക് അവരുടെ കാഴ്ച ഭാഗികമായി ശരിയാക്കാൻ, പെരിഫറൽ കാഴ്ച ഉപയോഗിക്കാൻ ശീലിക്കുന്നതിലൂടെ കഴിയും.[70]
മാഗ്നിഫൈയിംഗ് ഗ്ലാസുകൾ, പ്രത്യേക കണ്ണട ലെൻസുകൾ, കമ്പ്യൂട്ടർ സ്ക്രീൻ റീഡറുകൾ, മെറ്റീരിയൽ വായന വിപുലീകരിക്കുന്ന ടിവി പോലെയുള്ള അഡാപ്റ്റീവ് ഉപകരണങ്ങൾ ആളുകളെ വായിക്കാൻ സഹായിക്കുന്നു. സംവിധാനങ്ങൾ എന്നിവ ഇതിൽ ഉൾപ്പെടുന്നു.
കമ്പ്യൂട്ടർ സ്ക്രീൻ റീഡറുകളായ JAWS അല്ലെങ്കിൽ തണ്ടർ സാധാരണ വിൻഡോസ് കമ്പ്യൂട്ടറുകളിൽ പ്രവർത്തിക്കുന്നു. കൂടാതെ, ആപ്പിൾ ഉപകരണങ്ങൾ വോയ്സ് ഓവർ, സ്ക്രീൻ റീഡറുകൾ, ബ്രെയ്ലി മുതലായ വൈവിധ്യമാർന്ന സവിശേഷതകൾ നൽകുന്നു.
വീഡിയോ ക്യാമറകൾ സ്റ്റാൻഡേർഡ് അല്ലെങ്കിൽ പ്രത്യേക-ഉദ്ദേശ്യ കമ്പ്യൂട്ടർ മോണിറ്ററുകളിലേക്ക് ചേർത്ത് ചിത്രം വലുതാക്കി നോക്കാൻ കഴിയും. ലിഖിത മെറ്റീരിയൽ നീക്കാൻ ചലിക്കുന്ന ടേബിളും ഈ സിസ്റ്റങ്ങളിൽ പലപ്പോഴും ഉൾപ്പെടുന്നു.
വലിയ ഫോണ്ടുകൾ ഉള്ള പുസ്തകങ്ങൾ, ട്രാക്കിംഗ് എളുപ്പമാക്കുന്നതിനുള്ള പാറ്റേണുകൾ, വാചകവും ഓഡിയോയും ഉള്ള ഓഡിയോബുക്കുകൾ, ഡെയ്സി പുസ്തകങ്ങൾ എന്നിവയും കാഴ്ച കുറവ് ഉള്ളവർക്ക് വേണ്ടിയുണ്ട്.

ഏഷ്യക്കാരെയും ആഫ്രിക്കക്കാരെയും അപേക്ഷിച്ച് പ്രായവുമായി ബന്ധപ്പെട്ട ഏത് മാക്യുലർ ഡീജനറേഷനും യൂറോപ്പുകാരിൽ കൂടുതലാണ്.[72] ഏഷ്യക്കാരും ആഫ്രിക്കക്കാരും തമ്മിൽ കണക്കിൽ കാര്യമായ വ്യത്യാസമില്ല. പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷനും അതുമായി ബന്ധപ്പെട്ട സവിശേഷതകളും പ്രായത്തിനനുസരിച്ച് വർദ്ധിക്കുന്നതിനാൽ 55 വയസ്സിന് താഴെ പ്രായമുള്ള ആളുകളിൽ ഇത് കുറവാണ്.[73] രോഗ വർദ്ധനയുമായി ബന്ധപ്പെട്ട് പരിഷ്ക്കരിക്കാവുന്ന ഏറ്റവും ശക്തമായ ഘടകമാണ് പുകവലി.[74] യുഎസ്എയിലെ വെളുത്ത ജനസംഖ്യയിൽ കാഴ്ചശക്തി നഷ്ടപ്പെടുന്നതിന്റെ കാരണങ്ങളിൽ 54% ത്തിലധികവും പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ മൂലം ആണ്. ഏകദേശം 8 ദശലക്ഷം അമേരിക്കക്കാരെ പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ ബാധിക്കുന്നു, അവരിൽ 1 ദശലക്ഷത്തിലധികം പേർക്ക് അടുത്ത 5 വർഷത്തിനുള്ളിൽ പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ തീവ്ര അവസ്ഥയിലാകും. യുകെയിൽ, 65–74 വയസ് പ്രായമുള്ളവരിൽ ഏകദേശം 42% നും, 75–84 വയസ് പ്രായമുള്ളവരിൽ മൂന്നിൽ രണ്ട് ഭാഗത്തിനും, 85 വയസ്സ് മുതൽ മുകളിലോട്ട് പ്രായമുള്ളവരിൽ മുക്കാൽ ഭാഗത്തിനും അന്ധതയ്ക്ക് കാരണമാകുന്നത് പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷനാണ്.
എഎംഡിയുമായി ബന്ധപ്പെട്ട ഡ്രൂസൻ, തന്മാത്രാ ഘടനയിൽ പ്രായവുമായി ബന്ധപ്പെട്ട മറ്റ് രോഗങ്ങളായ അൽഷിമേഴ്സ് രോഗം, ആർത്തെറോസ്ലീറോസിസ് പോലെയുള്ള രോഗാവസ്ഥകളിലെ ബീറ്റാ-അമിലോയിഡ് (βA) പ്ലേക്കുകൾക്കും ഡെപ്പോസിറ്റുകൾക്കും സമാനമാണെന്നും പഠനങ്ങൾ സൂചിപ്പിക്കുന്നു. എഎംഡിയുടെയും പ്രായവുമായി ബന്ധപ്പെട്ട മറ്റ് രോഗങ്ങളുടെയും കാരണങ്ങളിൽ സമാനമായ മാർഗങ്ങൾ ഉൾപ്പെട്ടിരിക്കാമെന്ന് ഇത് സൂചിപ്പിക്കുന്നു.[75]
എഎംഡിയുമായി ബന്ധപ്പെട്ട ജനിതക മാർക്കറുകളുടെ ഒരു പ്രായോഗിക പ്രയോഗം എഎംഡിയുടെ രോഗത്തിൻറെ പ്രാരംഭ ഘട്ടത്തിൽ നിന്ന് നിയോവാസ്കുലറൈസേഷനിലേക്കുള്ള പുരോഗതി പ്രവചനത്ത്ന് സഹായകരമാവും.[41] [42]
അസ്ഥി മജ്ജ സ്റ്റെം സെല്ലുകൾ ഉപയോഗിച്ചുള്ള സെൽ അധിഷ്ഠിത ചികിത്സകളും, റെറ്റിന പിഗ്മെന്റ് എപ്പിത്തീലിയൽ ട്രാൻസ്പ്ലാൻറേഷനും പഠനവിധേയമാക്കിയിട്ടുണ്ട്.[76] ഇതുമായി ബന്ധപ്പെട്ട് പ്രോത്സാഹജനകമായ ഫലങ്ങളുമായി മനുഷ്യരിൽ നിരവധി പരീക്ഷണങ്ങൾ നടന്നിട്ടുണ്ട്. [77]
സമാനമായ ലക്ഷണങ്ങളുള്ള മറ്റ് ചില (അപൂർവ) തരം മാക്യുലർ ഡീജനറേഷൻ ഉണ്ട്, പക്ഷേ വെറ്റ് അല്ലെങ്കിൽ ഡ്രൈ മാക്കുലാർ ഡീജനറേഷനുമായി എറ്റിയോളജിക്കലി ഇവയ്ക്ക് ബന്ധമില്ല. കുട്ടിക്കാലത്തോ മധ്യവയസ്സിലോ ഉണ്ടാകാവുന്ന ജനിതക വൈകല്യങ്ങളാണ് അവയെല്ലാം.
വളരെ വ്യത്യസ്തമായ എറ്റിയോളജിയും വ്യത്യസ്ത ചികിത്സയും ഉള്ള, എപിറെറ്റിനൽ മെംബ്രൺ (മാക്യുലാർ പക്കർ), സെൻട്രൽ സീറസ് റെറ്റിനോപ്പതി പോലുള്ള മാക്കുലയെ ബാധിക്കുന്ന മറ്റ് അവസ്ഥകളിലും സമാന ലക്ഷണങ്ങൾ ഉണ്ടാകാം.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.