
Цезиум хлорид
хемиско соединение / From Wikipedia, the free encyclopedia
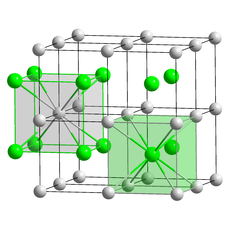
Цезиум хлорид — неорганско соединение со формула CsCl. Оваа безбојна сол е важен извор на јони на цезиум во различни примени. Неговата кристална структура формира голем структурен тип каде секој цезиумски јон е координиран со 8 хлоридни јони. Цезиум хлоридот се раствора во вода. CsCl се менува во својата структура и добива структура на NaCl при загревање. Цезиум хлоридот природно се јавува како нечистотии во карналит (до 0,002%), силвит и каинит. Помалку од 20 тони CsCl се произведуваат годишно ширум светот, главно од минерален загадувач што содржи цезиум.[7]
 | |
 | |
 | |
Назив според МСЧПХ Цезиум хлорид | |
Други називи Цезиум хлорид | |
| Назнаки | |
|---|---|
| 7647-17-8 | |
| ChemSpider | 22713 |
| EC-број | 231-600-2 |
| 3Д-модел (Jmol) | Слика |
| PubChem | 24293 |
| |
| UNII | GNR9HML8BA |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | бела цврста супстанца хигроскопна |
| Густина | 3.988 g/cm3[1] |
| Точка на топење | |
| Точка на вриење | |
| 1910 g/L (25 °C)[1] | |
| Растворливост | растворлив во етанол[1] |
| Забранет појас | 8.35 eV (80 K)[2] |
Магнетна чувствителност (χ) |
-56.7·10−6 cm3/mol[3] |
| Показател на прекршување (nD) | 1.712 (0.3 μm) 1.640 (0.59 μm) 1.631 (0.75 μm) 1.626 (1 μm) 1.616 (5 μm) 1.563 (20 μm)[4] |
| Структура | |
| Кристална структура | CsCl, cP2 |
Просторна група |
Pm3m, No. 221[5] |
Константа на решетката |
|
Координациска геометрија |
Кубична (Cs+) Кубична (Cl−) |
| Опасност | |
| GHS-ознаки: | |
Пиктограми |
  |
Сигнални зборови |
Предупредување |
Изјави за опасност |
H302, H341, H361, H373 |
Изјави за претпазливост |
P201, P202, P260, P264, P270, P281, P301+P312, P308+P313, P314, P330, P405, P501 |
| Смртоносна доза или концентрација: | |
LD50 (средна доза) |
2600 mg/kg (орално, стаорец)[6] |
| Слични супстанци | |
| Други анјони | Цезиум флуорид Цезиум бромид Цезиум јодид Цезиум астатид |
| Други катјони | Литиум хлорид Натриум хлорид Калиум хлорид Рубидиум хлорид Франциум хлорид |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Цезиум хлоридот е широко употребувана медицинска структура во изопикничнoто центрифугирање за одвојување на различни типови на ДНК. Тој е реагенс во аналитичката хемија, каде што се користи за идентификување на јоните според бојата и морфологијата на талогот. Кога е збогатен со радиоизотопи, како што се 137CsCl или 131CsCl, цезиум хлоридот се користи во методи на јадрената медицина, како што се третман на рак и дијагноза на миокарден инфаркт. Друга форма на третман на рак беше проучувана со користење на конвенционален нерадиоактивен CsCl. Додека конвенционалниот цезиум хлорид има прилично ниска токсичност за луѓето и животните, радиоактивната форма лесно ја контаминира животната средина поради високата растворливост на CsCl во вода. Распространетоста на прав од 137CsCl од контејнер од 93 грама во 1987 година во Гојанија, Бразил, резултираше со една од најлошите несреќи со излевање на радијација во која загинаа четворица, а директно беа погодени 249 луѓе.