хемиско соединение From Wikipedia, the free encyclopedia
Калиум цијанид — соединение со формулата KCN. Оваа безбојна кристална сол, по изглед слична на шеќерот, е многу растворлива во вода. Повеќето KCN се користи во ископувањето на злато, во органски синтези и за галванизација. Помалите употреби вклучуваат при хемиско обложување и печење на накит.[4]
 | |
 | |
Назив според МСЧПХ Калиум цијанид | |
| Назнаки | |
|---|---|
| 151-50-8 | |
| ChEBI | CHEBI:33191 |
| ChemSpider | 8681 |
| EC-број | 205-792-3 |
| 3Д-модел (Jmol) | Слика |
| PubChem | 9032 |
| RTECS-бр. | TS8750000 |
| |
| UNII | MQD255M2ZO |
| ОН-бр. | 1680 |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | Бела кристална цврста супстанца deliquescent |
| Мирис | слаб, арома на бадем |
| Густина | 1,52 g/cm3
Solubility = 71.6 g/100 ml (25 °C) |
| Точка на топење | |
| Точка на вриење | |
| Растворливост во метанол | 4,91 g/100 mL (20 °C) |
| Растворливост во глицерол | soluble |
| Растворливост во формамид | 14,6 g/100 mL |
| Растворливост во етанол | 0,57 g/100mL |
| Растворливост во хироксиламин | 41 g/100 mL |
| Киселост (pKa) | 11,0 |
Магнетна чувствителност (χ) |
−37,0·10−6 cm3/mol |
| Показател на прекршување (nD) | 1,410 |
| Термохемија | |
| Ст. енталпија на образување ΔfH |
−131,5 kJ/mol |
| Стандардна моларна ентропија S |
127,8 J K−1 mol−1 |
| Опасност | |
| GHS-ознаки: | |
Пиктограми |
    |
Сигнални зборови |
Опасност |
Изјави за опасност |
H290, H300, H310, H330, H370, H372, H410 |
Изјави за претпазливост |
P260, P264, P273, P280, P284, P301+P310 |
| NFPA 704 | |
| Температура на запалување | не-запаливо |
| Смртоносна доза или концентрација: | |
LD50 (средна доза) |
5 mg/kg (орално, зајак) 10 mg/kg (орално, стаорец) 5 mg/kg (орално, стаоред) 8.5 mg/kg (орално, глушец)[1] |
| NIOSH (здравствени граници во САД): | |
PEL (дозволива) |
TWA 5 mg/m3[2] |
REL (препорачана) |
C 5 mg/m3 (4.7 ppm) [10-минути][2] |
IDLH (непосредна опасност) |
25 mg/m3[2] |
| Безбедносен лист | ICSC 0671 |
| Слични супстанци | |
| Други анјони | Калиум цијанит Калиум тиоцијанат |
| Други катјони | Натриум цијанид Рубидиум цијанид Литиум цијанид Цeзиум цијанид |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Калиум цијанидот е многу токсичен. Влажната цврста сол од KCN испушта мали количини на цијановодород поради хидролиза, што може да мириса на горчлив бадем.[5] Сепак, не секој може да намириса цијанид; способноста да се направи тоа е генетска одлика.
Вкусот на калиум цијанид е опишан како остар и горчлив, со чувство на печење[6] слично на лугата.[7]
KCN се произведува со третирање на цијановодород со воден раствор на калиум хидроксид, проследено со испарување на растворот во вакуум:[8]
Годишно се произведуваат околу 50.000 тони калиум цијанид.[4]
Пред 1900 година и пронаоѓањето на Кастнеровиот процес, калиум цијанидот бил најважниот извор на цијаниди од алкални метали.[4] Во овој историски процес, калиум цијанидот бил произведен со распаѓање на калиум фероцијанид:[9]
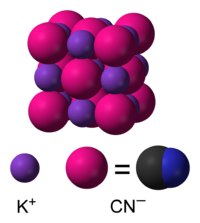
Во воден раствор, KCN дисоцира на хидрирани јони на калиум(K+) и цијанидни јони (CN−). Вообичаената форма на цврст KCN, стабилна на амбиентален притисок и температура, ја има истата кубна кристална структура како и натриум хлоридот, при што секој јон на калиум е опкружен со шест јони на цијанид, и обратно. И покрај тоа што јоните на цијанид се двоатомски, а со тоа и помалку симетрични од хлоридот, тие ротираат толку брзо што нивната форма во просек за време е сферична. При ниска температура и висок притисок, оваа слободна ротација е попречена, што резултира со помалку симетрична кристална структура со цијанидни јони распоредени во листови [10][11]
KCN и натриум цијанид (NaCN) широко користени во органската синтеза за подготовка на нитрили и карбоксилни киселини, особено во реакцијата на von Richter. Исто така, наоѓа употреба за синтеза на хидантоини, кои можат да бидат корисни синтетички посредници, кога реагираат со карбонилно соединение како што е алдехид или кетон во присуство на амониум карбонат.
KCN се користи како фотографски фиксатор во процесот на колодиум на влажна плоча.[12] KCN го раствора среброто онаму каде што не станало нерастворливо од развивачот. Ова ја открива и стабилизира сликата, што ја прави повеќе нечувствителна на светлина. Модерните фотографи со влажна плоча можеби претпочитаат помалку токсични фиксатори, често избирајќи натриум тиосулфат, но KCN сè уште се користи
Во ископувањето злато, KCN формира сол растворлива во вода калиум злато цијанид (или злато калиум цијанид) и калиум хидроксид од метално злато во присуство на кислород (обично од околниот воздух) и вода:
Сличен процес користи NaCN за производство на натриум злато цијанид (NaAu(CN2)).
Калиум цијанидот е моќен инхибитор на клеточното дишење, делувајќи на митохондријалната цитохром c оксидаза, па оттука ја блокира оксидативната фосфорилација. Потоа се јавува млечна ацидоза како последица на анаеробен метаболизам. Првично, акутното труење со цијанид предизвикува црвен или румен тен кај жртвата бидејќи ткивата не се во можност да го користат кислородот во крвта. Ефектите на калиум цијанид и натриум цијанид се идентични, а симптомите на труење обично се јавуваат во рок од неколку минути по внесувањето на супстанцијата: лицето ја губи свеста и на крајот следи мозочна смрт. Во овој период жртвата може да претрпи конвулзии. Смртта е предизвикана од церебрална хипоксија. Очекуваната доза на LD100 (човечка) за калиум цијанид е 200–300 mg додека средната смртоносна доза LD50 се проценува на 140 mg.[13]
Луѓето кои умреле со самоубиство или биле убиени користејќи калиум цијанид се:
Високи личности во нацистичка Германија, како Ервин Ромел, долгогодишната придружничка на Хитлер, Ева Браун, Џозеф Гебелс, Хајнрих Химлер и Херман Геринг
Професионалните ентомолози го користат како средство за убивање при собирање во тегли, бидејќи инсектите за неколку секунди подлегнуваат на испарувањата од HCN што ги испушта, со што се минимизира штетата дури и на многу кревките примероци.
KCN може најефикасно да се детоксицира со водород пероксид или со раствор од натриум хипохлорит. Таквите раствори треба да се чуваат алкални секогаш кога е можно за да се елиминира можноста за создавање на цијановодород:[4]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.