From Wikipedia, the free encyclopedia
Staphylococcus aureus (познат како златен стафилокок) ― Грампозитивна, топчеста бактерија која е дел од нормалната микрофлора на телото, често се наоѓа во носот, респираторниот систем и на кожата. Позитивна е на каталаза и редукција на нитрат и е факултативен анаероб.[1] Иако S. aureus не е секогаш патогена (и најчесто може да се најде како коменсал), таа е честа причина за инфекции на кожата, вклучувајќи апсцеси, респираторни инфекции, како што се синузити, труење со храна и друго. Патогените соеви предизвикуваат инфекции преку создавање на фактори на вирулентност, како што се јаки белковински токсини, и со присуство на површински белковини кои врзуваат и онеспособуваат антитела. Појавата на антибиотски-резистентни соеви од S. aureus како метицилин резистентниот S. aureus (MRSA) е светски проблем во клиничката медицина. И покрај бројните истражувања, сè уште не е одобрена вакцина за S. aureus.
| Staphylococcus aureus | |
|---|---|
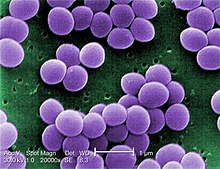 | |
| Скенирачки електронски микрограф на S. aureus со фалс боја | |
| Научна класификација | |
| Домен: | Bacteria |
| Колено: | Firmicutes |
| Класа: | Bacilli |
| Ред: | Bacillales |
| Семејство: | Staphylococcaceae |
| Род: | Staphylococcus |
| Вид: | S. aureus |
| Научен назив | |
| Staphylococcus aureus Rosenbach 1884 | |
Staphylococcus видот за првпат бил идентификуван во 1880 во Единбург, Шкотска, од страна на хирургот Александар Огстон, во гној од хируршки апсцес во колено.[2] Ова име подоцна било променето во Staphylococcus aureus од страна на Фридрих Јулиј Розенбах.[3] Околу 20% до 30% од човечката популација се носители на S. aureus[4][5] кој се наоѓа како дел од нормалната микрофлора на кожата, во ноздрите,[6] и во долниот репродуктивен тракт на жената.[7][8] S. aureus може да предизвика голем број на болести, од мали инфекции на кожата, како што се акни,[9] импетиго, фурункули, карбункули, целулит, фоликулит, стафилококен ексфолијативен дерматит (Ритерова болест) и животно загрозувачки болести како пневмонија, менингит, остеомиелит, ендокардит, токсичен шок-синдром, бактериемија, и сепса. Сè уште е една од петте најчести причини на болнички инфекции и често е причина за рани постоперативни инфекции. Секоја година, околу 500.000 пациенти во болниците на САД заболуваат од стафилококни инфекции, главно од S. aureus,[10] а 50.000 смртни случаи годишно се резултат на инфекции од истата бактерија.[11]
| Staphylococcus aureus | |
|---|---|
| Специјалност | Infectious disease |


S. aureus (од грчкиот збор: σταφυλόκοκκος, „гроздовидни зрна“ и латинскиот aureus, „златен“[12][13]) е факултативно анаеробна, Грам-позитивна кока, позната како „златен стафилокок“. Тие се неподвижни и не формираат ендоспори.[14] На микроскоп се гледаат како големи, тркалезни топчиња аранжирани во неправилни, гроздовидни структури со златно-жолта боја. Култивирани на крвен агар прават хемолиза.[15] S. aureus се репродуцира бесполово со двоично цепење (проста делба). За комплетно одделување на клетките-ќерки потребен е автолизин и во негово отсуство или инхибиција, клетките-ќерки остануваат поврзани една со друга при што формираат кластери.[16]
S. aureus е каталаза-позитивен затоа што го произведува ензимот каталаза. Тој го разградува водород пероксидот (H2O2) на вода и кислород. Затоа каталаза-тестовите се користат да се направи разлика на стафилококи од ентерококи и стрептококи. Порано, S. aureus бил разликуван од другите стафилококи со помош на коагулаза тестот. Сепак, не сите S. aureus соеви се коагулаза-позитивни[17] и неточната идентификација влијае на ефикасен третман и спроведување на мерките за контрола.[18]
Природна генетска преобразба е размножувачка постапка на пренос на ДНК од една бактерија на друга и интеграција на дарителската секвенца во геномот на реципиентот со хомологна рекомбинација. Било пронајдено дека S. aureus е способен за природна генетска преобразба, но со мала честота под опитните услови кои биле применети.[19] Понатамошните истражувања покажале дека развојот на компетентност за природна генетска преобразба може да биде значително зголемен под соодветни услови, кои допрва треба да бидат откриени.[20]
Кај луѓето, S. aureus е дел од нормалната микрофлора присутна во горниот респираторен тракт,[21] на кожата и слузници и во дигестивниот систем.[22]
S. aureus, заедно со сличните видови кои се дел од микрофлората и се однесуваат симбиотски, предизвикаат болест ако почнат да ги инвадираат ткивата. Таквите бактериски заедници се нарекуваат „патобионти“.[21]

Додека S. aureus обично е коменсална бактерија која асимптоматски колонизира околу 30% од човечката популација, понекогаш може да предизвика болест.[23] Таа е една од најчестите причини за појава на бактериемија и инфективен ендокардит. Дополнително, може да предизвика разни инфекции на кожата и меките ткива, особено кога нивните одбранбени бариери се пробиени.
Инфекциите со S. aureus се шират преку директен допир со гној од заразена рана или индиректно со користење на предмети за лична употреба на заразени лица, како пешкири, чаршави, облека, или спортска опрема.
Посебно ранливи пациенти како дијабетичари, пациенти корисници на парентерална терапија и срцево болните, треба да се преземаат дополнителни мерки на претпазливост за да избегнат можност за инфицирање со S. aureus. Претпазливите мерки се често миење на рацете со сапун и често туширање или капење.
S. aureus е причинител на хронични инфекции со создавање на биофилмови на медицински импланти.[24]
Откако симптомите на инфекции со S. aureus ќе се појават, домаќинот е заразен околу две недели, а целокупната болест трае неколку недели. Нелечена, болеста може да биде смртоносна.[25]
Длабокопродирачките инфекции можат да бидат мошне сериозни.
Најчести инфекции со S. aureus се инфекциите на кожата. Можат да се манифестираат како: фоликулит, импетиго, целулит, фурункули, карбункули, апсцеси и други тешки инвазивни мекоткивни инфекции.[5][9]
Предиспонирани лица кон овие инфекции се тие кои веќе имаат некое нарушување на кожата, како на пр. атопичен дерматит. Присуството на S. aureus кај лица со атопичен дерматитис не е секогаш индикација за третман со орални антибиотици и најчесто лечењето започнува со зајакнување на кожната бариера. Кај новороденчиња, стафилококните инфекции можат да доведат до тешко заболување наречено стафилококен ексфолијативен дерматит (SSSS).[26]
S. aureus е исто така одговорен за труења со храна. Бактериите се способни за лачење на токсини кои предизвикуваат труење со храна.[27] Периодот на инкубација трае од еден до шест часа,[28] а болеста може да трае од триесет минути до три дена.[29] Превентивните мерки кои треба да се преземат за да се спречи ширењето на болеста вклучуваат миење на рацете со сапун и вода пред подготовка на храната. Лицата кои работат на подготовка на храна, ако се клицоносители или болни со стафилококна инфекција, треба да носат ракавици доколку имаат отворени рани на рацете или на зглобовите. Доколку храната се чува подолго од 2 часа пред употреба, тоа да се прави на температура над 60°С или под 4°С.[30]
S. aureus е бактеријата што најчесто е одговорна за сите поголеми коскени и зглобни инфекции. Овие инфекции се јавуваат во форма на: остеомиелит, септички артритис или инфекции при ортопедски интервенции.[31]
S. aureus е водечка причина за бактериемија во индустријализираните земји.[31] Инфекцијата е поврзана со продор низ кожата и мукозните мембрани при повреди, операции или употреба на интраваскуларни апликатори како што се катетери, при хемодијализа или парентерална терапија. Навлегувањето на бактериите во крвотокот може да доведе до инфективен ендокардит, септички артритис, остеомиелит и сепса.[31] Бактериемијата е најчеста и најтешка кај многу млада и многу стара популација.
Стапката на морталитет од бактериемија со S. aureus, доколку не е третирана со антибиотици, е исклучително висока и изнесува околу 80%.[5] Со антибиотски третман, стапката на морталитет изнесува 15% - 50% во зависност од возраста и здравјето на пациентот, како и на антибиотската резистенција на бактеријата.[5]
S. aureus често може да се најде во биофилмови формирани на медицински уреди имплантирани во телото. Често се среќава заедно со Candida albicans во биофилмовите. Се смета дека Candida albicans му овозможува на S. aureus да навлезе во човековото ткиво.[32] Во вакви случаи стапката на морталитет расте.[33]
S. aureus се среќава кај кучињата,[34] мачките,[35] коњите,[36] и може да предизвика болест на нозе кај птици и глодачи.[37] Некои сметаат дека кучињата на здравствените работници треба да се сметаат за значаен извор на антибиотски-резистентни S. aureus, особено во време на епидемија.[34]
S. aureus е еден од причинителите на маститис кај млечните крави. Бактеријата се штити од имунолошкиот систем на кравата со создавање на големи полисахаридни капсули.[38]
S. aureus произведува повеќе ензими: коагулаза (врзана и слободна коагулаза) ја коагулира плазмата, ја прекрива бактериската клетка, веројатно за да се спречи фагоцитоза; хијалуронидаза (позната и како фактор на ширење) ја разградува хијалуронската киселина и помага во ширењето на бактеријата; деоксирибонуклеаза (ДНКаза) ги разградува ДНК молекулите; липаза, ги разградува липидите; стафилокиназа, го раскинува фибринот и помага во ширењето; бета-лактамаза, ензим одговорен за резистентност кон бета-лактамски антибиотици.[39]
Во зависност од сојот, S. aureus е способен за секреција на неколку егзотоксини, кои може да се категоризираат во три групи. Многу од овие токсини се поврзани со специфични болести.[40]
Постојат голем број на мали РНК молекули кои се вклучени во контролата на бактериската вирулентност кај S. aureus; на пример, RNAIII,[45] SprD,[46] RsaE,[47] SprA1,[48] SSR42,[49] ArtR,[50] SprX и Teg49.[51]
Утврдено е дека многу информациски РНК молекули (иРНК) кај S. aureus носат три примарни нетранслатирани региони (3'UTR) подолги од 100 нуклеотиди, кои потенцијално имаат регулаторна функција.[52]
Понатамошното проучување на icaR иРНК (иРНК која кодира за репресорот на главното полисахаридно соединение на матрицата на бактерискиот биофилм) покажало дека 3' UTR врзувањето за 5' UTR може да интерферира со комплексот за иницијација на транслација и да генерира двојно-верижен супстрат за рибонуклеаза III. Се покажало дека интеракцијата е меѓу UCCCCUG мотивот во 3' UTR и Shine-Dalagarno регионот на 5' UTR. Бришењето на мотивот резултира со акумулација на icaR репресорот и инхибиција во создавањето на биофилм. Создавањето на биофилм е главната причина за стафилококни инфекции кај импланти.[53]
Белковината А се зацврстува за пентаглицинските мостови (синџири од пет глицински остатоци) на пептидогликанот со помош на транспептидазата сортаза А.[54] Тој е врзувач на имуноглобулин G (IgG) и се врзува на Fc регионот на антителата. Истражувањата со мутација на гените кои ја кодираат белковината А покажале намалена вирулентност на S. aureus (со мерење на нивно преживување во крв), што доведе до шпекулации дека белковината А придонесува за вирулентноста преку врзување на Fc регионот на антителата.[55]
Белковината А во различни рекомбинантни форми се користи со децении за врзување и пречистување на антитела со имуноафинитетна хроматографија. Транспептидазите, како што се сортазите одговорни за врзување на белковината А за пептидогликанот, се изучуваат со надеж за развој на нови антибиотици кои би ги таргетирале MRSA инфекциите.[56]

Некои соеви на S. aureus се способни за синтеза на стафилоксантин — златно-обоен каротиноиден пигмент. Овој пигмент делува како фактор на вируленција, на тој начин што како антиоксиданс ги неутрализира реактивните кислородни видови кои имуниот систем ги создава за да го убие патогенот.[57][58]
Мутантите на S. aureus со недостаток на гени за синтеза на стафилоксантин имаат помала веројатност да преживеат инкубација со оксиданси, како што е водород пероксидот, во споредба со нормалните клетки кои го продуцираат пигментот. Мутантните колонии брзо се уништуваат од страна на неутрофилите, додека многу од пигментираните колонии би преживеале.[57] Пигментираните соеви инокулирани во рани на глувци предизвикуваат апсцеси кои бавно заздравуваат, а раните инфицирани со непигментираните соеви брзо исцелуваат.
Овие тестови покажуваат дека Staphylococcus соевите го употребуваат стафилоксантинот како одбрана против човековиот имунолошки систем. Лековите за инхибирање на синтезата на стафилоксантинот ја ослабнуваат бактерија и ја зголемуваат нејзината осетливост кон антибиотици. Поради сличностите во биосинтетските патишта на стафилоксантинот и човековиот холестерол, најдено е дека еден лек за намалување на нивото на холестерол во крвта способен е да ја инхибира пигментацијата на S. aureus и прогресијата на болеста.[59]

Дијагнозата се поставува со земање на соодветен примерок и испраќање во лабораторија за биохемиска идентификација и ензимски тестови. Прво се прави боење по Грам, со кој се докажува типична Грам-позитивна кока, аранжирана во гроздовидна формација. Потоа се прави култивирање на селективен медиум - агар кој содржи манитол и 7-9% NaCl, кој овозможува S. aureus да расте и создава жолти колонии, како резултат на ферментација на манитолот и пад на pH на медиумот.
За диференцирање на видовите се користат ензимските тестови: каталаза тест (позитивен за сите Staphylococcus видови), коагулаза тест (згрутчување на фибринот, позитивен за S. aureus), ДНК-аза тест (зона на расчистување на ДНК-аза агар), липаза тест (жолта боја и мирис на ужегната маст), и фосфатаза тест (розова боја).
Неодамнешните напредоци во генетиката овозможија сигурни и брзи техники за идентификација и карактеризација на клинички изолати на S. aureus во реално време. Овие алатки ги поддржуваат стратегиите за контрола на инфекцијата за да го ограничат ширењето на бактериите и да обезбедат соодветна употреба на антибиотици. Квантитативната полимераза верижна реакција (анг. Real-Time Polymerase Chain Reaction) или скратено RTPCR, сè повеќе се користи за да се идентификуваат епидемии на инфекција.[60][61]
При следење на еволуцијата на S. aureus и неговата способност да се прилагоди на секој изменет антибиотик, се користат два основни методи познати како „бенд-засновани“ или „засновани на секвенца“.[62] Имајќи ги предвид овие две методи, другите методи, како што се multilocus sequence typing (MLST), pulsed-field gel electrophoresis (PFGE), bacteriophage typing, spa locus typing, и SCCmec typing, често се користат повеќе од останатите.[63] Со овие методи може да се утврди каде настанале соевите на MRSA, и каде се во дадениот момент.[64]
Со MLST, оваа техника на типизација користи фрагменти од неколку универзални клеточни гени познати како aroE, glpF, gmk, pta, tip и yqiL. На овие секвенци потоа им се доделува број кој дава низа од неколку броеви кои служат како профил на алели. Иако ова е честа метода, нејзино ограничување е одржувањето на микроарејата која ги детектира новоалелните профили, што го прави експериментот скап и бавен.[62]
Со PFGE, метод кој сè уште е многу користен, а датира од 1980-тите години, овозможено е да се направи диференцијација на изолатите на MRSA.[64] Оваа техника користи повеќекратна гел електрофореза, заедно со напонски градиент за прикажување на јасни резолуции на молекулите. S. aureus фрагментите транзитираат низ гелот, правејќи специфични линиски формации кои подоцна се споредуваат со други изолати со цел идентификување на сродните соеви. Ограничувањата на методот вклучуваат практични тешкотии со униформни линиски формации и неговата чувствителност.
Spa locus typing е популарна техника која користи една локус зона во полиморфен регион на S. aureus за да се разликува каква било форма на мутации.[64] Иако оваа техника е често евтина и одзема помалку време, шансата за губење на дискриминаторската моќ го отежнува диференцирањето помеѓу MLST CCs, што претставува суштинско ограничување.
Третманот од избор за инфекции со S. aureus е пеницилин. Пеницилинот го инхибира формирањето на вкрстени врски кај пептидогликанот, кои обезбедуваат ригидност и јачина на бактерискиот клеточен ѕид. Четиричлениот β-лактамски прстен на пеницилинот се врзува за ензимот DD-транспептидаза, кој, кога е функционален, ги синтетизира вкрстените врски на пептидогликанот кој го формира ѕидот на бактериската клетка. Врзувањето на β-лактамот за DD-транспептидазата ја инхибира функционалноста на ензимот, кој повеќе не може да го катализира формирањето на вкрстените врски. Како резултат на тоа, формирањето и деградацијата на бактерискиот клеточен ѕид стануваат неусогласени процеси, што резултира со смрт на бактеријата. Меѓутоа, во повеќето земји, резистентноста кон пеницилин е многу честа, а прва линија на терапија најчесто е β-лактамски антибиотик резистентен на пеницилиназа (на пример, оксацилин или флуклоксацилин, кои имаат ист механизам на дејство како пеницилинот). Комбинираната терапија со гентамицин може да се користи за лекување на сериозни инфекции, како што е ендокардитот,[65][66] но неговата употреба е контроверзна поради високиот ризик од оштетување на бубрезите.[67] Времетраењето на третманот зависи од местото и тежината на инфекцијата. Рифампицинот кој порано се користел како адјуванс на пеницилинскиот третман на бактериемија со S. aureus, покажал дека нема предности во однос на стандардната терапија со антибиотици.[68]
Отпорноста на антибиотици кај S. aureus била невообичаена кога пеницилинот првпат бил воведен во 1943 година. Всушност, првичната Петриева плоча на која Александар Флеминг од Кралскиот колеџ во Лондон ја набљудувал антибактериската активност на габата Penicillium, содржела култура на S. aureus. Веќе до 1950 година, 40% од болничките S. aureus изолати биле отпорни на пеницилин, а до 1960 година, процентот се зголемил на 80%.[69]
MRSA е еден од бројните соеви на S. aureus кои станале отпорни на повеќето β-лактамски антибиотици. Поради оваа причина, ванкомицин, кој е гликопептиден антибиотик, најчесто се користи за борба против MRSA. Ванкомицин ја инхибира синтезата на пептидогликанот, но за разлика од β-лактамските антибиотици, гликопептидните антибиотици целно се врзуваат за аминокиселините во клеточниот ѕид, спречувајќи го формирањето на вкрстените врски во пептидогликанот. MRSA соевите најчесто се наоѓаат поврзани со институции како што се болниците, но стануваат се поприсутни во инфекции стекнати во заедницата.
Малите инфекции на кожата може да се третираат со тројна антибиотска маст.[70]
Стафилококната отпорност кон пеницилин е посредувана од производство на пеницилиназа (облик на β-лактамаза): ензим кој го расцепува β-лактамскиот прстен на молекулата на пеницилин, правејќи го антибиотикот неефективен. β-лактамските антибиотици отпорни на пеницилиназа, како што се метицилин, нафцилин, оксацилин, клоксацилин, диклоксацилин и флуклоксацилин, се отпорни на разградување со стафилококна пеницилиназа.
Отпорноста кон метицилинот е посредувана преку mec оперонот, кој е дел од стафилококната cassette chromosome mec (SCCmec). Отпорноста се добива од mecA генот, кој кодира изменет пеницилиноврзувачка белковина (PBP2a или PBP2 ') кој има помал афинитет за врзување на β-лактами (пеницилини, цефалоспорини и карбапенеми). Ова дава резистентност кон сите β-лактамски антибиотици и ја спречува нивната клиничка употреба за инфекции со MRSA. Затоа, гликопептидот ванкомицин често се користи против MRSA.
Аминогликозидните антибиотици, како што се канамицин, гентамицин, стрептомицин и други, некогаш биле ефикасни против стафилококните инфекции, сè додека соевите не еволуирале механизми за да го инхибираат дејството на аминогликозидите, кое се случува преку протониран амин и/или хидроксил интеракција со рибозомната РНК на бактериската 30S рибозомна подединица.[71] Во моментов прифатени се три главни механизми за развој на отпорност кон аминогликозидите: ензими кои ги модифицираат аминогликозидите, рибозомни мутации и активно исфрлање на лекот надвор од бактериската клетка.
Аминогликозид-модифицирачките ензими го онеспособуваат аминогликозидот со ковалентно поврзување на фосфат, нуклеотид или ацетилна група за клучната аминска или алкохолна функционална група на антибиотикот. Ова го менува полнежот или стерично го попречува антибиотикот, намалувајќи го афинитетот за врзување за рибозомот. Во S. aureus, најдобро карактеризираниот аминогликозид-модифицирачки ензим е аминогликозид аденилилтрансфераза 4 'IA (ANT (4') IA). Структурата на овој ензим е откриена со рендгенска кристалографија.[72] Ензимот е способен да прикачи аденил група на 4' хидроксилната група на многу аминогликозиди, вклучувајќи ги и камамицин и гентамицин.
Отпорност кон гликопептидите е посредувана со здобивање на vanA генот, кој потекнува од ентерококите и кодира ензим кој произведува алтернативен пептидогликан, за кој ванкомицинот не може да се поврзе.
Денес, S. aureus стана отпорен на често употребуваните антибиотици. Во Велика Британија, само 2% од сите изолати на S. aureus се чувствителни на пеницилин, а слично е и во остатокот од светот. Пеницилините отпорни на β-лактамаза (метицилин, оксацилин, клоксацилин и флуклоксацилин) биле развиени за третман на пеницин-резистентните S. aureus соеви и сè уште се користат како прва линија на третман. Метицилинот бил првиот припадник на оваа класа антибиотици (воведен во 1959 година), но, само две години подоцна, првиот случај на MRSA бил пријавен во Англија.[73]
И покрај тоа, MRSA генерално остана невообичаен наод, дури и во болнички услови, сè до 1990-тите години, кога преваленцата на MRSA во болниците експлодирала и сега е ендемска.[74]
Инфекциите со MRSA во болници и во заедници најчесто се третираат со не-β-лактамски антибиотици, како што се клиндамицин и котримоксазол (исто така познат како триметоприм/сулфаметоксазол). Резистентноста кон овие антибиотици, исто така, доведе до употреба на нови, анти-Грам-позитивни антибиотици со широк спектар, како што е линезолид, поради неговата достапност како орален лек. Терапија од прв избор за сериозни инвазивни инфекции од MRSA, во моментов, се гликопептидни антибиотици (ванкомицин и теикопланин). Сепак, постојат голем број проблеми со овие антибиотици, како што се потребата за интравенска администрација (не е достапна орална примена), токсичност и потреба за редовно следење на нивоата на лековите со крвни тестови. Исто така, гликопептидните антибиотици не пробиваат многу добро во некои инфицирани ткива (ова е особено загрижувачки кај инфекции на мозокот и менингите и кај ендокардитис). Гликопептидите не смеат да се користат за третман на метицилин-чувствителните S. aureus (MSSA), бидејќи резултатите се инфериорни.[75]
Поради високиот степен на резистенција кон пеницилините и поради потенцијалот на MRSA да развие отпорност кон ванкомицин, Американскиот центар за контрола и превенција на болести објави упатства за соодветна употреба на ванкомицинот. Во случаи каде инциденцата на инфекции со MRSA е познато дека е висока, лекарот може да избере да користи гликопептиден антибиотик додека не се открие идентитетот на инфективниот организам. Доколку се потврди дека инфекцијата е резултат на сој на S. aureus чувствителен на метацилин, третманот треба да се смени со флуклоксацилин или пеницилин, како што е соодветно.
Ванкомицин-резистентниот S. aureus (VRSA) е сој кој стана отпорен на гликопептидите. Првиот случај на ванкомицин-интермедиерен S. aureus (VISA) бил пријавен во Јапонија во 1996 година;[76] но првиот случај на S. aureus кој е навистина резистентен кон гликопептидни антибиотици бил објавен во 2002 година.[77] Три случаи на инфекција со VRSA биле пријавени во САД до 2005 година.[78]
Околу 33% од американската популација се носители на S. aureus и околу 2% се носители на MRSA.[79]
Клицоносителството на S. aureus е важен извор на болнички инфекции (познати и како нозокомијални) и MRSA стекнати во заедницата. Иако S. aureus може да биде присутен на кожата на домаќинот, поважно е клицоносителството во горниот респираторен тракт, а може да биде присутен и во ушите.[80] Можноста на носните канали да се носители на S. aureus е резултат на комбинација од ослабен или дефектен имунитет на домаќинот и способноста на бактеријата да го избегне вродениот имунитет на домаќинот.[81] Носното клицоносителство е, исто така, имплицирано за развој на стафилококни инфекции.[82]
Ширењето на S. aureus (вклучувајќи MRSA) генерално е преку директен контакт човек со човек, иако неодамна некои ветеринари откриле дека инфекцијата може да се шири преку домашните миленици,[83] а загадувањето на животната средина се смета дека не е толку релевантно. Основните начини на миење на рацете се ефикасни во спречувањето на неговото пренесување. Употребата на заштитна облека и ракавици за еднократна употреба од страна на персоналот, го намалува контактот на кожа со кожа, со што се намалува ризикот од пренесување.
Неодамна, бројни случаи на S. aureus се пријавени во болниците низ САД. Преносот на патогенот се олеснува во медицински услови каде хигиената на здравствениот работник е недоволна. S. aureus е неверојатно отпорна бактерија, како што било покажано во една студија каде што бактериите преживеале на полиестер околу три месеци;[84] полиестерот е главниот материјал што се користи во завесите за приватност во болниците.
Бактериите се пренесуваат на рацете на здравствените работници, кои можат да ги соберат од навидум здрав пациент кој носи доброќуден или комензален сој на S. aureus, а потоа го пренесуваат на следниот пациент. Влезот на бактерии во крвотокот може да доведе до разни компликации, вклучувајќи ендокардитис, менингитис и сепса.
Етанолот се покажал како ефикасен топичен дезифициенс против MRSA. Кватенерни амониумови катјони може да се користи заедно со етанолот за да се зголеми времетраењето на дезинфекционото дејство. Превенцијата на нозокомијални инфекции вклучува рутинско и терминално чистење. Незапалива алкохолна пареа во CO2 NAV-CO2 системите имаат предност, бидејќи не оштетуваат метали или пластика што се користат во медицинските средини и не придонесуваат за антибактериска отпорност.
Важен, но претходно несогледан начин за MRSA колонизација и пренос е сексуалниот контакт.[85]
S. aureus се уништува за една минута на 78 °C и за десет минути на 64 °C.[86]
Одредени соеви на S. aureus се опишани како отпорни на дезинфекција со хлор.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.