
Натриум карбонат
хемиско соединение / From Wikipedia, the free encyclopedia
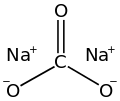
Натриум карбонат (исто така познат како сода за перење, сода и кристална сода) — неорганско соединение со формулата Na
2CO
3 и неговите различни хидрати. Сите форми се бели, без мирис, растворливи во вода соли кои даваат алкални раствори во водата. Историски гледано, тој бил извлечен од пепелта на растенија одгледувани во почви богати со натриум. Бидејќи пепелта на овие растенија богати со натриум била значително различна од пепелта од дрво (кога се користела за производство на поташа), натриум карбонат станал познат како „сода пепел“.[13] Се произведува во големи количини од натриум хлорид и варовник со Солвејскиот процес, како и со карбонирање на натриум хидроксид кој се прави со процесот на хлор-алкали.
 | |
 | |
Назив според МСЧПХ Натриум карбонат | |
Претпочитано име по МСЧПХ: Динатриум карбонат | |
Други називи Сода пепел, сода за перење, сода кристали, натриум триоксокарбонат | |
| Назнаки | |
|---|---|
| 497-19-8 (безводен) 5968-11-6 (монохидрат) 6132-02-1 (декахидрат) | |
| ChEBI | CHEBI:29377 |
| ChEMBL | ChEMBL186314 |
| ChemSpider | 9916 |
| EC-број | 207-838-8 |
| 3Д-модел (Jmol) | Слика |
| PubChem | 10340 |
| RTECS-бр. | VZ4050000 |
| |
| UNII | 45P3261C7T 2A1Q1Q3557 (monohydrate) LS505BG22I (decahydrate) |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | Бело цврсто, хигроскопско |
| Мирис | Без мирис |
| Густина | |
| Точка на топење | |
Безводен, g/100 mL:
| |
| Растворливост | Растворлив во алкали,[3] глицерол етанол CS2, ацетон, ацетат, алкохол амонијак[4] |
| Растворливост во глицерин | 98.3 g/100 g (155 °C)[4] |
| Растворливост во етанедиол | 3.46 g/100 g (20 °C)[5] |
| Растворливост во диметилформамид | 0.5 g/kg[5] |
| Киселост (pKa) | 10.33 [6] |
Магнетна чувствителност (χ) |
−4.1·10−5 cm3/mol[2] |
| Показател на прекршување (nD) | 1.485 (безводен) 1.420 (монохидрат)[7] 1.405 (декахидрат) |
| Вискозност | 3.4 cP (887 °C)[5] |
| Структура | |
| Кристална структура | Monoclinic (γ-form, β-form, δ-form, безводен)[8] Orthorhombic (монохидрат, хептахидрат)[1][9] |
Просторна група |
C2/m, No. 12 (γ-form, безводен, 170 K) C2/m, No. 12 (β-form, безводен, 628 K) P21/n, No. 14 (δ-form, безводен, 110 K)[8] Pca21, No. 29 (монохидрат)[1] Pbca, No. 61 (хептахидрат)[9] |
Константа на решетката |
|
Константа на решетката |
|
| Octahedral (Na+, безводен) | |
| Термохемија | |
| Ст. енталпија на формирање ΔfH |
−1130.7 kJ/mol[2][5] |
| Стандардна моларна ентропија S |
135 J/mol·K[2] |
| Специфичен топлински капацитет, C | 112.3 J/mol·K[2] |
| Опасност | |
| Безбедност при работа: | |
Главни опасности |
Надразнувачки |
| GHS-ознаки: | |
Пиктограми |
 [10] [10] |
Сигнални зборови |
Опасен |
Изјави за опасност |
H319[10] |
Изјави за претпазливост |
P305+P351+P338[10] |
| NFPA 704 | |
| Смртоносна доза или концентрација: | |
LD50 (средна доза) |
4090 mg/kg (rat, oral)[12] |
| Безбедносен лист | MSDS |
| Слични супстанци | |
| Други анјони | Сода бикарбона |
| Други катјони | Литиум карбонат Калиум карбонат Рубидиум карбонат Цезиум карбонат |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
