From Wikipedia, the free encyclopedia
Azoto rūgštis (pagal naujausią IUPAC nomenklatūrą nitrato rūgštis) – stipri neorganinė rūgštis. Cheminė formulė HNO3. Tai koroziją sukeliantis ir nuodingas junginys. Sukelia odos nudegimus. Net nuo mažos koncentracijos tirpalų oda kuriam laikui pagelsta. Todėl reikia imtis papildomų atsargumo priemonių dirbant su šia medžiaga.
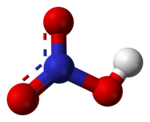
| Azoto rūgštis | |
|---|---|
  | |
| Sisteminis (IUPAC) pavadinimas | |
| Azoto rūgštis | |
| CAS numeris | 7697-37-2 |
| RTECS numeris | QU5775000 |
| Cheminė formulė | HNO3 |
| Molinė masė | 63,012 g/mol |
| SMILES | O[N+](=O)[O-] |
| Rūgštingumas (pKa) | |
| Bazingumas (pKb) | |
| Valentingumas | |
| Fizinė informacija | |
| Tankis | |
| Išvaizda | bespalvis skystis |
| Lydymosi t° | -42 °C, 231 K, -44 °F |
| Virimo t° | 83 °C, 356 K, 181 °F |
| Lūžio rodiklis (nD) | |
| Klampumas | |
| Tirpumas H2O | |
| Šiluminis laidumas | |
| log P | |
| Garavimo slėgis | |
| kH | |
| Kritinis santykinis drėgnumas | |
| Farmakokinetinė informacija | |
| Biotinkamumas | |
| Metabolizmas | |
| Pusamžis | |
| Pavojus | |
| MSDS | |
| ES klasifikacija | Oksiduojanti (O), Ėsdinanti (ardanti) (C) |
| NFPA 704 | |
| Žybsnio t° | |
| Užsiliepsnojimo t° | |
| R-frazės | R8, R35 |
| S-frazės | (S1/2), S23, S26, S36, S45 |
| LD50 | |
| Struktūra | |
| Kristalinė struktūra | |
| Molekulinė forma | |
| Dipolio momentas | 2,17 ± 0.02 D |
| Simetrijos grupė | |
| Termochemija | |
| ΔfH |
|
| Giminingi junginiai | |
| Giminingi grupė | |
| Giminingi junginiai | Nitrozilo hidroksidas, Diazoto pentaoksidas |
| Giminingos grupės | |
Azoto rūgštis, kurios koncentracija yra didesnė nei 70 %, vadinama koncentruota. Jei koncentracija viršija 86 %, tokia azoto rūgštis vadinama rūkstanti azoto rūgštis. Rūkstanti azoto rūgštis skirstoma į baltą ir raudoną. Raudona spalva gali atsirasti, jei iš rūgšties išsiskiriantys raudonai rudi NO2 garai reaguoja su rūgštyje esančiu vandeniu ir taip pasigamina nitritinė rūgštis.
Azoto rūgšties pKa yra −2 vandeniniame tirpale, taigi ji pilnai skyla į NO3- ir H+ jonus. Azoto rūgšties druskos vadinamos nitratais, jos puikiai tirpsta vandenyje ir kituose poliniuose tirpikliuose.
Kambario temperatūroje rūgštis skyla ir po skilimo išsiskiriantys azoto oksidai matomi kaip geltoni, rudi ar raudoni dūmai. Dar greitesnis skilimas kaitinant šviesoje. Lygtis:
Jei ji karšta ir koncentruota tai labiau linkusi reaguoti kaip oksidatorius.
Praskiesta jau reaguoja panašiau kaip ir kitos stiprios rūgštys.
Dėl tokių savybių H2 retai susidaro. Tik magnis ir kalcis išstumia vandenilį iš HNO3 „paprastai“, bet ir tuomet reikia šaldyti ir naudoti skiestą rūgštį.
Koncentruota azoto rūgštis nereaguoja (tiksliau sakyti reaguoja nepalyginamai lėčiau nei skiesta) su dauguma metalų. Tai vadinama oksidaciniu pasyvavimu.
Baltymai reaguodami su koncentruota azoto rūgštimi – suyra, susidaro ryškiai geltonos spalvos medžiaga, tokia reakcija yra vadinama ksantoproteinine ir yra naudojama baltymams atpažinti.[1]
Visų pirma tai esminė medžiaga gaminant daugumą sprogmenų ir trąšų. Taip pat ji svarbi vaistų gamyboje. Azoto rūgštis panaudojama gaunant tokias medžiagas: Nitroglicerinas, TNT, RDX, PETN, Amonio nitratas.
Azoto rūgštis dar svarbi metalurgijoje, ypač tauriųjų metalų apdirbime. Azoto rūgšties mišinys su druskos rūgštimi dar žinomas kaip karališkasis vanduo, tai vienas iš nedaugelio reagentų tirpdančių net platiną ir auksą.
Kartais ji kaip stiprus oksidatorius naudojama raketų kurui.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.