
산화 리튬
화합물 / From Wikipedia, the free encyclopedia
산화 리튬(Lithium oxide)은 화학식 Li
2O을 갖는 무기 화합물이다. 백색 고체이다. 특별한 중요성을 보이지는 않으나 수많은 물질들이 Li2O를 기초로서 구성되어 있다. 예를 들어 스포듀민의 Li2O 함량은 8.03%이다.[2]
간략 정보 이름, 식별자 ...
 | |
 | |
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름
Lithium oxide | |
| 별칭
Lithia, Kickerite | |
| 식별자 | |
3D 모델 (JSmol) |
|
| ChemSpider |
|
| ECHA InfoCard | 100.031.823 |
PubChem CID |
|
| RTECS 번호 |
|
| UNII | |
CompTox Dashboard (EPA) |
|
| |
| |
| 성질 | |
| Li 2O | |
| 몰 질량 | 29.88 g/mol |
| 겉보기 | 하얀 고체 |
| 밀도 | 2.013 g/cm3 |
| 녹는점 | 1,438 °C (2,620 °F; 1,711 K) |
| 끓는점 | 2,600 °C (4,710 °F; 2,870 K) |
| 반응하여 LiOH를 형성 | |
| log P | 9.23 |
굴절률 (nD) |
1.644[1] |
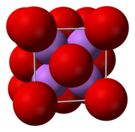
| 구조 | |
| 반형석 (입방 구조), cF12 | |
| Fm3m, No. 225 | |
배위 기하 구조 |
Tetrahedral (Li+); cubic (O2−) |
| 열화학 | |
열용량 (C) |
1.8105 J/g K or 54.1 J/mol K |
표준 몰 엔트로피 (S |
37.89 J/mol K |
표준 생성 엔탈피 (ΔfH⦵298) |
-20.01 kJ/g or -595.8 kJ/mol |
기브스 자유 에너지 (ΔfG˚) |
-562.1 kJ/mol |
| 위험 | |
| 주요 위험 | 부식성, 물과 강하게 반응 |
| NFPA 704 (파이어 다이아몬드) | |
| 인화점 | 타지 않음 |
| 관련 화합물 | |
다른 음이온 |
황화 리튬 셀레늄화 리튬 텔루륨화 리튬 폴로늄화 리튬 |
다른 양이온 |
산화 나트륨 산화 칼륨 산화 루비듐 산화 세슘 |
| 과산화 리튬 초과산화 리튬 | |
관련 화합물 |
수산화 리튬 |
닫기
