Loading AI tools
화합물 위키백과, 무료 백과사전
트레오닌(영어: threonine) (기호: Thr 또는 T)[2]은 단백질의 생합성에 사용되는 α-아미노산이다. 트레오닌은 α-아미노기(생물학적 조건에서 양성자화된 −NH+
3 형태), α-카복실기(생물학적 조건에서 탈양성자화된 −COO− 형태) 및 곁사슬인 하이드록실기를 포함하고 있다. 트레오닌은 극성 비전하 아미노산으로 분류된다. 트레오닌은 필수 아미노산으로 인체에서 합성되지 않으며 음식을 통해 섭취해야 한다. 트레오닌은 대장균과 같은 세균에서 아스파르트산으로부터 합성된다.[3] 트레오닌은 AC로 시작하는 모든 코돈(ACU, ACC, ACA, ACG)에 의해 암호화되어 있다.
 L-트레오닌의 골격 구조식 | |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
threonine | |||
| 별칭
2-amino-3-hydroxybutanoic acid | |||
| 식별자 | |||
3D 모델 (JSmol) |
| ||
| ChEBI |
| ||
| ChEMBL |
| ||
| ChemSpider |
| ||
| DrugBank |
| ||
| ECHA InfoCard | 100.000.704 | ||
| EC 번호 |
| ||
| |||
| KEGG |
| ||
PubChem CID |
| ||
| UNII |
| ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| C4H9NO3 | |||
| 몰 질량 | 119.120 g·mol−1 | ||
| (H2O, g/dl) 10.6(30°),14.1(52°),19.0(61°) | |||
| 산성도 (pKa) | 2.63 (카복실기), 10.43 (아미노기)[1] | ||
트레오닌의 곁사슬은 보통 수소 결합되어 있다. 형성되는 가장 일반적인 작은 모티프는 ST 턴, ST 모티프(보통 α 나선의 시작 부분) 및 ST 스테이플(일반적으로 α 나선의 중간 부분)이며, 이들은 세린과의 상호작용을 기반으로 한다.
트레오닌 잔기는 수 많은 번역 후 변형에 민감하다. 곁사슬의 하이드록실기는 O-결합 글리코실화를 겪을 수 있다. 또한 트레오닌 잔기는 트레오닌 키네이스에 의해 인산화된다. 트레오닌의 인산화된 형태는 포스포트레오닌이라고 할 수 있다. 포스포트레오닌은 3개의 잠재적인 배위 자리(카복실기, 아미노기, 인산기)를 가지고 있으며, 생물에서 생성되는 인산화된 리간드와 금속 이온 사이의 배위 방식을 결정하는 것은 생물학적 과정에서 포스포트레오닌의 기능을 설명하는 데 중요하다.[4]
트레오닌은 20가지의 단백질생성성 아미노산들 중에서 가장 나중에 발견되었다. 트레오닌은 1936년에 커티스 마이어(Curtis Meyer)와 윌리엄 커밍 로즈[5]가 공동으로 발견했다. 4탄당인 트레오스의 유도체로 분자식이 C4H8O5인 트레온산과 구조가 유사하기 때문에 트레오닌이라고 명명되었다.[6]
트레오닌은 아이소류신과 함께 2개의 입체 중심이 있는 2가지 단백질생성성 아미노산 중 하나이다. 트레오닌은 (2S,3R), (2R,3S), (2S,3S), (2R,3R)의 입체배치를 갖는 4가지 가능한 입체 이성질체로 존재할 수 있다. 그러나 L-트레오닌이라는 이름은 하나의 단일 입체 이성질체인 (2S,3R)-2-아미노-3-하이드록시뷰탄산에 사용된다. 자연계에는 거의 존재하지 않는 두 번째 입체 이성질체 (2S,3S)를 L-알로트레오닌이라고 한다.[7] 2가지 다른 입체 이성질체인 (2R,3S)-2-아미노-3-하이드록시뷰탄산과 (2R,3R)-2-아미노-3-하이드록시뷰탄산은 그다지 중요하지 않다.
트레오닌은 필수 아미노산으로 인체에서 합성되지 않으며, 식사를 통해 섭취해야 한다. 성인의 경우 매일 체중 1 kg당 20 mg의 트레오닌이 필요하다.[8] 식물과 미생물에서 트레오닌은 α-아스파르틸-세미알데하이드 및 호모세린을 거쳐 아스파르트산으로부터 합성된다. 호모세린은 O-인산화를 겪는다. 이 인산 에스터는 하이드록실기의 재배치와 함께 가수분해를 겪는다.[9] 트레오닌의 일반적인 생합성에 관여하는 효소는 다음과 같다.
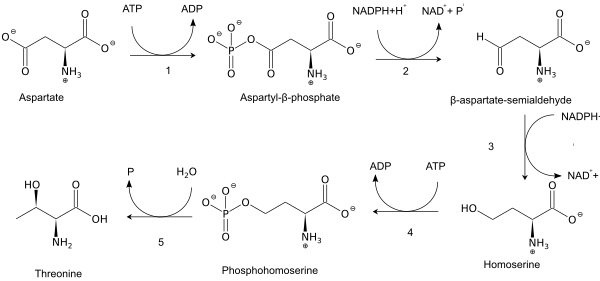 |
트레오닌은 적어도 세 가지 방식으로 대사된다.
트레오닌이 많이 함유된 식품으로는 코티지 치즈, 가금류, 생선, 고기, 렌즈콩, 검정거북콩,[15] 및 참깨가 있다.[16]
라세미 트레오닌은 아세트산 수은(II)을 사용하여 알파-기능화에 의해 크로톤산으로부터 제조할 수 있다. threonine can be prepared from crotonic acid by alpha-functionalization using mercury(II) acetate.[17]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.