메테인(영어: methane 메세인[*] [mɛθeɪn], CH
4) 또는 메탄(독일어: Methan)은 가장 간단한 탄소 화합물로, 탄소 하나에 수소 4개가 붙어 있다. 분자량은 16이다. 녹는점은 -183 °C, 끓는점은 -162 °C로 상온에서 기체이다.
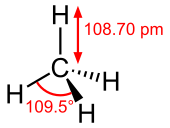 | |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Methane[1] | |||
| 체계명
Carbane (never recommended[1]) | |||
별칭
| |||
| 식별자 | |||
3D 모델 (JSmol) |
|||
| 3DMet | |||
| 1718732 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.739 | ||
| EC 번호 |
| ||
| 59 | |||
| KEGG | |||
| MeSH | Methane | ||
PubChem CID |
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1971 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| CH4 | |||
| 몰 질량 | 16.043 g·mol−1 | ||
| 겉보기 | 무색 기체 | ||
| 냄새 | Odorless | ||
| 밀도 |
| ||
| 녹는점 | −182.5 °C; −296.4 °F; 90.7 K | ||
| 끓는점 | −161.50 °C; −258.70 °F; 111.65 K[3] | ||
| 임계점 (T, P) | 190.56 K, 4.5992 MPa | ||
| 22.7 mg·L−1 | |||
| 용해도 | 에탄올, 다이에틸 에터, 벤젠, 톨루엔, 메탄올, 아세톤에 대해 가용성, 물에 대해 불용성 | ||
| log P | 1.09 | ||
헨리 상수 (kH) |
14 nmol·Pa−1·kg−1 | ||
| 짝산 | Methanium | ||
| 짝염기 | Methyl anion | ||
자화율 (χ) |
−12.2×10−6 cm3·mol−1 | ||
| 구조 | |||
점군 |
Td | ||
| Tetrahedron | |||
| 0 D | |||
| 열화학 | |||
열용량 (C) |
35.69 J·(K·mol)−1 | ||
표준 몰 엔트로피 (S |
186.25 J·(K·mol)−1 | ||
표준 생성 엔탈피 (ΔfH⦵298) |
−74.87 kJ·mol−1 | ||
표준 연소 엔탈피 (ΔcH⦵298) |
−891.1 to −890.3 kJ·mol−1 | ||
| 위험[4] | |||
| GHS 그림문자 |  | ||
| 신호어 | 위험 | ||
GHS 유해위험문구 |
H220 | ||
GHS 예방조치문구 |
P210 | ||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | −188 °C (−306.4 °F; 85.1 K) | ||
| 537 °C (999 °F; 810 K) | |||
| 폭발 한계 | 4.4–17% | ||
| 관련 화합물 | |||
관련 알케인 |
|||
자연적으로는 유기물이 물 속에서 부패, 발효할 때 생기므로 늪지대의 바닥 등에서 발생한다. 또 석탄층 속에 함유되어 석탄갱내에서 발생하여 공기와 섞여 폭발을 일으킬 때도 있다. 천연 가스나 석탄 가스의 주성분을 이룬다.
C-H의 결합 길이는 0.110nm이며, C-H의 결합 사이의 결합각은 109.5°이며, 무극성 분자이다.
순수한 메탄은 냄새가 없으나, 산업용으로 사용할 때 누출 여부 확인을 위해 냄새가 나는 다른 화합물을 일부 첨가하여 판매한다.[출처 필요]
천연 가스의 주성분으로, 연료로 많이 사용된다. 메탄 분자 하나를 태우면 이산화 탄소 한 분자와 물 두 분자가 생성된다. 반응식은 다음과 같다.
- CH4 + 2O2 → CO2 + 2H2O
메테인의 치환반응
메테인은 햇빛존재하에 상온의 염소와 반응하여 치환 반응을 하는데, 중심의 탄소와 공유결합을 하고있는 수소가 차례로 염소와 치환되어 성질이 다른 분자로 바뀌어간다.
바뀌는 순서는 다음과 같다.
각주
같이 보기
외부 링크
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.



