トップQs
タイムライン
チャット
視点
Fas受容体
ウィキペディアから
Remove ads
Fas受容体(Fasじゅようたい、英: Fas receptor、Fas、FasR)は、ヒトではFAS遺伝子にコードされるタンパク質であり、APO-1(apoptosis antigen 1、APT)、CD95(cluster of differentiation 95)、TNFRSF6(tumor necrosis factor receptor superfamily member 6)という名称でも知られる[5][6]。Fasはヒト線維芽細胞株FS-7によって免疫化を行ったマウスによって産生されたモノクローナル抗体を用いて最初に同定された。そのため、Fasという名称はFS-7-associated surface antigenの略称に由来する[7]。
Fas受容体は細胞表面に位置する細胞死受容体であり、そのリガンドであるFasリガンド(FasL)が結合した場合にプログラム細胞死(アポトーシス)をもたらす。この経路は2つのアポトーシス経路のうちの1つであり、もう1つはミトコンドリアを介した経路である[8]。
Remove ads
遺伝子
Fas受容体をコードする遺伝子は、ヒトでは10番染色体の長腕(10q24.1)、マウスでは19番染色体に位置する。ヒトの遺伝子は+鎖に位置し、長さは25,255塩基対で、タンパク質をコードする9つのエクソンからなる構成をしている。進化的に関連した類似の配列(オルソログ)は、大部分の哺乳類に存在している[9]。
タンパク質
8種類のスプライスバリアントが同定されており、7種類のアイソフォームへと翻訳される。アポトーシスを誘導するFas受容体がアイソフォーム1とされており、I型膜貫通タンパク質である。他のアイソフォームの多くは稀なハプロタイプであり、多くの場合は疾患と関係している。アポトーシスを誘導する膜貫通型アイソフォームと可溶型アイソフォームは正常な産物であり、選択的スプライシングによるこれらのアイソフォームの産生は細胞毒性を有するRNA結合タンパク質TIA1によって調節される[10]。
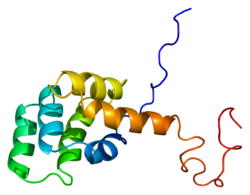
成熟型Fasタンパク質は319アミノ酸からなり、48 kDaと予測され、細胞外ドメイン、膜貫通ドメイン、細胞質ドメインの3つのドメインに分けられる。細胞外ドメインは157アミノ酸からなり、システイン残基に富む。膜貫通ドメインと細胞質ドメインはそれぞれ17アミノ酸、145アミノ酸からなる。エクソン1からエクソン5が細胞外領域をコードする。エクソン6は膜貫通領域、エクソン7からエクソン9は細胞内領域をコードする。
Remove ads
機能
要約
視点
Fasはリガンドの結合に伴って細胞死誘導性シグナル伝達複合体(death-inducing signaling complex、DISC)を形成する。隣接する細胞の表面の膜に固定されたFasリガンド三量体は、Fasのオリゴマー化を引き起こす。DISC中では、最大5分子から7分子のFasがオリゴマー化することが示唆されている[11]。
その後のデスドメイン(DD)の凝集に伴って、受容体複合体は細胞のエンドソーム装置を介してインターナリゼーションされる。その結果、アダプター分子であるFADDは自身のDDを介してFasのDDに結合できるようになる[12]。
FADDのN末端近傍にはデスエフェクタードメイン(DED)も存在し[13]、カスパーゼ-8(FLICE)のDEDへの結合を促進する。その後、カスパーゼ-8はp10サブユニットとp18サブユニットへの切断によって自身を活性化し、これら2つのサブユニットは活性型のヘテロ四量体酵素を形成する。活性型のカスパーゼ-8はDISCから細胞質基質へ放出されて他のエフェクターカスパーゼを切断し、最終的にはDNAの分解、膜のブレブの形成やその他アポトーシスの顕著な特徴が引き起こされる。
発がんプログレッションの過程でFasは高頻度でダウンレギュレーションされるか、細胞はアポトーシス抵抗性を獲得するが、Fasは腫瘍の成長を促進することも示されている。Fasはアポトーシス感受性をもたらすにもかかわらず、がん細胞は一般的にFasの構成的活性に依存しており、がんが産生するFasリガンドによって刺激されている[14]。
マウスモデルではこうしたFasの腫瘍成長促進が示されているが、ヒトのがんゲノミクスデータベースの解析では、FASは3131の腫瘍のデータセットで有意な局所的増幅はみられず、有意な局所的欠失がみられることから[15]、ヒトではがん抑制因子として機能していることが示唆される。
培養細胞では、FasリガンドはFas受容体を介してさまざまな種類のがん細胞でアポトーシスを誘導する。AOM/DSS誘発性結腸がんやMCA誘発性肉腫のマウスモデルでは、Fasががん抑制因子として作用することが示されている[16]。さらに、Fas受容体は腫瘍特異的細胞傷害性T細胞(CTL)による抗腫瘍細胞傷害も媒介する[17]。よく知られた標的に対するCTLの抗腫瘍細胞傷害に加えて、Fasは標的抗原を発現していない(バイスタンダー)細胞に対しても腫瘍細胞死を誘導する別の機能を持つとされる。CTLを介したバイスタンダー細胞死は1986年に報告され[18]、その後Fasを介した細胞溶解が原因であることがin vitroで示された[19]。また、二重特異性抗体を用いたin vitroでの研究や[20]、T細胞とCAR-T細胞を用いたin vivoでの研究でもFasを介したバイスタンダー腫瘍細胞の細胞死が実証されている[21]。
相互作用
FASは次に挙げる因子と相互作用することが示されている。
出典
関連文献
外部リンク
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads