トップQs
タイムライン
チャット
視点
アンフィンセンのドグマ
ウィキペディアから
Remove ads
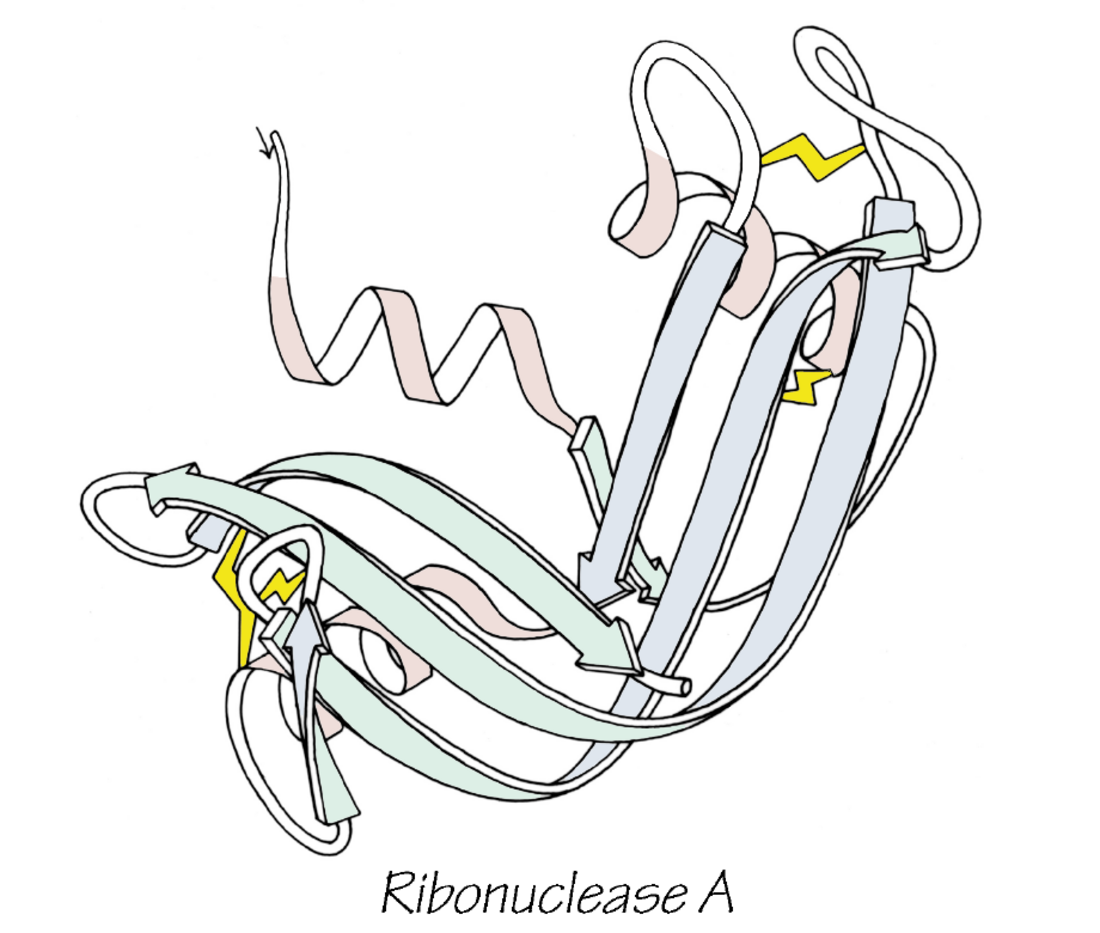
アンフィンセンのドグマ(英: Anfinsen's dogma)は、熱力学的仮説(英: thermodynamic hypothesis)としても知られる、分子生物学の仮説である。その仮説は、少なくとも標準的な生理学的環境における小さな球状タンパク質については、本来の構造はタンパク質のアミノ酸配列によってのみ決定されるというものである[1]。このドグマは、ノーベル賞受賞者[2]のクリスチャン B. アンフィンセンが、リボヌクレアーゼAの折りたたみ(フォールディングとも呼ぶ)に関する彼の研究から提唱したものである[3][4]。この仮説は、折りたたみが行われる環境条件(温度、溶媒濃度、組成など)において、本来の構造はユニークで安定しており、速度論的に到達可能な最小の自由エネルギーである、というものである。言い換えれば、ユニークなタンパク質構造を形成するには、次の3つの条件がある。
- 一意性
- その配列に、同等の自由エネルギーを持つ他の構成がないことが必要。したがって、その自由エネルギーの最小値はゆるぎのないものでなければならない。
- 安定性
- 周囲の環境が少し変化しただけでは、最小構成に変化を引き起こすことはできない。これは、自由エネルギー面を、スープ皿(複数の低エネルギー状態が密接に関連している)ではなく、漏斗(その底に天然状態がある)のように描くことができることを意味する。安定性を得るためには、天然状態の周りの自由エネルギー面はかなり急で高くなければならない。
- 運動学的到達性
- 自由エネルギー面におけるアンフォールド状態からフォールド状態への経路が適度に滑らかでなければならないこと、言い換えれば、鎖の折りたたみに(結び目などの高次立体構造のような)非常に複雑な形状の変化を伴わないことを意味する。

Remove ads
アンフィンセンのドグマへの挑戦
細胞内でのタンパク質のフォールディングは非常に複雑なプロセスであり、新たに合成されたタンパク質のターゲティングを経た適切な細胞内区画への輸送、恒久的なミスフォールディング(誤った折りたたみ)、一時的なアンフォールド状態(折りたたみの展開)、翻訳後修飾、品質管理、シャペロンにより促進されるタンパク質複合体の形成などが含まれる。
一部のタンパク質は、正しく折りたたむためにシャペロンタンパク質の助けを必要とする。これはアンフィンセンのドグマの反証を示唆している。ただし、シャペロンはタンパク質の最終的な状態に影響を与えないようで、その機能は主に、タンパク質が最終的に折りたたまれた状態になる前に、複数のタンパク質分子が凝集するのを防ぐ働きをするようである。ただし、対象となるタンパク質を適切に折りたたむには、少なくともいくつかのシャペロンが必要である[5]。
また、多くのタンパク質は、凝集やミスフォールドを起こす可能性がある。たとえばプリオンは、本来の折りたたみ状態とは異なるタンパク質の安定したコンフォメーションである。牛海綿状脳症では、天然タンパク質が、異なる安定したコンフォメーションに再折りたたみし、致命的なアミロイドの蓄積を引き起こす。アルツハイマー病やパーキンソン病などの他のアミロイド疾患も、アンフィンセンのドグマの例外である[6]。
タンパク質の中には、複数の固有の構造を持っていて、何らかの外部要因によってその折りたたみを変化させるものがある。たとえば、KaiBタンパク質複合体は、1日の中で折りたたみを切り替え、シアノバクテリアの時計として機能する。PDBタンパク質の約0.5 - 4 %がフォールドを切り替えると推定されている[7]。代替構造の切り替えは、タンパク質と低分子リガンドまたは他のタンパク質との相互作用、化学修飾(リン酸化など)、あるいは温度、pH、膜電位などの環境条件の変化によって促進される。それぞれの代替構造は、与えられた条件下でのタンパク質の自由エネルギーの大域的最小値に対応するか、より高い自由エネルギーの局所的最小値に動力学的に閉じ込められているかのいずれかである[8]。
Remove ads
参照項目
- タンパク質フォールディング
- タンパク質ダイナミクス
- プロテオパチー - タンパク質のミスフォールディングに関する疾患
脚注
推薦文献
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads