Loading AI tools
reazione chimica Da Wikipedia, l'enciclopedia libera
Ossidoriduzione o redox (composto dall'inglese reduction, riduzione e oxidation, ossidazione), in chimica, indica tutte quelle reazioni chimiche in cui cambia il numero di ossidazione degli atomi, cioè in cui si ha un passaggio di elettroni da una specie chimica a un'altra.[1]
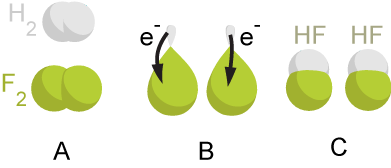
Questo tipo di reazione può variare da un semplice processo redox (come l'ossidazione del carbonio che genera diossido di carbonio o la riduzione del carbonio dall'idrogeno che produce metano), fino alla più complessa ossidazione degli zuccheri nel corpo umano, attraverso una serie di complicati processi di trasferimento degli elettroni.
Una reazione redox può essere pensata come lo svolgersi contemporaneo di due distinte "semireazioni":[1]
Quindi le semireazioni di riduzione e di ossidazione comportano sempre un cambiamento nel numero di ossidazione; in particolare un'ossidazione comporta un incremento del numero di ossidazione, mentre una riduzione comporta una diminuzione del numero di ossidazione.[1]
Le semireazioni di riduzione e ossidazione possono essere rappresentate nel seguente modo:[2]
essendo n il numero (o le moli) di elettroni scambiati durante la reazione, è uguale in entrambe le semireazioni.
La reazione redox globale può essere quindi rappresentata come:
In elettrochimica, le specie chimiche coinvolte direttamente nel processo di trasferimento di elettroni vengono dette «specie elettroattive», per distinguerle da eventuali altre specie chimiche presenti nel sistema che non subiscono riduzione o ossidazione.
Le reazioni chimiche di ossidoriduzione possono essere bilanciate con vari metodi, tra cui il "metodo ionico-elettronico". Questo metodo consiste nei seguenti passaggi:
Una reazione redox può avvenire in due modi:[3]
Nel caso di reazione in fase eterogenea all'interfaccia elettrodo-elettrolita, la reazione redox è preceduta e seguita da diversi stadi di reazione, per cui il meccanismo di reazione è in genere costituito dai seguenti stadi di reazione:[5][6]
A ciascuno di questi stadi è associata una sovratensione, cioè una variazione del potenziale di cella rispetto alle condizioni di equilibrio. In particolare si ha:
Allo stadio cineticamente determinante è associata la sovratensione più elevata.

Le reazioni di ossidoriduzione sono alla base di moltissimi processi biochimici essenziali alla vita (un esempio è la respirazione) e sono sfruttate per la produzione di composti chimici (ad esempio nel processo cloro-soda per ottenere cloro e idrossido di sodio) e nell'ambito della chimica elettroanalitica.
Se i reagenti vengono mantenuti separati ma viene garantito il contatto elettrico tramite materiali conduttori, è possibile intercettare il flusso di elettroni e sfruttarlo per produrre corrente elettrica continua, il cui potenziale dipende dalla natura chimica delle specie coinvolte. Tale principio viene sfruttato nella pila.
Una reazione di ossidoriduzione può avvenire spontaneamente o essere forzata in senso inverso tramite l'applicazione di un opportuno potenziale elettrico. Questo fenomeno è ampiamente sfruttato nelle pile ricaricabili e nelle batterie per autotrazione (che fungono da accumulatori di energia elettrica sotto forma di energia chimica), nonché nel processo di elettrolisi.
L'atomo di carbonio in natura si trova in differenti stati di ossidazione e in chimica organica il numero di ossidazione dipende da numerosi fattori; esso può essere anche frutto di una media che porta a un numero di ossidazione razionale (per esempio nel propino il numero di ossidazione medio dei carboni è pari a -4/3). Non si può quindi definire a priori una regola precisa, tuttavia generalmente il suo valore segue il seguente ordine:
Dove il carbonio assume valore +1 quando è legato con un elemento più elettronegativo, 0 quando è legato con un altro carbonio e -1 quando è legato con un elemento più elettropositivo: il carbonio avrà quindi numero di ossidazione pari a -4 nel metano e a +4 nell'anidride carbonica.
In generale quindi la concezione di ossidoriduzione in chimica organica è molto diversa rispetto a quella comune, sebbene il meccanismo sia analogo; infatti per riduzione di un carbonio generalmente si intende l'addizione di un idrogeno o di un elemento più elettropositivo del carbonio, come nell'idrogenazione di un alchene, mentre per ossidazione si intende l'addizione di un ossigeno o generalmente di un elemento più elettronegativo del carbonio, come in un'epossidazione.
Gli atomi di carbonio a diverso grado di ossidazione nel catabolismo ossidativo vengono portati al grado massimo di ossidazione (CO2) con recupero di energia (processo di respirazione). Il processo inverso invece che prevede l'anabolismo riduttivo del carbonio dell'anidride carbonica a carbonio organico è la fotosintesi clorofilliana.
In molti batteri questo non è possibile, in quanto non arrivano alla produzione di CO2, si fermano solamente agli alcoli. Questo processo dei batteri prende il nome di "fermentazione".
Quindi gli elettroni possono essere trasferiti da uno stato all'altro in quattro modi diversi:
Gli enzimi che catalizzano le reazioni di ossidoriduzione sono detti ossidoreduttasi. Alcuni importanti esempi di questa classe di enzimi sono le deidrogenasi e le flavoproteine. Le molecole che subiscono il processo di ossidoriduzione opposto (cioè si riducono se la sostanza organica si ossida, o viceversa) sono poche e sono detti "accettori di equivalenti riducenti". I più comuni sono: NAD, NADP, FAD, FMN.
Nell'ambito delle reazioni redox esistono due tipi di reazione molto particolari: reazioni redox influenzate da pH e reazioni di dismutazione.
Le prime sono delle reazioni il cui andamento è influenzato dal pH della soluzione di partenza; ciò vuol dire che a seconda del pH si possono ottenere diversi prodotti a partire dagli stessi reagenti. Un esempio di queste reazioni è la reazione dello ione permanganato MnO−4, la cui soluzione è di colore violaceo:
Nei casi di queste reazioni particolari è quindi necessario specificare il pH dell'ambiente di reazione.
Il secondo particolare tipo di ossidoriduzioni sono le cosiddette reazioni di dismutazione o disproporzione; più precisamente queste reazioni sono caratterizzate dalla contemporanea ossidazione e riduzione di una stessa specie chimica. I prodotti sono quindi specie chimiche diverse contenenti lo stesso elemento iniziale che in parte si è ridotto e in parte si è ossidato. Per il loro bilanciamento esistono due metodi ugualmente validi: prendendo, ad esempio, la reazione KClO → KClO3 + KCl si può bilanciare così:
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.