Carcinoma polmonare a piccole cellule
neoplasia polmonare Da Wikipedia, l'enciclopedia libera
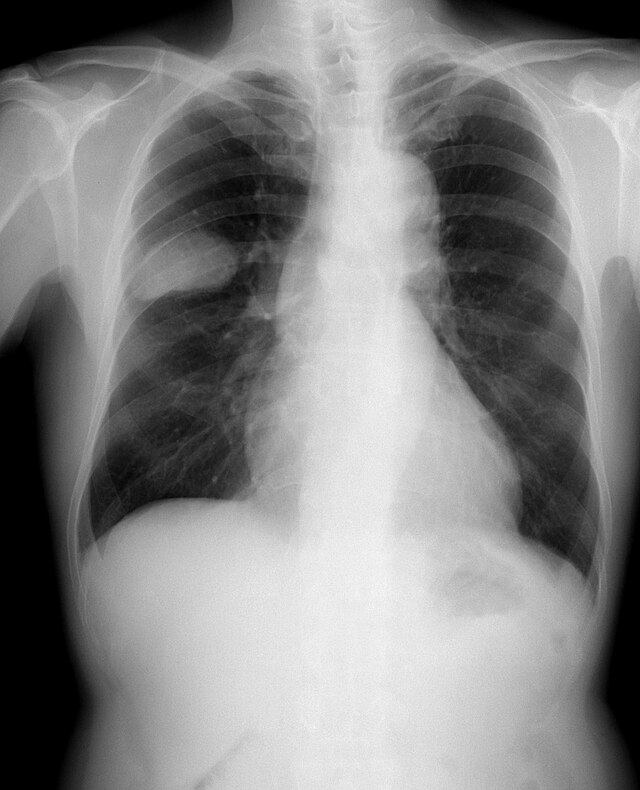
Il carcinoma polmonare a piccole cellule (SCLC) o microcitoma è una neoplasia polmonare che origina dalle cellule neuroendocrine dei grossi bronchi, caratterizzato da elevata malignità[1] e precoce capacità metastatica.[2]
Fattori di rischio
Il fumo di sigaretta costituisce il principale fattore di rischio per l'insorgenza di microcitoma,[3] tanto da sospettare un errore diagnostico se riscontrato in soggetti non fumatori.[4] Ulteriore fattore di rischio è l'esposizione al radon.
Classificazione
I tumori del polmone vengono divisi in non a piccole cellule (NSCLC) e a piccole cellule (SCLC); questi ultimi rappresentano il 16,8% di tutti i tumori polmonari.[5] Tale dicotomia rende conto delle profonde differenze terapeutiche, prognostiche e patogenetiche tra NSCLC e SCLC, configurandosi non solo come criterio di studio classificativo ed epidemiologico, ma anche come indice di mortalità e di speranza terapeutica. Un'ulteriore classificazione può essere posta in base alla preferenziale sede di insorgenza, essendo il microcitoma un tumore che colpisce quasi esclusivamente le zone centrali del polmone (tumore centrale).[6]
Epidemiologia
Il tumore del polmone a piccole cellule rappresenta il 16,8% di tutti i tumori del polmone.[7]

Anatomia patologica
Il microcitoma insorge preferenzialmente in sede ilare, con tipico interessamento delle vie respiratorie di calibro maggiore.[1] Lo sviluppo della massa tumorale è prevalentemente sottomucoso, anche se in alcuni casi possono essere presenti esfoliazioni bronchiali. Le cellule del microcitoma sono caratterizzate da un'elevata conta mitotica, con formazione di gruppi cellulari senza organizzazione squamosa o ghiandolare. Le cellule sono piccole, ovali o rotonde, con margini ben definiti. Il citoplasma è scarso, il materiale nucleare è finemente disperso e il nucleolo spesso è poco evidente.[2] La necrosi tissutale e perivascolare costituisce un reperto istologico comune. Tramite colorazioni immunoistochimiche è possibile ricercare marcatori neuroendocrini come la cromogranina, la sinaptofisina e la Leu-7, in virtù dell'origine dalle cellule del sistema APUD.[8] Un'ulteriore conferma può essere data ricercando il gene anti-apoptotico (vedi patogenesi) Bcl-2, iperespresso in oltre il 90% di questi tumori.[2] Occorre prestare particolare attenzione nella diagnosi differenziale tra SCLC e carcinoide polmonare atipico.
Patogenesi
Riepilogo
Prospettiva
Il microcitoma è un tumore che origina da cellule neuroendocrine presenti nell'epitelio bronchiale (cellule del sistema APUD); in particolare, rappresenta l'estremità maligna di una serie di tumori ad origine neuroendocrina di cui fanno parte il carcinoide tipico ed atipico e il carcinoma polmonare a grandi cellule. A differenza dei NSCLC, il microcitoma non è connesso con mutazione del recettore per EGF[9] o con un'alterazione della via di trasduzione legata alla proterina RAS;[10][11] questo tuttavia non significa che durante le fasi di progressione neoplastica non si possano sviluppare mutazioni a carico di questi geni. L'evento patogenetico scatenante è da ricercare nella mutazione dei geni della famiglia Myc che comprendono cMyc, MYCN e MYCL; in particolare, la mutazione di questi 2 ultimi è specifica del SCLC.[12][13] Ulteriori geni coinvolti nella specifica patogenesi del SCLC sono p53 e Bcl-2;[14] l'inattivazione del primo e la amplificazione del secondo, giustificano la capacità di evasione dalla apoptosi e la peculiare progressione neoplastica di questo tipo di tumore. Ultimamente l'attenzione è stata focalizzata nel gene CMRP1 (collapsin response mediator protein 1) che codifica una proteina implicata nei processi di regolazione dello sviluppo delle cellule del sistema nervoso;[15] l'alterata espressione di questa proteina nelle cellule tumorali potrebbe essere implicata nella precoce capacità metastatica propria del carcinoma polmonare a piccole cellule SCLC.[16]

Profilo clinico
Riepilogo
Prospettiva
Le manifestazioni cliniche del SCLC sono tipiche dei tumori centrali; la sintomatologia è in relazione al calibro del bronco interessato e della grandezza raggiunta dalla massa tumorale.[1] La tosse è in genere stizzosa e può essere scatenata da una inspirazione profonda;[4] è provocata sia dalla irritazione dell'epitelio bronchiale dovuta alla massa tumorale vegetante, sia dall'irritazione ostruttiva ed infiammatoria linfangitica. L'emoftoe è un segno clinico molto precoce.[6] L'ostruzione bronchiale favorisce inoltre il ristagno del materiale mucoso a valle, evento in grado di favorire episodi broncopneumonici recidivanti e febbre; l'ostruzione completa può portare all'atelettasia del segmento polmonare interessato. Il grado di dispnea può essere molto variabile,[7] in relazione soprattutto con la riserva respiratoria del malato e con il calibro del bronco interessato (maggiore è il calibro, maggiore è la dispnea). Segno tipico delle forme centrali è la presenza di tirage (rientramento inspiratorio degli spazi intercostali) e cornage (rumore aspro da stenosi), con rumori inspiratori assimilabili a fischi e fortemente connessi con il grado di infiltrazione tracheale sostenuta dal tumore polmonare. Deve essere sempre controllata la possibile comparsa di una sindrome mediastinica. Al di là delle caratteristiche cliniche dovute al quadro locale, il SCLC, in virtù della sua natura neuroendocrina, è in grado di realizzare una o più sindromi paraneoplastiche. Tra queste, è possibile riscontrare
- Sindrome da inappropriata secrezione di ADH[17]
- Sindrome di Cushing[18]
- Sindrome di Lambert-Eaton[19][20]
Astenia, anoressia, calo ponderale e anemizzazione sono segni gravissimi e tardivi della malattia neoplastica.
Profilo diagnostico e stadiazione
Riepilogo
Prospettiva
Una corretta diagnosi di tumore del polmone deve realizzarsi fornendo l'istotipo, la sede e la diffusione della malattia neoplastica. Quest'ultimo punto è particolarmente importante per SCLC, poiché non si usa la consueta stadiazione TNM ma è possibile distinguere due livelli di diffusione della malattia:
- malattia localizzata (Limited disease): malattia confinata ad un emitorace
- malattia in stadio avanzato (Extended disease): malattia presente al di fuori di un emitorace
Questa distinzione è fondamentale in quanto la forma localizzata può essere inserita in un unico campo di radioterapia.[21]
Come per tutte le forme neoplastiche polmonari, l'algoritmo diagnostico deve procedere partendo da anamnesi ed esame obiettivo, entrambe procedure atte ad identificare sintomi e segni tipici della malattia neoplastica polmonare e stabilire il migliore approccio strumentale. In seguito si procede con una radiografia del torace, in grado di evidenziare formazioni nodulari e di porre una prima diagnosi differenziale.[22] Nei casi dubbi si può ricorrere alla citologia dell'espettorato, ricercando le lesioni cellulari tipiche delle neoplasie polmonari; in associazione con tale esame è possibile effettuare una broncoscopia, che nel caso di SCLC risultata di particolare aiuto essendo una forma centrale (per definizione, raggiungibile con il broncoscopio) e per la possibilità di effettuare biopsia durante l'indagine. La biopsia è l'unico esame in grado di dimostrare e confermare la presenza di SCLC[21] e rappresenta lo svincolo dell'algoritmo diagnostico. In caso di positività per SCLC è necessario avvalersi della TAC e della PET al fine evidenziare la diffusione toracica e la presenza di metastasi a distanza;[22] ulteriori indagini devo essere fatte per scongiurare la presenza di metastasi in sede addominale, pelvica e cranica. La mediastinoscopia è un utile presidio per indagare il grado di invasione mediastinica, degli organi vicinori e delle stazioni linfonodali. I profili emato-chimici devono essere indagati per lo studio e il follow-up delle sindromi paraneoplastiche.[1]
Terapia
La chirurgia è sconsigliata.[4]
La forma limitata ad un emitorace risponde molto bene alla chemioterapia associata alla radioterapia, soprattutto con combinazioni farmacologiche che usino il cis-platino.[23] Possono essere usate anche combinazioni con carboplatino, gemcitabina, paclitaxel, vinorelbina, topotecano ed irinotecano.[24][25]
La malattia estesa non può attualmente essere guarita e la chemioterapia (a base di platino ed etoposide) ha quindi solo una finalità palliativa.
Le metastasi cerebrali possono essere controllate usando una radioterapia mirata e nella malattia localizzata può essere utile effettuare una radioterapia del cranio per prevenire la comparsa di lesioni secondarie cerebrali.
La malignità intrinseca del tumore e la rapida insorgenza di polichemioresistenza rendono la chemioterapia e la radioterapia presidi terapeutici non ancora in grado di portare alla risoluzione completa della malattia.[6] Tuttavia sia la chemioterapia sia la radioterapia sono interventi terapeutici di primaria importanza poiché offrono un miglioramento della qualità della vita e un aumento dell'aspettativa di vita.[26]
Note
Bibliografia
Voci correlate
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.

