Timeline
Chat
Prospettiva
Idruro di antimonio
composto chimico Da Wikipedia, l'enciclopedia libera
Remove ads
L'idruro di antimonio o stibina è il composto inorganico con formula SbH3. È il principale idruro covalente dell'antimonio ed è l'analogo più pesante di ammoniaca e fosfina. In condizioni normali è un gas incolore con un odore disgustoso simile a quello del solfuro di idrogeno (uova marce). È un gas estremamente tossico.
Remove ads
Remove ads
Storia
La stibina fu preparata per la prima volta indipendentemente da Lewis Thompson e Christoph Heinrich Pfaff nel 1837.[2][3] Occorse però molto tempo prima che le proprietà di questa sostanza tossica fossero determinate. Nel 1876 Francis Jones esaminò vari metodi di preparazione,[4] ma solo a partire dail 1901 Alfred Stock riuscì a determinare varie proprietà della stibina.[5][6]
Struttura molecolare e configurazione elettronica
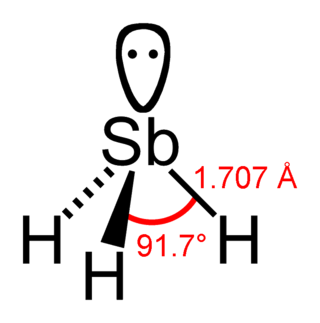
SbH3 è un composto molecolare; la struttura della molecola è piramidale, analogamente all'ammoniaca. Gli angoli di legame Sb–H sono di 91,6° e le distanze Sb–H sono di 170.4 pm.[7]
Sintesi
Riepilogo
Prospettiva
SbH3 è in genere preparato facendo reagire composti di Sb3+ con generatori di ioni H–:[8]
In alternativa si possono far reagire composti di Sb3– con reagenti protonici (come l'acqua stessa):
Remove ads
Reattività
Riepilogo
Prospettiva
Le proprietà chimiche di SbH3 assomigliano a quelle dell'arsina (AsH3):[9] Analogamente a tipici idruri pesanti come AsH3, H2Te e SnH4, anche SbH3 è instabile rispetto alla dissociazione negli elementi costituenti. Il gas si decompone lentamente a temperatura ambiente, e più rapidamente a 200 °C:
La decomposizione è autocatalitica e può essere esplosiva.
SbH3 è facilmente ossidato da ossigeno o anche dall'aria:
SbH3 è meno basico di PH3 ma può essere protonato con superacidi:[10]
Con basi molto forti SbH3 può anche essere deprotonato:
Remove ads
Usi
SbH3 di elevata purezza è usato nell'industria dei semiconduttori per drogare il silicio con il processo di deposizione chimica da vapore.[11]
Tossicità / Indicazioni di sicurezza
SbH3 è un gas molto infiammabile e altamente tossico, ma è così instabile che è difficile trovarlo al di fuori dei laboratori. La stibina va utilizzata con grande cautela, con adeguati indumenti protettivi e maschera, lontano da fiamme libere e scintille. Può causare una grave reazione allergica respiratoria. Per contatto cutaneo o inalazione può provocare la morte. Sintomi di sovraesposizione includono mal di testa, debolezza, nausea, dolore addominale, dolore lombare, ittero, e irritazione dei polmoni. La stibina ha un'azione emolitica e danneggia il sangue, il fegato, i reni e il sistema nervoso centrale.[11]
Remove ads
Note
Bibliografia
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads










![{\displaystyle {\ce {SbH3 + HF + SbF5 -> [SbH4]+ [SbF6]-}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/6e09be1bc03d1e783f38ef8426c2545c324cb991)
