Loading AI tools
composto chimico Da Wikipedia, l'enciclopedia libera
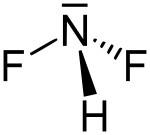
La difluoroammina è il composto inorganico con formula NHF2. Questo alogenuro di azoto in condizioni normali è un gas incolore fortemente reattivo. È un composto instabile che può esplodere facilmente.[2][4]
| Difluoroammina | |
|---|---|
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | F2HN |
| Aspetto | gas incolore |
| Numero CAS | |
| PubChem | 25242 |
| SMILES | N(F)F |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,424[1] |
| Temperatura di fusione | −116,4 °C (157 K)[2] |
| Temperatura di ebollizione | −23,6 °C (250 K)[2] |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | -67[2] |
| Indicazioni di sicurezza | |
| Frasi H | --[3] |
Una sostanza ritenuta difluoroammina fu descritta da Ruff e Staub nel 1931,[5] ma i tentativi successivi di riprodurre la sintesi fallirono, e le proprietà fisiche riportate da Ruff non sono in accordo con quelle attuali.[1] La difluoroammina fu sintetizzata e caratterizzata con certezza per la prima volta nel 1959 da Al Kennedy e Charles B. Colburn,[6] isolandola in piccola quantità come sottoprodotto dalla reazione a 250-300 ºC tra trifluoruro di azoto e arsenico.
La difluoroammina si può sintetizzare con una resa del 74% scaldando sotto vuoto una miscela di tetrafluoroidrazina e tiofenolo, con successiva distillazione sotto vuoto. La reazione complessiva risulta:[7]
Alternativamente si può fluorurare l'urea e idrolizzare il difluoruro di urea formato:[8]
La difluoroammina si decompone termicamente formando N2F2 in presenza di KF (che assorbe HF rilasciato):
La reazione a bassa temperatura con ClF produce clorodifluoroammina:
NHF2 è una base debole e può formare addotti reagendo a -80 ºC con acidi di Lewis come BF3, PF5 e SO2; aumentando la temperatura questi addotti si decompongono prima di arrivare a temperatura ambiente. Sotto i -80 ºC reagisce con AsF5 in HF anidro formando NH2F+2 e AsF−6.
La difluoroammina può reagire anche come acido:
se non ci sono basi disponibili, l'anione NF−2 reagisce formando N2F2:
In chimica organica la difluoroammina viene talvolta usata per ottenere difluoroammino derivati di composti organici.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.