Loading AI tools
Dihidroksilasi asimetris Sharpless (disebut juga dengan bishidroksilasi Sharpless) adalah reaksi kimia alkena dengan osmium tetroksida dengan keberadaan ligan khiral kuinina untuk membentuk suatu diol visinal.[1][2][3]
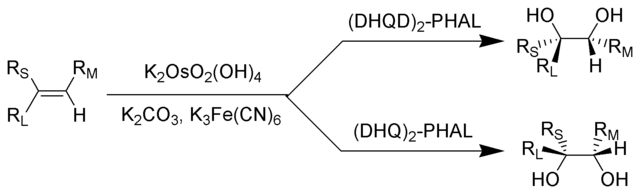
RL = Substituen terbesar; RM = Substituen sedang; RS = Substituen terkecil
Sudah menjadi praktik umum melakukan reaksi ini menggunakan sejumlah kecil osmium tetroksida sebagai katalis, yang setelah reaksi dapat diregenerasi menggunakan kalium ferisianida[4][5] atau N-metilmorfolina N-oksida.[6][7][8] Hal ini mengurangi secara drastis kebutuhan osmium tetraoksida yang sangat beracun dan sangat mahal. Keempat pereaksi ini tersedia secara komersial sebagai premiks ("AD-mix"). Campuran yang mengandung (DHQ)2-PHAL yang disebut Ad-mix-α, sedangkan campuran yang mengandung (DHQD)2-PHAL disebut AD-mix-β.[9]
Diol khiral semacam ini penting dalam sintesis organik. Introduksi khiralitas ke dalam pereaksi nonkhiral melalui penggunaan katalis khiral adalah konsep penting dalam sintesis organik. Reaksi ini pertama kali dikembangkan oleh K. Barry Sharpless berdasarkan rasemat dihidroksilasi Upjohn yang telah dikenal. Atas karyanya ini, Sharpless menerima anugerah Nobel Kimia pada tahun 2001.
Dihidroksilasi alkena menggunakan osmium tetroksida adalah metod lawas dan sangat berguna bagi fungsionalisasi olefin. Namun, karena osmium(VIII) mahal dan sangat beracun, maka perlu dikembangkan variasi katalitik untuk reaksi ini. Beberapa oksidan terminal stoikiometrik yang telah digunakan dalam reaksi katalitik ini antara lain kalium klorat, hidrogen peroksida (hidroksilasi Milas), NMO (dihidroksilasi Upjohn), tBHP (tert-butil hidroperoksida), dan kalium ferisianida. K. Barry Sharpless adalah yang pertama mengembangkan dihidroksilasi alkena enansioselektif yang berlaku umum dan handal, dirujuk sebagai Dihidroksilasi Asimetris Sharpless (Sharpless Asymmetric Dihydroksilasi, SAD). Reaksi ini masih melibatkan penggunaan sejumlah kecil OsO dengan oksidan stoikiometris (K), namun ini memanfaatkan ligan nitrogen khiral yang menciptakan lingkungan asimetris di sekitar oksidan.
Mekanisme reaksi dihidroksilasi Sharpless diawali dengan pembentukan kompleks osmium tetroksida – ligand (2). Suatu [3+2]-sikloadisi dengan alkena (3) menghasilkan intermediat siklik4.[10][11] Hidrolisis dalam suasana basa membebaskan diol (5) dan mereduksi osmat (6). Terakhir, oksidan stoikiometris meregenerasi kompleks osmium tetroksida – ligand (2).

Mekanisme Dihidroksilasi Asimetris Sharpless telah dipelajari mendalam dan potensi siklus katalitik sekunder telah berhasil diidentifikasi (lihat di bawah).[12][13] Jika intermediat ester osmilat dioksidasi sebelum terdisosiasi, maka akan terbentuk kompleks osmium(VIII)-diol yang kemudian dapat melakukan dihidroksilasi terhadap alkena lainnya.[14] Dihidroksilasi yang dihasilkan dari jalur sekunder ini biasanya lebih mengalami kesulitan selektivitas enansiomer daripada yang dihasilkan dari jalur primer. Skema di bawah menunjukkan jalur katalitik sekunder ini. Jalur sekunder ini dapat ditekan dengan menggunakan ligan dengan konsentrasi molar yang lebih tinggi.

Mekanisme tepat dari reaksi Dihidroksilasi Asimetris Sharpless pernah menjadi issue perdebatan sengit. SAD pertama kali dilaporkan oleh K. Barry Sharpless pada tahun 1980, dan dalam laporan awalnya Sharpless mengusulkan reaksi dilakukan melalui sikloadisi [2+2] OsO pada alkena untuk menghasilkan intermediat osmaoksetana (lihat di bawah).[15] Intermediat ini kemudian mengalami 1,1-insersi migratori membentuk ester osmilat yang setelah hidrolisis akan menghasilkan diol yang sesuai. Pada tahun 1989, E.J. Corey mempublikasikan varian reaksi ini yang sedikit berbeda dan mengusulkan bahwa reaksi lebih mungkin melalui sikloadisi [3+2] OsO dengan alkena untuk menghasilkan ester osmilat secara langsung.[16] Usulan Corey berdasarkan pada studi komputasional sebelumnya yang dilakukan oleh Jorgensen dan Hoffman yang menentukan jalur reaksi [3+2] adalah jalur dengan energi yang lebih rendah. Corey menambahkan alasan bahwa repulsi sterik pada intermediat oktahedral sebagai penghalang jalur [2+2]

Sepuluh tahun berikutnya muncul sejumlah publikasi, baik oleh Corey maupun Sharpless, yang masing-masing menunjang versi mekanisme yang merka yakini. Sementara studi-studi ini tidak mampu membedakan dua jalur siklisasi yang diusulkan, mereka sukses menunjukkan jalur mekanisme laini. Sebagai contoh, Sharpless memberikan bukti bahwa reaksi berlangsung melalui mekanisme bertahap.[17] Sebagai tambahan, baik Sharpless maupun Corey menunjukkan bahwa katalis aktif memapar kantung ikatan khiral berbentuk U.[18][19][20] Corey juga menunjukkan bahwa katalis mematuhi kinetika Michaelis-Menten dan bertindak selaku kantung enzim dengan suatu pra-kesetimbangan.[21] Pada Journal of the American Chemical Society terbitan Februari 1997, Sharpless mempublikasikan hasil studi (analisis Hammett) yang ia klaim lebih mendukung siklisasi [2+2] daripada [3+2].[22] Namun, pada terbitan Oktober 1997, Sharpless juga mempublikasikan hasil studi lainnya yang dilakukan bekerja sama dengan Ken Houk dan Singleton dengan kesimpulan yang mendukung mekanisme [3+2].[11] Oleh karena itu, Sharpless dipaksa untuk mengakui perdebatan yang berlangsung selama satu dekade.

Bukti kristalografi telah menunjukkan bahwa katalis aktif memapar spesies osmium pentakoordinat yang terikat pada kantung ikatan berbentuk U. Ligan nitrogen mengikat OsO dalam lingkungan khiral yang menjadikan pendekatan satu sisi olefin secara steris terhalang, sementara sisi lain tidak.[21]
Sejumlah sistem dan modifikasi katalitik telah dikembangkan untuk SAD. Berikut adalah selayang pandang beragam komponen sistem katalitik:
- Oksidan Katalitik: Ini selalu OsO, namun aditif tertentu dapat berkoordinasi dengan osmium(VIII) dan mengubah sifat elektroniknya. OsO sering dibuat in situ dari K (suatu spesies Os(VI)) karena pertimbangan keselamatan.
- Suplemen Khiral: Biasanya menggunakan alkaloid cinchona.
- Oksidan Stoikiometris:
- Peroksida merupakan oksidan stoikiometris pertama yang digunakan dalam siklus katalitik ini; lihat hidroksilasi Milas. Kerugian peroksida termasuk masalah selektivitas kimia.[14]
- Trialkilamonium N-oksida, misalnya NMO—seperti dalam reaksi Upjohn—dan trimetilamina N-oksida.[14]
- Kalium ferisianida (K) adalah oksidan stoikiometris yang umum digunakan untuk reaksi ini, dan merupakan oksidan yang terdapat di pasaran dalam bentuk preparat AD-mix.
- Aditif:
- Asam sitrat: Osmium tetroksida adalah suatu oksidan elektrofilik dan bereaksi lambat dengan olefin yang kekurangan elektron. Telah diketahui bahwa laju oksidasi olefin yang kekurangan elektron dapat diakselerasi dengan mempertahankan pH reaksi sedikit asam.[14] Di lain pihak, pH tinggi dapat meningkatkan laju oksidasi olefin internal, dan juga meningkatkan kelebihan enansiomer (enantiomeric excess (e.e.)) untuk oksidasi olefin terminal.[14]
Secara umum, dihidroksilasi asimetris Sharpless lebih menyukai oksidasi alkena yang lebih kaya elektron (skema 1).[23]

Pada contoh ini, SAD memberikan diol alkena terdekat kepada gugus para-metoksibenzoil (penarik elektron), meskipun dalam hasil rendah. Hal ini tampaknya disebabkan oleh kemampuan cincin aril untuk berinteraksi dengan titik aktif katalis via susunan π. Dengan cara ini, substituen aril dapat bertindak selaku gugus pengarah.[24]

Diastereoselektivitas SAD ditentukan terutama berdasarkan pemilihan ligan (yaitu, AD-mix-α vs AD-mix-β), namun, faktor-faktor seperti khiralitas yang sudah ada dalam substrat atau gugus fungsi tetangga dapat juga memainkan peranan. Dalam contoh di bawah, substituen para-metilbenzoil bertindak terutama sebagai sumber sterik besar demi memungkinkan katalis membedakan dua wajah alkena.[24]

Sering kali sulit untuk memperoleh diastereoselektivitas tinggi pada cis-alkena ketika kedua sisi olefin memiliki lingkungan sterik yang sama.
Dibandingkan dengan reaksi yang melibatkan osmium dalam jumlah stoikiometris, dihidroksilasi asimetris katalitik menurunkan ongkos prosedur sebesar 99,9%, membuka jalan untuk pengembangan biomimetik dan osmat simpatetik.
Dihidroksilasi asimeteris telah diterapkan untuk alkena pada setiap substitusi, dan enansioselektivitas yang tinggi telah dibuktikan untuk setiap pola substitusi. Reaksi dihidroksilasi asimetris juga selektif situs, menghasilkan produk-produk yang diturunkan dari reaksi ikatan rangkap kaya elektron dalam suatu substrat.[25]
- Oksidasi katalitik asimetris
- Hidroksilasi Milas
- Dihidroksilasi Upjohn
- Aminohidroksilasi Sharpless
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.