
Պարբերական աղյուսակի խումբ
From Wikipedia, the free encyclopedia
Քիմիական տարրերի պարբերական համակարգի խումբ, ատոմների հաջորդականություն՝ դասավորված միջուկի լիցքի աճման կարգով, որոնք օժտված են արտաքին շերտում միանման էլեկտրոնային կառուցվածքով։
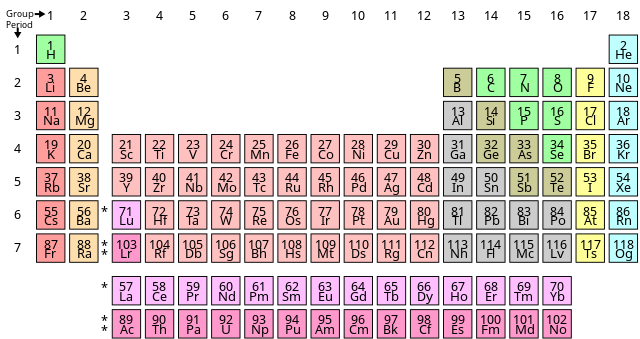
Խմբի համարը որոշվում է ատոմի արտաքին էլեկտրոնային շերտում էլեկտրոնների թվով (վալենտային էլեկտրոնները) և որպես կանոն, համապատասխանում է ատոմի առավելագույն վալենտականությանը։
Պարբերական համակարգի կարճ ձևում խմբերը դասակարգում են ենթախմբերի՝ գլխավոր (կամ Ա խմբեր), որոնց են պատկանում s և p տարրերը և երկրորդական (B ենթախումբ), որը ներառում է d-տարրերը։ Ենթախմբերը անվանում են նաև ամենափոքր միջուկի լիցք ունեցող տարրի անունով (որպես կանոն գլխավոր ենթախմբերի համար՝ երկրորդ պարբերության տարրերը, և երկրորդական ենթախմբի համար՝ չորրորդ պարբերության տարրերը)։ Միևնույն ենթախմբի տարրերը օժտված են նման հատկություններով։
Նույն խմբի տարրերի մոտ կարգաթվի աճմանը զուգընթաց աճում է էլեկտրոնային թաղանթների թիվը, մեծանում է ատոմային շառավիղը, ինչի հետևանքով էլեկտրաբացասականությունը թուլանում է, մետաղական հատկությունները ուժեղանում են, իսկ ոչ մետաղական հատկությունները՝ թուլանում։ Ուժեղանում են նրանց կողմից ձևավորվող նյութերի վերականգնիչ, և թուլանում օքսիդիչ հատկությունները։