
Ազոտական թթու
քիմիական միացություն / From Wikipedia, the free encyclopedia
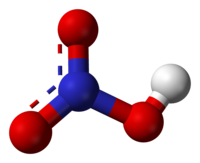
Ազոտական թթու, քիմիական բանաձևն է (HNO3), խոնավ օդում ծխացող նյութ է, ուժեղ միահիմն թթու և շատ ուժեղ օքսիդիչ, մանավանդ խիտ լուծույթներում հանդես է գալիս գլխավորապես որպես օքսիդիչ։ Խիտ ազոտական թթուն ունի երկու տարաձևություն՝ մոնոկլինային և ռոմբիկ բյուրեղացանցով։ Ջրի հետ խառնվում է ցանկացած հարաբերությամբ։ Ջրային միջավայրում համարյա ամբողջությամբ դիսոցվում է իոնների։ Ջրի հետ փոխազդում է 68,4% և 120 °C ջերմաստիճանային պայմաններում և մթնոլորտային ճնշման տակ։ Հայտնի են երկու բյուրեղահիդրատներ՝ մոնոհիդրատ (HNO3·H2O) և եռհիդրատ (HNO3·3H2O)։
Արագ փաստեր Ազոտական թթու, Քիմիական բանաձև ...
| Ազոտական թթու | |
|---|---|
 | |
 | |
 | |
| Քիմիական բանաձև | HNO₃ |
| Ֆիզիկական հատկություններ | |
| Ագրեգատային վիճակ | հեղուկ |
| Մոլային զանգված | 1,0E−25 կիլոգրամ[1] գ/մոլ |
| Մոլյար կոնցենտրացիա cM | 63.012 մոլ/լ |
| Խտություն | 1,5 ± 0,01 գ/սմ³[2] գ/սմ³ |
| Իոնիզացման էներգիա | 11,95 ± 0,01 Էլեկտրոն-վոլտ[2][3] կՋ/մոլ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | −44 ± 1 ℉[2] և −41,6 °C[3] °C |
| Եռման ջերմաստիճան | 181 ± 1 ℉[2] և 83 °C[3] °C |
| Գոյացան էնթալպիա | -174,1 կՋ/մոլ |
| Հալման էնթալպիա | 10,47 կՋ/մոլ կՋ/մոլ |
| Եռման էնթալպիա | 39,1 կՋ/մոլ կՋ/մոլ |
| Գոլորշու ճնշում | 48 ± 1 mm Hg[2] |
| Քիմիական հատկություններ | |
| Լուծելիությունը ջրում | խառնուրդ գ/100 մլ |
| pKa | −1,64 |
| Բեկման ցուցիչ | 1,397 |
| Դիպոլ մոմենտ | 7,2E−30 Կլ·մ[3] |
| Դասակարգում | |
| CAS համար | 7697-37-2, 12507-77-6 |
| PubChem | 944 |
| EINECS համար | 231-714-2 |
| SMILES | [N+](=O)(O)[O-] |
| ЕС | 231-714-2 |
| RTECS | QU5775000 |
| ChEBI | 919 |
| Թունավորություն | |
| ՄԲ50 | 430 |
| Թունավորություն |
  |
| IDLH | 64,5 ± 0,1 mg/m³[2] |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Փակել
