Klórossav
kémiai vegyület From Wikipedia, the free encyclopedia
A klórossav gyenge, szervetlen sav, képlete HClO2. A tiszta klórossav instabil, benne a klór oxidációs száma +3. Diszproporcióval hipoklórossavra és klórsavra bomlik (ezekben a klór oxidációs száma rendre +1, illetve +5):
- 2 HClO2 → HClO + HClO3
| klórossav | |||
 A klórossav szerkezeti képlete | |||
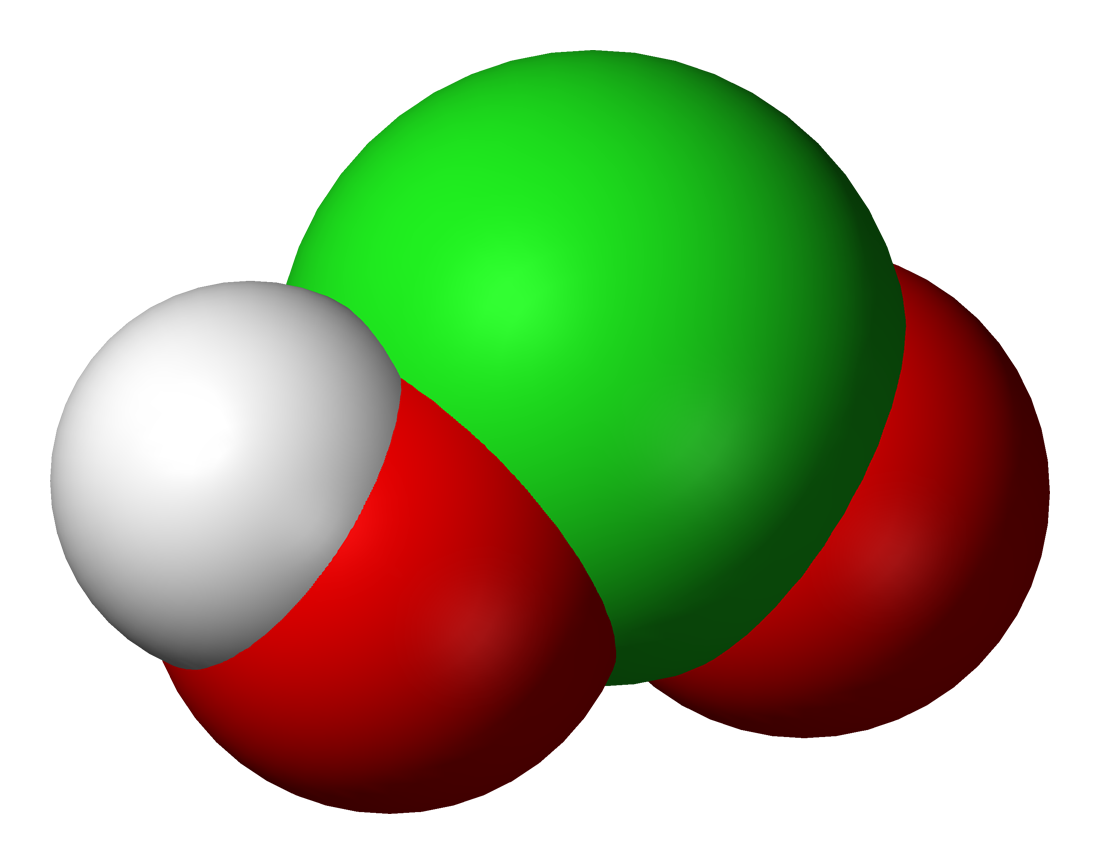
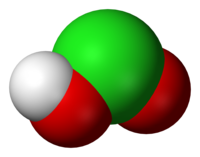 A klórossav kalottamodellje | |||
| IUPAC-név | klórossav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 13898-47-0 | ||
| PubChem | 24453 | ||
| ChemSpider | 22861 | ||
| KEGG | C01486 | ||
| ChEBI | 29219 | ||
| |||
| |||
| InChIKey | QBWCMBCROVPCKQ-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | HClO2 | ||
| Moláris tömeg | 68,46 g/mol | ||
| Savasság (pKa) | 1,96 | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Nehéz tisztán előállítani, de konjugált bázisa, a klorition ClO−2 stabil, egyik ismert sója a nátrium-klorit. A nátrium-kloritot és a hasonló sókat néha felhasználják klór-dioxid előállítására.
Előállítása
Előállítható bárium-klorit és hígított kénsav reakciójával:
- Ba(ClO2)2 + H2SO4 → BaSO4 + 2HClO2
Tulajdonságai
A klórossav erős oxidálószer, bár ezt a tulajdonságát némileg ellensúlyozza diszproporcióra való hajlama.
A klór az egyetlen halogén, mely HXO2 összegképletű izolálható savat alkot.[1] A fluor, mivel nem oxidálható, csak hipofluorossavat képez. A brómossavat és a jódossavat nem izolálták. A brómossav sói (a bromitok) ismertek, a jódossav sói (a joditok) azonban ismeretlenek.
Jegyzetek
Fordítás
Wikiwand - on
Seamless Wikipedia browsing. On steroids.