
Xenon-tetroxid
szervetlen vegyület / From Wikipedia, the free encyclopedia
A xenon-tetroxid az oxigén és a xenon kémiai vegyülete, képlete XeO4, és arról nevezetes, hogy a nemesgázokat tartalmazó vegyületek között stabilnak számít. Sárga, kristályos, szilárd anyag. −35,9 °C alatt stabil, fölötte robbanékony, xenonra és oxigénre (O2) esik szét.[3][4]
További információk Kémiai azonosítók, Kémiai és fizikai tulajdonságok ...
| Xenon-tetroxid | |
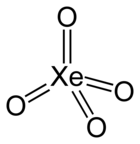 Xenon-tetroxid |  A xenon-tetroxid molekula térbeli szerkezetének a modellje |
| IUPAC-név | xenon-tetraoxid xenon(VIII)-oxid |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 12340-14-6 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | XeO4 |
| Moláris tömeg | 195,29 g mol−1 |
| Megjelenés | −36 °C alatt sárga színű, szilárd |
| Sűrűség | ? g cm−3, szilárd |
| Olvadáspont | −35,9 °C |
| Forráspont | 0 °C[1] |
| Kristályszerkezet | |
| Molekulaforma | tetraéderes[2] |
| Dipólusmomentum | 0 D |
| Termokémia | |
| Std. képződési entalpia ΔfH | ? kJ·mol−1 |
| Standard moláris entrópia S | ? J·K−1·mol−1 |
| Veszélyek | |
| EU osztályozás | Explozív (E) |
| Rokon vegyületek | |
| Rokon vegyületek | Perxenonsav Xenon-trioxid |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
Bezárás
A xenonnak mind a nyolc vegyértékelektronja részt vesz az oxigénnel alkotott kémiai kötésben. A xenon atom oxidációs száma +8. Az oxigén az egyetlen elem, mely a xenont a legmagasabb oxidációs állapotba tudja vinni, még a fluor is – valószínűleg sztérikus okok miatt – csak XeF6-ot képez.