
Xenon-tetrafluorid
szervetlen vegyület / From Wikipedia, the free encyclopedia
A xenon-tetrafluorid, képlete XeF4, a xenonból és a fluorból származtatott nemesgázvegyület. Ez volt az elsőként felfedezett vegyület, ami csak egy nemesgázt és egyetlen más kémiai elemet tartalmazott.[2]
| Xenon-tetrafluorid | |||
 XeF4 kristályok, 1962. | |||
 | 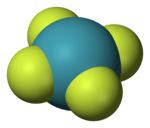 | ||
| IUPAC-név | xenon-tetrafluorid | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 13709-61-0 | ||
| PubChem | 123324 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | XeF4 | ||
| Moláris tömeg | 207,2836 g mol−1 | ||
| Megjelenés | fehér, szilárd | ||
| Sűrűség | 4,040 g cm−3, szilárd | ||
| Olvadáspont | 117 °C (390 K)[1] | ||
| Kristályszerkezet | |||
| Koordinációs geometria | D4h | ||
| Molekulaforma | síknégyzetes | ||
| Dipólusmomentum | 0 D | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH | −284 kJ/mol[1] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A molekula szerkezetét 1963-ban NMR spektroszkóppal és röntgensugaras kristályszerkezeti vizsgálattal határozták meg.[3][4] Ahogy azt a neutrondiffrakciós vizsgálatok kimutatták,[5] és a vegyértékelektronpár-taszítási elmélet is alátámasztotta, a molekula síknégyzetes elrendezésű. A molekula síkja felett és alatt két magányos elektronpár van.
A xenon-tetrafluorid színtelen kristályokat alkot, 115,7 °C-on szublimál.
A xenon-fluoridok szobahőmérsékleten exergonikusak és stabilak. A vízzel könnyen reakcióba lépnek, még a levegőből is kivonják a vizet, ezért vízmentes körülmények között kell tárolni őket.