
Hibridizáció
From Wikipedia, the free encyclopedia
A kémiában a hibridizáció a kémiai kötés leírására szolgáló egyik elmélet, a vegyértékkötés-elmélet módszere: az atompályák keverésével olyan új hibridpályákat hoz létre, melyek alkalmasak az atomok közötti kötés jellemzőinek leírására. A hibridpályák jól használhatók a molekulapályák alakjának magyarázására.

| Ez a szócikk a kémiai hibridizációról szól. Hasonló címmel lásd még: hibrid (egyértelműsítő lap). |
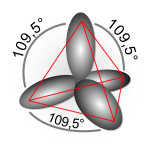
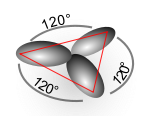
A hibridizáció elméletét Linus Pauling vezette be,[1] hogy megmagyarázza az olyan molekulák szerkezetét, mint például a metán (CH4). Ezt az eljárást eredetileg csak az ilyen egyszerű kémiai rendszerekre fejlesztették ki, de később szélesebb körben is alkalmazni kezdték, és ma a szerves vegyületek szerkezetének leírásában hatékony heurisztikának tekintik.
A hibridizációs elmélet kvantitatív számításokra nem annyira alkalmas, mint a molekulapálya-elmélet. Különösen a d pályák bevonása esetén – például a koordinációs kémia és a fémorganikus kémia területén – lépnek fel nehézségek. Bár a hibridizációs sémák használhatók az átmenetifémek kémiájában, ezek általában nem annyira pontosak.
Fontos megjegyezni, hogy a pályák az elektronok molekulán belüli viselkedésének leírására szolgáló modellek. Az egyszerű hibridizáció esetén ez a közelítés a hidrogén atompályáin alapul. A hibridpályákat ezen atompályák – különböző arányú – keverékének tekintjük. Az egyszerű hibridizációs sémák alapjául azért a hidrogén pályáit választjuk, mert ezek azon kevés pályák közé tartoznak, melyekre a Schrödinger-egyenletnek pontos analitikus megoldása van. A nehezebb atomok, például a szén, nitrogén és oxigén esetén feltételezzük, hogy ezek a pályák valamelyest torzulnak, de nem jelentős mértékben. A hibridizáció elmélete ilyen feltételek esetén használható a leghatékonyabban. Meg kell jegyezni, hogy a molekulák leírásához nincs szükség a hibridizációra, de a szénből, nitrogénből és oxigénből (valamint, bár kisebb mértékben, a kénből és foszforból) álló molekulák esetén a hibridizációs elmélet/modell sokkal egyszerűbbé teszi a leírást.
A hibridizációs elmélet fő felhasználási területe a szerves kémia, azon belül is leginkább a szén, nitrogén és oxigén (kisebb mértékben a foszfor és a kén) atomokra vonatkozóan alkalmazzák. A hibridizáció magyarázata a metán kötéseinek leírásával kezdődik.