
Koordinacijski broj
From Wikipedia, the free encyclopedia
Koordinacijski broj u kemiji označava broj čestica poredanih oko središnje čestice u kristalnoj rešetki, odnosno broj atomskih skupina ili iona oko središnjeg atoma kod kompleksnih spojeva.[1] Tako kod ionskih kristala koordinacijski broj označava broj iona suprotnog naboja koji se u ionskom kristalu nalaze oko središnjeg iona.[2]
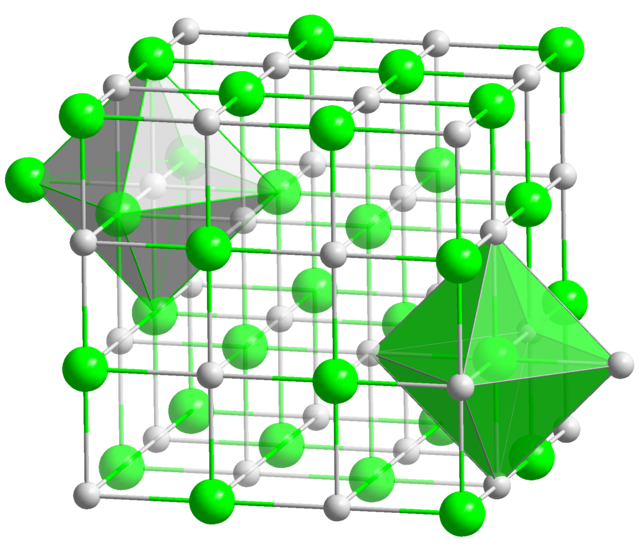
Među najčešćim koordinacijskim brojevima u prirodi javljaju se 4 i 6, a relativno često se javljaju i 2, 3, 8 (titan) i 12 (aluminij). Koordinacijski brojevi 2 i 6 karakteristični su za linearnu, odnosno oktaedarsku, a broj 4 za tetraedarsku i kvadratnu strukturu.[3] Metalni kationi visokog naboja (poput aluminijevog kationa) uglavnom imaju koordinacijski broj 6, ali u ovisnosti s temperaturom i djelovanjem katalizatora mogu promijeniti svoj koordinacijski broj na 4.[4] Koordinacijski broj u kristalima se uglavnom povećava povećanjem tlaka, npr. prelazom iz grafita (KB: 3) u dijamant (KB: 4), čime se mijenjaju svojstva samoga kristala; grafit je mekan, dok je dijamant jedna od najtvrđih tvari u prirodi.[5]