Loading AI tools
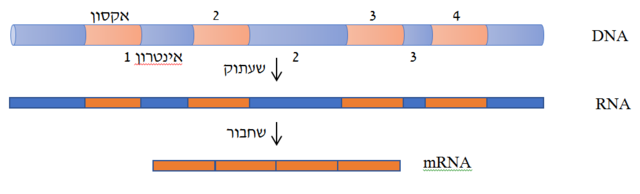
שחבור (באנגלית: Splicing) הוא מונח בגנטיקה מולקולארית, המתאר תהליך בתא אֵיקַרְיוֹטִי בו מולקולת RNA המתועתקת לפי רצף DNA עוברת עיבוד ליצירת RNA שליח (mRNA) המכיל את הרצף המתורגם לחלבון[1], או במקרה של RNA שאינו מקודד לחלבון (non-coding RNA) שעובר עיבוד עד ליצירת מולקולת ה־RNA הבשלה. בתהליך השחבור, מקטעים המכונים אינטרונים שאינם מקודדים לחלבון או ל־RNA פעיל, נחתכים ממולקולת ה־RNA המשועתקת בגרעין, כך שהרצפים המרכיבים את ה־RNA שליח, המכונים אקסונים, מחוברים לפי הסדר ליצירת רצף חומצות גרעין ב־RNA הבשל. האינטרונים נחתכים על ידי מכלול חלבוני הנקרא "ספלייסוזום"[2]. בגנים מסוימים, ישנם אינטרונים המקיימים שחבור עצמי[3].
תופעת השחבור מתקיימת בעיקר בכל ממלכת האיקריוטים, היות שגנים המקודדים בגרעין התא, במרבית המינים מאותה ממלכה, מכילים רצפי אינטרונים חסרי מסגרת קריאה (כלומר, שאינם מקודדים לחלבון) הנחתכים ממולקולת ה־RNA המשועתקת ואינם לוקחים חלק במולקולת ה־mRNA. בנוסף, ישנם גנים המתועתקים למולקולות RNA אשר אינן מתורגמות לחלבון אך עדיין עוברות שחבור[4]. ביצורים איקריוטים קדומים יותר, במיוחד חד-תאיים, תופעת השחבור אינה שכיחה, היות שתדירות האינטרונים המצויים בתוך רצפי גנים נמוכה[5]. עם העלייה במורכבות היצורים במהלך האבולוציה, עלתה גם שכיחות האינטרונים בכל גן[5].
הנוכחות של רצפים שנחתכים ממולקולת ה־mRNA מעלה את השאלה מניין אותם רצפים (לכאורה חסרי תכלית) הופיעו. אך ככל הנראה, מקור האינטרונים אינו יחיד, וישנן מספר אפשרויות שדרכן הם יכלו להופיע. להלן ארבעה מודלים אפשריים המנסים להסביר את מקור האינטרונים:
- טרנספוזיציה – אינטרון שהוסר ממולקולת mRNA של גן אחד עובר שחבור הופכי לתוך אתר חסר אינטרון של גן אחר או של אותו גן[6].
- טרנספוזונים – רצפים בגנום בעלי יכולת "לקפוץ" מאזור מסוים לאזור אחר בגנום. בהנחה שטרנספוזון ינחת ברצף של גן מסוים, ויעבור ברירה טבעית להיות מוסר במהלך תהליך השעתוק, הוא יתפתח ויהפוך לאינטרון של אותו גן[7].
- הכפלה – רצפי גנים מסוימים עשויים לעבור מוטציית הכפלה, כך שהרצף המקורי מוכפל לשני רצפים שזהים רצף המקורי, ועוקבים זה אחר זה. אם מתקיים רצף לא מקודד המפריד בין שני הגנים המשוכפלים, רצף זה יכול להיות מוסר בתהליך התיעתוק כאינטרון[7].
- שחלוף – רקומבינציה הומולוגית בין גנים בעלי דמיון רצפי ומקור אבולוציוני משותף המכונים פרלוגים. פרלוגים הם גנים שנבעו משכפול קדום של גן קדמון משותף ומתקיימים באותו גנום. שחלוף שגוי (בין רצפי DNA דומים ברצף, אך אינם בהכרח על גבי אותו הכרומוזום) בין פרלוג אחד למשנהו יכולה להוליך להוספת אינטרון מפרלוג ראשון בעל אינטרון, לפרלוג שני שלפני כן היה חסר אינטרון[8].
בין שנות ה־60 לשנות ה־70 של המאה ה־20 ניטש ויכוח בין חוקרי ביולוגיה מולקולרית של איקריוטים בנוגע ליצירת mRNA בתאי בעלי חיים. במחקרים אשר התקיימו בפרוקריוטים (חיידקים), לא נראה הבדל בין אורך הרצף המתורגם לחלבון לרצף הגן המשועתק ל־RNA מהגנום. לעומת זאת, ביצורים איקריוטים, נראה שמולקולת ה־RNA (נקראה: heterogenous nuclear RNA – hnRNA) המתועתקת בתוך הגן עוברת פירוק, ורק חלק קטן ממנה יוצא מהגרעין היכן היא מתפקדת כmRNA[9][10]. מולקולת ה־hnRNA המשועתקת מהגן האיקריוטי יותר ארוכה ממוקולת ה־mRNA שמתקיימת מחוץ לגרעין. בנוסף, נראה שרצפי הקצוות של ה־hnRNA נשמרים במולקולת ה־mRNA המתקיימת בגרעין[11]. אך לא ניתן היה להוכיח באמצעות שיטות סימון רדיואקטיביות, בהן השתמשו כדי לעקוב אחר מולקולות מתא, שמולקולות mRNA נובעת ממולקולות hnRNA.
נגיפי DNA ותרומתם להבנת מנגנון השחבור
מחקר בהבנת מנגנון התעתוק ובקרתו התקיים בעזרתם של הבקטריופאג'ים (נגיפים המדביקים חיידקים)[12]. בימים בהם לא הייתה אפשרות לשבט גנים בתאיים איקריוטים (סוף שנות ה־70 של המאה ה־20), לא ניתן היה לחקור ביטוי של גנים תאיים ספציפיים (למעט pre-mRNA). לכן, כפי שחקרו ביטוי גנים בחיידקים על ידי בקטריופאג'ים, כך גם ניסו חוקרים להשתמש בנגיפים אנימאליים, כגון נגיפי DNA, כדי לנסות להבין את מנגנוני הביטוי של גנים בתאים איקריוטים[13]. לנגיפי DNA מספר גנים מצומצם, ותבנית ה־DNA המקודדת לאותם גנים ניתנת לבידוד על ידי מיצוי של חלקיקים נגיפיים. נגיפי המודל שעבדו עימם היו הנגיף האנושי Adenovirus 2 (Ad2) והנגיף האנושי Adenovirus 5. היתרון בנגיפים אלו הוא שהגנום שלהם יחסית קטן (36 אלף בסיסים) וניתן היה לגדל אותם בקלות ולהפיק כמות רבה של DNA. יתרה מכך, מולקולות RNA שמקורן בווירוס Ad2 היו ארוכות בגרעין התא, התקיימו לזמן קצר, והכילו את הרצפים של ה־mRNA היציבים.
חוקרים ניסו למפות את הגנום של הנגיף על ידי התאמת מולקולות mRNA של גנים המקודדים למרכיבי הנגיף למולקולת ה־DNA הגנומי. השיטה עשתה שימוש בצילום באמצעות מיקרוסקופ אלקטרונים, בו ניתן לראות את האזור אליו מולקולת ה־mRNA סופחה למולקולת ה־DNA ליצירת "R-loop" חד־גדילי של DNA[13].
הנחת היסוד הייתה שהקצה ההתחלתי של מולקולת mRNA מייצג את אזור תחילת התיעתוק של גן מסוים, לכן ניתן למפות את גני הנגיף על ידי מעקב אחר מיקום הסיפוח של מולקולת ה־mRNA ל־DNA הגנומי. כך, על ידי מיפוי מולקולת mRNA של כל גן, ניתן יהיה למקם כל גן נפרד על גנום הנגיף. בניגוד להנחת היסוד, כל רצפי ה־mRNA, על אף שמקודדים לחלבונים שונים, היו בעלי רצף התחלתי זהה. בנוסף, הסיפוח של כל מולקולת mRNA הובילה ליצירת R-loop שונה. מחקרים אלו הובילו לגילוי של מנגנון עיבוד RNA מתועתק באיקריוטים, ואף אפשרות למנגנון היכול ליצור mRNA שונים מרצף pre-mRNA אחד (שחבור חליפי)[13].
כדי להבין את מנגנון השחבור, ראשית חשוב לדעת כיצד מובדלים האינטרונים מהאקסונים, כיצד האינטרונים נחתכים מה־pre-mRNA (mRNA לפני הסרת אינטרונים), וכן כיצד האקסונים מתחברים יחד ליצירת mRNA. התחימה בין רצפי האקסונים לרצפי האינטרונים מתקיימת ברמת רצף חומצות הגרעין של ה־pre-mRNA. את האינטרון, אם כן, תוחמים שני אתרים מוגדרים: תחום אקסון – אינטרון המגדיר את סוף האקסון ותחילת האינטרון, ותחום אינטרון־אקסון המגדיר סוף האינטרון ותחילת אקסון נוסף. אתרים אלו יגדירו את המיקומים בהם האינטרון יוסר מהרצף, ושני האקסונים יתחברו במהלך השחבור[14]. אתר נוסף הנוכח ברצף האינטרון שחשוב לתהליך החשבור הוא 'רצף ההסתעפות' (באנגלית branchpoint sequence)[15]. רצף זה מתקיים בתוך רצף האינטרון, קרוב יותר לתחום האינטרון־אקסון (או סוף האינטרון); לאחרי רצף ההסתעפות ישנו רצף של פירימידינים רבים (המורכב מהנוקלאוטידים T ו־C) הקרוי polypyrimidine tract[16].

טרנסאסטריפיקציה
טרנסאסטריפיקציה היא התגובה הכימית האחראית לניתוק האינטרון מה־pre-mRNA. במהלך השחבור מתקיימות שתי תגובות טרנסאסטרפיקציה עוקבות. בראשונה, קבוצת הידרוקסיל OH'2 של אדנין (A), שמורה ברצף ההסתעפות מתחברת לקבוצת זרחה של גואנין) (G) בגבול האקסון־אינטרון. כתוצאה מכך נוצר קשר פוספודיאסטרי בין הסוכר (ריבוז) של הנוקלאוטיד (A) לקבוצת הזרחה של הנוקלאוטיד G בגבול האקסון־אינטרון, כך שהקשר בין האקסון לאינטרון ניתק. הבתגובה השנייה, האקסון שנותק מהקשר עם האינטרון מכיל קבוצת הידרוקסיל OH'3 חשופה, שחופשית לבצע חיבור עם קבוצת זרחה בגבול אינטרון־אקסון. השלכות התגובה הן חיבור שני האקסונים שנפרדו על ידי האינטרון ושחרור האינטרון עצמו מה־pre-mRNA. האינטרון משוחרר כרצף דמוי לולאה הקרוי לאריאט[6].
לאריאט
הצורה בה אינטרון עוזב את ה־pre-mRNA. הלאריאט קרוי על שם האות היוונית סיגמא המייצגת את צורת האינטרון לאחר חיבור בין הקצה "אקסון־אינטרון" של האינטרון לרצף ההסתעפות, וחיבור בין קצה האקסון המשוחרר מתחילת האינטרון לאקסון המחובר לקצה "אינטרון־אקסון", מה שמשחרר את הלאריאט ומחבר בין שני האקסונים[17].
ספלייסוזום
ב־1985 נתגלה, שתהליך השחבור מתקיים בשמרים על ידי מבנה חלבוני קרוב בגודלו לריבוזום[18]. המכלול החלבוני מכיל חמש מולקולות RNA המקודדות בגרעין (small nuclear RNA – snRNA) שכל אחת מהן מתקיימת בהרכב עם חלבונים נוספים. השילוב בין מולקולות ה־RNA הקטנות לחלבונים נקרא גם small nuclear ribonuclear proteins (snRNP). הספלייסוזום מורכב מ־snRNP אך ההרכב משתנה כתלות בשלב השחבור הפעיל. ל־snRNP שונים יש תפקידים נפרדים בתהליך השחבור, בין זיהוי ה־pre-mRNA, הקרבת 'רצף ההסתעפות' לתחום האקסון־אינטרון וייעול התגובה היוצרת את הלריאט וחיבור בין שני האקסונים[19].
שחבור עצמי (Self Splicing)
בנוסף למנגנון השחבור של גנים גרעיניים באיקריוטים בו נעשה שימוש בספלייסוזום כדי להסיר אינטרונים לקבלת mRNA, ישנם מקרים בהם האינטרונים מוסרים באופן עצמאי (Self Splicing) ללא מכלול חלבוני המסייע לתהליך[20]. בשחבור עצמי, אינטרונים מסירים את עצמם מה־pre-mRNA על ידי ביצוע תגובות טרנסאסטריפיקציה דומות לתגובות המתבצעות על ידי הספלייסוזום. האינטרונים המבצעים שחבור עצמי מתחלקים לשתי קבוצות[21][20]:
- Group I introns: מתקיימים בגנים של RNA ריבוזומאלי (rRNA) או גנים של אברונים בתא. בקבוצת אינטרונים זו קיים נוקלאוטיד G נוסף ב'אתר ההסתעפות'. נוכחות הבסיס הנוסף, מאפשרת את ניתוק הקצה ההתחלתי של האינטרון מהאקסון ללא יצירת לריאט. קבוצת אינטרונים זו היא היחידה בה לא נוצר לריאט בתהליך השחבור.
- Group II introns: מתקיימים במספר גנים איקריוטים מעטים. מנגנון דומה למנגנון המתקיים באינטרונים המוסרים על ידי הספלייסוזום, בכל שנוצר לאריאט בסוף התהליך. האינטרונים בקבוצה זו יוצרים מתוך עצמם מבנה מרחבי המאפשר ביצועה תגובת הטרנסרסטרפיקציה.
RNA לא מקודד
מולקולות RNA ארוכות לא מקודדות (long non coding RNA – lncRNA) הן מולקולות RNA המשועתקות על ידי גנים אך אינן מתורגמות לחלבון. בהקשר לשחבור, התגלה שביטוי של lncRNA יכול להשפיע על אופן שחבור של גנים מסוימים[22]. שילוב של lncRNA במנגנון השחבור מראה על תופעות של בקרה יותר הדוקה על ביטוי של גנים מסוימים.
שחבור cis
תהליך זה מתאר את מנגנון השחבור הקלאסי, בו אקסונים מאותו גן מתחברים ליצירת mRNA. אומנם תהליך זה מתקיים ברוב האיקריוטים, אך אינו מהווה צורת שחבור אפשרית אחת.
שחבור trans
שחבור זה, המכונה גם שחבור בהצלבה, תהליך שבו תעתיקים שמקורם אינו מאותו אזור גנומי, או מאותו גן, יוצרים מולקולת mRNA[23]. כתוצאה מכך, מולקולת ה־mRNA מהווה איחוי (כימרה) בין שני תעתיקים נפרדים שמקורם מגנים שונים[23]. תופעה זאת התגלתה באאוקיוטים מסדרת הטריפנוזומטידות[24], ונצפתה גם בתולעים נימיות[25].
הסרת אינטרונים ממולקולת ה־pre-mRNA הוא תהליך הכרחי לביטוי תקין של רוב הגנים בגנום האנושי. תקינות תהליך השחבור תלויה במערך של גורמים, מרצף מולקות ה־RNA ועד למרכיבי הספלייסוזום, שפעילותם הכרחית כדי לאפשר שחבור נכון והנבת תוצר תקין. במולקולת ה־pre-mRNA, מוטציה באחד מאזורי קצוות האינטרון, או באזור ההסתעפות, יכולה להוביל לאי הסרת אינטרון ממולקולת ה־pre-mRNA ופגיעה בביטוי הגן. בנוסף לכך, מוטציה באחד מהגנים האחראיים למרכיבי הספלייסוזום עלולה להוביל להשבתה של תהליך השחבור ולפגוע בתהליך הטרנסאסטריפיקציה[26].
פרוגריה
פרגוריה, המכונה גם תסמונת פרוגריה (על שם) הטצ'ינסון־גילפורד (HGPS), היא מחלה בעלת דגם תורשה דומיננטי. חולים במחלה זאת סובלים ממגוון תופעות כגון גובה נמוך, משקל גוף נמוך, איבוד שיער מוקדם והזדקנות מוקדמת[27]. המחלה נובעת ממוטציה בגן LMNA, המקודד לחלבון גרעיני Lamin A אשר אחראי על מגוון תפקידים כגון עיגון חלבונים לממברנת הגרעין, שמירה על מבנה תקין של ממברנת הגרעין וקשירת כרומטין אליה. אחת המוטציות שגורמות למחלה מובילה לשינוי אתר השחבור בין אקסון 11 לאקסון 12 של הגן LMNA. שינוי בבסיס אחד בתוך אקסון 11 גורם ליצירת תעתיק אלטרנטיבי המחסיר 150 בסיסים מאקסון 11 ומוביל ליצירת חלבון לא תקין[28].
רטיניטיס פיגמנטוזה
רטיניטיס פיגמנטוזה היא מחלה בעלת דגם תורשה דומינטטי המאופיינת בפגיעה בראייה[29]. המוטציה נמצאת בגן PRPF6 המקודד לאחד מחלבוני הספלייסוזום. המוטציה גורמת לשינוי בחומצה אמינית שמורה בחלבון, והובלה לא רגילה של החלבון בתוך גרעין התא. בנוסף, המוטציה פוגעת בהרכבת הספלייסוזום וכך פוגעת בתיעתוק תקין של גנים[30].
ניוון שרירים שדרתי
ניוון שרירים שדרתי הוא מחלה ניוונית בעלת דגם תורשה רצסיבי המשפיעה על מבנה ופעילות שרירים רצוניים. המחלה גורמת לאי תקינות של פעילות עצבים מוטוריים בחוט השדרה, ונובעת מפגיעה בגן SMN[31] אשר מקודד לחלבונים המסייעים ביצירת snRNP[32]. פגם בגן זה פוגע בפעילות מנגנון השחבור בכללו.
טרשת אמיוטרופית צידית
טרשת אמיוטרופית צידית מאופיינת בניוון של עצבים מוטוריים ועם זאת ניוון שרירים רצוניים[33]. המחלה יכולה להיות מורשת, או ספוראדית (ללא רקע משפחתי) וקשורה למספר גנים שמוטציה בהם יכולה להוביל לפנוטיפ המחלה[33]. אחת האפשרויות היא מוטציה בגן FUS המקודד לחלבון קושר RNA. חלבון זה לנקשר ל־snRNP ולגן SMN. מוטציה בגן FUS פוגמת באינטראקציה עם snRNP ואילו האינטראקציה עם SMN דווקא מתחזקת. זה גורם לשיבוש מנגנון השחבור ופגיעה בביטוי גנים רבים[34].
- דר' אדריאן ישראלסון, דר' סלח אבו חמאד, מחלת ALS – ניוון שרירים, מכון דוידסון, 15.09.2014
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.