
Ácido oxálico
composto químico / From Wikipedia, the free encyclopedia
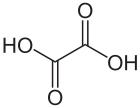
O ácido oxálico é un composto orgánico coa fórmula C2H2O4. É un sólido branco cristalino que forma unha solución incolora en auga. A súa fórmula condensada é HOOCCOOH, que indica a súa clasificación como o ácido dicarboxilico máis simple.
| Ácido oxálico | |
|---|---|
 | |
 |
 |
 | |
ácido etanodioico[1] | |
Outros nomes PIN: Ácido oxálico[1] | |
| Identificadores | |
| Número CAS | 144-62-7 (anhidro), 6153-56-6 (dihidrato) |
| PubChem | 971 |
| ChemSpider | 946 |
| UNII | 9E7R5L6H31 |
| Número CE | 205-634-3 |
| Número UN | 3261 |
| DrugBank | DB03902 |
| KEGG | C00209 |
| MeSH | Oxalic+acid |
| ChEBI | CHEBI:16995 |
| ChEMBL | CHEMBL146755 |
| Número RTECS | RO2450000 |
| Referencia Beilstein | 385686 |
| Referencia Gmelin | 2208 |
| 3DMet | B00059 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C2H2O4 |
| Masa molar | 90,03 g mol−1 (anhidro) 126,065 g·mol−1 (dihidrato) |
| Aspecto | cristais brancos |
| Olor | inodoro |
| Densidade | 1,90 g·cm−3 (anhidro, a 17 °C)[2] 1,653 g·cm−3 (dihidrato) |
| Punto de fusión | 189–191 °C; 372–376 °F; 462–464 K |
| Solubilidade en auga | 90-100 g/L (20 °C)[2] |
| Solubilidade | 237 g/L (15 °C) en etanol 14 g/L (15 °C) en dietil éter [3] |
| Presión de vapor | <0.001 mmHg (20 °C)[4] |
| Acidez (pKa) | 1,25, 4,14[5] |
Susceptibilidade magnética (χ) |
-60,05·10−6 cm3/mol |
| Perigosidade | |
| Principais perigos | corrosivo |
| NFPA 704 | |
| Punto de inflamabilidade | 166 °C; 331 °F; 439 K |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
A súa forza como ácido é moita maior que a do ácido acético. O ácido oxálico é un axente redutor[6] e a súa base conxugada, denominada oxalato (C
2O2−
4), é un axente quelante para catións metálicos. Normalmente, o ácido oxálico encóntrase en forma de dihirato coa fórmula C2H2O4·2H2O.
Aparece de forma natural en moitos alimentos, pero a súa inxestión excesiva ou o seu prolongado contacto coa pel poden ser perigosos.
O seu nome procede de que foi illado das plantas do xénero Oxalis.
