La transplantation de moelle osseuse est une greffe consistant à transférer de la moelle osseuse d'un individu à un autre souffrant d'une pathologie de sa moelle. Elle est parfois la seule voie de guérison.
Elle permet l'utilisation de chimiothérapie et/ou de radiothérapie à des doses massives, ce qui a pour résultat d'améliorer la survie, voire d'envisager la guérison dans certains cas et de profiter de l'effet greffe contre tumeur (par les lymphocytes T du donneur). Ces traitements sont en effet très toxiques pour les cellules sanguines et la greffe permet la reconstruction et la régénération de la moelle osseuse et le maintien d'une production normale de ces cellules.
Cette transplantation, comme celle du rein ou du sang, est rendue possible par un donneur vivant qui offre son organe dans la plupart des cas. Dans certains pays, le donneur reçoit une rétribution ; ceci est illégal en France en raison du principe de non-patrimonialité du corps humain[1].
On distingue deux types de greffes :
- l'allogreffe de moelle osseuse, qui utilise un greffon médullaire provenant d'un donneur sain qui doit être HLA identique au receveur.
- l'autogreffe de moelle osseuse, qui utilise la propre moelle du patient.
Historique
Les premières expérimentations animales ont eu lieu au début des années 1950.
Les premières transplantations de moelle ont été faites chez l'être humain en 1957 par E. Donnall Thomas à New-York, aboutissant au décès des six receveurs en moins de trois mois[2]. Elles ont été faites à une époque où la notion d'histocompatibilité n'existait pas.
Les toutes premières greffes de moelles osseuses réussies ont été réalisées en 1958 par Georges Mathé, alors assistant de Jean Bernard à l'hôpital Saint-Louis à Paris, sur cinq physiciens yougoslaves irradiés accidentellement dans un réacteur nucléaire[3],[4]. Quatre ont survécu à la greffe. En 1963, Georges Mathé greffa avec succès un patient leucémique après irradiation totale[5]. Le patient resta en rémission complète pendant plus de dix huit mois avant de décéder d'une encéphalite[6].
Les premiers succès prolongés datent des années 1970[7] Les premières greffes HLA identiques ont été réalisées pour des enfants atteints de déficits immunitaires sévères par Robert Good à Minnéapolis aux Etats Unis en 1958 et Claude Griscelli en 1971 à l'hôpital Necker (Nouv presse Med , Mai 1973 jan1:2n220-7 et Clin .exp immunol1974 jun17:2 245-52).
La première description de réussite en cas de donneur non apparenté est faite peu après.
Dans les années 1980, Éliane Gluckman se voit confier par Jean Bernard la responsabilité du service de greffe de moelle à l'hôpital Saint-Louis. Elle est à l'origine de la première greffe de sang de cordon sur un enfant américain souffrant de la maladie de Fanconi (aplasie médullaire d'origine autosomique récessive).
En 1990, E. Donnall Thomas a reçu le Prix Nobel de médecine pour ses avancées dans le domaine.
Moelle osseuse
Fonctionnement
La moelle osseuse est un tissu qui se trouve à l'intérieur de tous les grands os (tibia, bassin, etc. ) et n'a rien à voir avec la moelle épinière. En fait, il y a deux types de moelles, la moelle blanche située dans la diaphyse des os longs (fémur, tibia, humérus…), et la moelle rouge hématopoïétique, située dans les os courts (cuboïde, astragale, scaphoïde…) ou plats (os iliaque, omoplate, sternum…) et dans l'épiphyse des os longs (tête du fémur, plateau tibial, malléoles…) où sont fabriqués les éléments figurés du sang. Cette dernière constitue le système hématopoïétique : elle produit les globules rouges, les globules blancs et les plaquettes.
Maladies
La question de la transplantation se pose lorsque les cellules de la moelle osseuse d'un patient ne remplissent plus leur fonction. Différentes hémopathies (maladies du sang) peuvent être causées par le dysfonctionnement de la moelle osseuse :
- L'aplasie médullaire est une maladie qui se caractérise par l'arrêt du fonctionnement de la moelle et qui touche principalement les enfants.
- Lors d'une leucémie (cancer du sang), la moelle continue de fonctionner, mais les cellules produites ne sont pas opérationnelles.
- Les enfants-bulle souffrent d'une déficience de leur système immunitaire, le plus souvent dès leur naissance.
- Lors d'un lymphome, le cancer frappe la production des globules blancs.
Le déficit de chacun des types de cellules produites par la moelle peut provoquer des troubles différents :
- celui en globules rouges conduit à des anémies,
- celui en globules blancs conduit à une neutropénie, c'est-à-dire à une faiblesse dans les défenses immunitaires et à des infections,
- et celui en plaquettes à une thrombopénie, donc à un risque accru de saignement, voire à des problèmes hémorragiques
Dans certaines de ces maladies, une transplantation de moelle osseuse peut être envisagée pour parvenir à la guérison. La transplantation n'est cependant pas nécessairement le traitement principal de toutes ces maladies. Ainsi, dans le cas de la leucémie myéloïde chronique, de nouveaux traitements ont été mis au point.
Problèmes de compatibilité
Si le traitement par une transplantation de moelle osseuse est choisi, il faut trouver un donneur compatible avec le malade.
Comme pour toutes les allogreffes, la compatibilité entre le donneur et le receveur est un problème important à résoudre : afin d'augmenter au maximum les chances de succès de la greffe, il faut que la compatibilité HLA (ou histocompatibilité) entre le donneur et le receveur soit la plus élevée possible.
Compatibilité HLA
Le système HLA est le système qui permet au corps et à son système immunitaire de reconnaître le soi (ensemble des tissus, etc.) du non-soi (virus, bactéries et… greffes). Chaque être humain possède un code HLA qui lui est propre et qui se trouve à la surface de ses cellules. Ainsi, tout corps étranger ou cellule qui ne présente pas les « bons » marqueurs HLA à sa surface se fait attaquer par le système immunitaire.
Le code HLA d'un individu est déterminé par les différents allèles qui représentent les 6 gènes (A, B, C, DR, DQ et DP) gouvernant l'histocompatibilité. Ces gènes sont tous présents sur le chromosome no 6 et comptent de nombreux allèles :
| Gène | Nombre d'allèles recensés |
| A | 268 |
| B | 517 |
| C | 129 |
| DR | 333 |
| DQ | 53 |
| DP | 109 |
Le grand nombre d'allèles pour chacun des gènes conduit à un nombre encore bien plus grand de combinaisons possibles qui sont autant de codes HLA. On estime que 10 à 30 % de personnes vivantes possèdent un code HLA qui leur est entièrement propre et qu'aucun autre être humain dans le monde ne partage.
Malgré cette difficulté, les codes HLA du donneur et du receveur doivent être les plus proches possible afin de permettre aux cellules du donneur de prendre place dans le corps du receveur sans pour autant déclencher une réaction de rejet. Dans le cadre de la transplantation de moelle osseuse, le système immunitaire du receveur est très affaibli ou inexistant. Ce n'est pas lui qui va être à l'origine de la réaction de rejet. Ce sont les cellules greffées du donneur, qui devront produire le nouveau système immunitaire du malade, qui vont attaquer les tissus du receveur, perçus comme hostiles, comme du non-soi. Il s'agit de la maladie du greffon contre l'hôte (GvH disease, Graft versus Host disease).
Trouver un donneur compatible
À la recherche d'un donneur, le médecin va d'abord se tourner vers les différents membres de la fratrie (frères et sœurs) du malade pour trouver les mêmes marqueurs HLA. Les vrais jumeaux sont souvent les plus compatibles entre eux.
En effet, il existe une chance sur 4 pour que deux membres d'une fratrie possèdent le même code HLA : un enfant reçoit un chromosome no 6 de son père et un autre de sa mère, qui en possèdent également chacun deux exemplaires. L'enfant va donc hériter d'une des quatre combinaisons de chromosomes possibles :
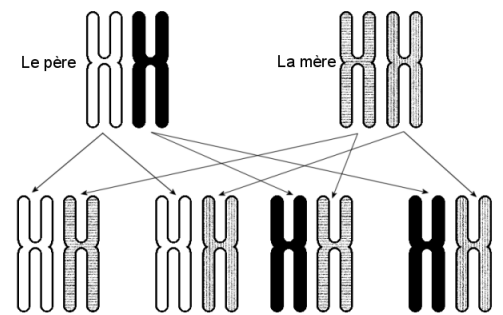
Si cependant aucun des membres de la fratrie ne possède le même code HLA que le malade, le médecin va chercher dans le fichier mondial de donneurs qui recense 31 millions de volontaires avec leurs informations HLA[8].
Si cette recherche échoue car aucun des volontaires enregistrés n'est compatible, il reste alors la solution du sang de cordon (voir ci-après) ou d'une greffe à partir d'un membre de la famille avec une histocompatibilité imparfaite, dite haplo-identique.
Déroulement du don

Une fois qu'un donneur compatible avec le malade a été trouvé, le processus de la transplantation peut commencer. Il consiste à transférer un certain nombre de cellules constituant la moelle osseuse (les cellules souches hématopoïétiques, ou CSH) vers le malade. Ces cellules iront reconstituer l'ensemble de la moelle osseuse chez le receveur après la greffe.
Don
Il existe plusieurs formes de dons :
- le prélèvement par voie intra-osseuse,
- la cytaphérèse,
- le prélèvement de sang de cordon.
Les cellules prélevées peuvent être greffées pendant 24 heures. Cela permet de les transporter sur de grandes distances. Si cependant des problèmes de logistique venaient à se poser, ce serait le donneur qui se rapprocherait du malade, trop fragile pour se déplacer. La congélation est aussi aujourd'hui pratiquée, assurant plus de souplesse aux conditions de transfert[9].
Prélèvement par voie intra-osseuse
Ce prélèvement se fait sous anesthésie générale et nécessite l'hospitalisation du donneur pour une durée de deux jours. L'intervention en elle-même dure une à deux heures. Elle consiste à prélever par des ponctions dans les os du bassin une quantité de moelle osseuse calculée en fonction du poids du donneur. Ce prélèvement permet de recueillir à la fois les cellules souches hématopoïétiques et le tissu cellulaire qui les entoure.
Une poche de sang du donneur peut parfois être prélevée avant l'intervention. Elle lui est restituée au décours pour favoriser sa récupération.
Cytaphérèse
Cette technique permet de prélever des cellules souches périphériques par centrifugation du sang du donneur. Les constituants du sang non prélevés sont rendus au donneur. La quantité de cellules souches hématopoïétiques prélevée est supérieure par rapport à la voie intra-osseuse. Quelques jours avant le prélèvement, la moelle osseuse du donneur est stimulée par injection sous-cutanée d'un médicament analogue au G-CSF (Granulocyte Colony Stimulating Factor), tel que les molécules filgrastim ou lenograstim, qui entraîne le passage des cellules souches hématopoïétiques de la moelle osseuse vers le sang. Le prélèvement se fait en une ou deux fois de 3 à 4 heures, sans hospitalisation.
Le choix entre aphérèse ou voie intra-osseuse est fait par le médecin en tenant compte de plusieurs critères liés à la fois au receveur et au donneur.
Prélèvement de sang de cordon
Du sang aux vertus thérapeutiques peut également être prélevé après la naissance d'un enfant[10]. Il s'agit du sang prélevé sur le placenta (et non sur le nouveau-né) à partir du cordon. Le sang placentaire contient également des CSH. Ceux-ci ont l'avantage d'être jeunes et immatures et cela permet de réduire les risques de rejet immunologique et de réaction du greffon contre l'hôte. Un don même vers un malade avec lequel la compatibilité HLA n'est pas parfaite est alors possible.
Ce sang est souvent destiné à des enfants, car la quantité limitée de cellules-souches s'y trouvant ne permet pas toujours de soigner un malade de plus de 50 kg. Certains travaux montrent qu'il est possible d'associer deux sangs de cordons (proches d'un point de vue de leur HLA) afin de soigner les adultes.
Greffe
Avant de recevoir la greffe, le malade est préparé : sa moelle, malade, est complètement détruite. Pour cela, il va recevoir une chimiothérapie, dite « de conditionnement » pendant une dizaine de jours. L'hospitalisation se fait dans une chambre stérile car la chimiothérapie aura mis le patient en aplasie profonde en détruisant son système immunitaire.
La greffe effective est réalisée au moyen d'une perfusion de moelle préparée pour le malade.
Les cellules greffées vont alors prendre place dans les os pour progressivement reconstituer tout le tissu de la moelle osseuse et reprendre la production des différentes cellules sanguines. Celle-ci n'est effective que 10 à 30 jours après la greffe, période pendant laquelle il faut continuer de protéger le malade des agents infectieux. Au bout de trois mois, les défenses immunitaires peuvent être reconstituées. Ce scénario peut cependant s'assombrir si une réaction de rejet se produit, si la maladie du greffon contre l'hôte se déclare (voir plus bas). Dans certains cas, par exemple de lymphome, une maladie du greffon contre l'hôte modérée est un facteur déterminant de guérison car le greffon, une fois développé, attaque les cellules cancéreuses.
Complications
Réaction du greffon contre l'hôte
La « maladie du greffon contre l'hôte » (graft-versus-host disease, GVHD ou GVH) est une complication fréquente et grave des greffes de moelle osseuse allogénique[11]. Elle est provoquée par les cellules immunocompétentes de la moelle osseuse du donneur qui vont attaquer l'organisme du receveur, incapable de les rejeter du fait de l'immunodépression induite avant la greffe (conditionnement du receveur par suppression de sa moelle et de sa mémoire immunitaire). Certains organes constituent la cible privilégiée de la GVH aiguë : peau, tube digestif et canalicules biliaires, mais également les poumons. Par définition, la GVH est dite aiguë quand elle survient avant le centième jour post-greffe, et chronique au-delà. Les poussées de GVH chronique n'ont pas nécessairement de caractère récurrent et régulier, contrairement au sens premier et trompeur du terme employé pour la qualifier. Elles surviennent plutôt de façon sporadique et imprévisible. Une GVH chronique peut apparaître sans qu'il y ait eu précédemment une GVH aiguë.
Afin de limiter, voire de supprimer totalement tout risque de rejet, les médecins utilisent des médicaments : les immunosuppresseurs. Leur but est de diminuer la réponse immunitaire de l'organisme en limitant le taux d'anticorps créés par les lymphocytes B et le nombre de lymphocytes T2. On citera comme immunosuppresseur les corticostéroïdes, les inhibiteurs de synthèse d'ADN et les sérums monoclonaux. Cependant, l'activité des immunosuppresseurs, bien quelle soit bénéfique pour le malade, entraîne une faiblesse du patient envers les attaques des maladies, et leurs effets secondaires ne sont pas négligeables. C'est pourquoi tous les patients mis sous immunosuppresseur ont un suivi médical très régulier.
Devenir donneur
Étant donné les contraintes de compatibilité, la stratégie du don de la moelle osseuse est différente de celle du don du sang. Cependant celle-ci évolue: il n'était en effet pas question de stocker des dons dans des banques en attendant un besoin éventuel, mais la congélation associée à des méthodes de purification est aujourd'hui pratiquée[9].
Les personnes volontaires au don de moelle osseuse sont recensées dans un registre national, dans lequel leur typage HLA est indiqué. Celui-ci est réalisé à partir d'une simple prise de sang. Le don de moelle, lui, ne sera effectué que si un malade compatible en a effectivement besoin et qu'il n'a pas trouvé dans sa famille un frère ou une sœur compatible. En France, le registre des donneurs volontaires est tenu par l'Agence de la biomédecine[12].
Entre l'inscription sur le fichier et le don effectif, un laps de temps très variable peut s'écouler (de quelques mois à de nombreuses années). Il est également possible que le don n'ait jamais lieu si aucun malade n'est jamais compatible.
Lors du don, les deux grands principes suivants sont appliqués :
- l'anonymat : le donneur et le receveur ne se rencontreront jamais et l'identité de l'un ne sera pas communiquée à l'autre
- la gratuité : le donneur ne sera pas rémunéré pour son geste. Par contre, tous les frais d'hospitalisation seront pris en charge.
Inscription
Pour se porter volontaire, il faut remplir cinq conditions :
- être majeur,
- être en bonne santé,
- avoir un Indice de Masse Corporelle inférieur à 30,
- avoir moins de 35 ans lors de l'inscription (le don, lui, étant possible jusqu'à 60 ans), 1
- accepter un entretien médical sur ses antécédents médicaux et sur son mode de vie.
C'est lors de l'entretien médical qu'a lieu un prélèvement salivaire ou une prise de sang servant à déterminer le typage HLA et à dépister certaines maladies. Cette analyse peut être partielle et une autre prise de sang peut avoir lieu si un début de compatibilité avec un malade se présente.
Lors de l'inscription, le nouveau code HLA est comparé à tous ceux des malades répertoriés.
Les pré-inscriptions se font en ligne sur le site dondemoelleosseuse.fr.
Situation en France
Le registre France Greffe de Moelle est accrédité par la World Marrow Donor Association (WMDA) qui regroupe 73 registres dans 52 pays, ce qui représente en avril 2021 38.7 millions de donneurs potentiels dans le monde[13],[14]. Le registre France Greffe de Moelle (FGM) est géré par l’Agence de la biomédecine[15]. À la fin de 2019, il y a 311 555 donneurs inscrits sur le fichier français[13],[16]. Il y a eu en 2014 1 943 allogreffes de cellules souches hématopoïétiques (CSH) et 927 greffes non apparentées avec donneurs volontaires dont 187 avec des unités de sang placentaire[17]. En 2016 il y a 205 donneurs du registre français qui ont effectivement donné leur moelle. Parmi ces dons, 75 % se font par aphérèse et 25 % par prélèvement intra-osseux[13]. La compatibilité entre un malade et un donneur en dehors de la famille est en moyenne d'1 sur 1 million, elle est de 1 cas sur 4 entre frères et sœurs d'une même famille[18].
Le don de moelle était comme le don de sang et celui d'organes, la « Grande cause nationale 2009 » en France. Une semaine nationale annuelle lui est consacrée. Depuis 2012, les donneurs potentiels inscrits au fichier se rassemblent en communauté et se nomment « les veilleurs de vie ».
Notes et références
Voir aussi
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.