Dichloroisocyanurate de sodium
composé chimique De Wikipédia, l'encyclopédie libre
Le dichloroisocyanurate de sodium (ou DCCNa, également troclosene sodique selon la Dénomination commune internationale) est une source stable de chlore libre.
Il est utilisé comme désinfectant, biocide antibactérien[8], anti-algue et désodorisant industriel. Ce composé hétérocyclique dérive de la triazine et est produit par action du chlore sur l'acide cyanurique.
| Dichloroisocyanurate de sodium | |
| |
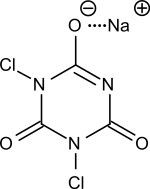
| Structure chimique du dichloroisocyanurate de sodium | |
| Identification | |
|---|---|
| Nom UICPA | sodium 3,5-dichloro-2,4,6- trioxo-1,3,5-triazinan-1-ide |
| No CAS | |
| No ECHA | 100.018.880 |
| No CE | 220-767-7 |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | poudre cristalline blanche, d'odeur âcre[1]. |
| Propriétés chimiques | |
| Formule | C3Cl2N3NaO3 [Isomères] |
| Masse molaire[2] | 219,946 ± 0,008 g/mol C 16,38 %, Cl 32,24 %, N 19,1 %, Na 10,45 %, O 21,82 %, |
| Propriétés physiques | |
| T° fusion | Se décompose au-dessous du point de fusion à 230 °C[1] |
| Solubilité | dans l'eau : 250 g·L-1[1] |
| Masse volumique | >1 |
| Pression de vapeur saturante | <0,000 05 mmHg |
| Précautions | |
| SGH[3] | |
| H272, H302, H319, H335, H410 et EUH031 |
|
| SIMDUT[4] | |
  C, D1B, D2B, |
|
| NFPA 704 | |
| Transport | |
| Inhalation | Toux. Mal de gorge[6], œdème pulmonaire lésionnel[7]. |
| Peau | Rougeur. Brûlures cutanées. Douleur[6]. |
| Yeux | Rougeur. Douleur. Perte de la vue. Brûlures profondes graves[6]. |
| Ingestion | Sensation de brûlure. Mal de gorge[6]. |
| Écotoxicologie | |
| CL50 | 0.27 à 1,17 mg·L-1 (rats) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier | |
C'est un sel de sodium de l'acide dichloroisocyanurique, soluble dans l'eau. Il réagit avec l'eau, l'urée, l'ammoniac, les agents réducteurs et les bases fortes.
De couleur blanche, il est proposé en granules, poudre ou pastilles, pour des usages professionnels ou pour le grand public.
Il constitue le chlore choc utilisé comme biocide pour la désinfection de l'eau des piscines. (Le chlore lent correspond à l'acide trichloroisocyanurique). Il est également utilisé, sous l’appellation de "javel en pastille" ou "pastille javel", comme substitut solide de l'eau de javel (solution aqueuse d'hypochlorite de sodium, NaClO, dont le principe actif est l'ion hypochlorite ClO−, faible biocide et fort oxydant), car dans l'eau, sa décomposition produit également l'ion hypochlorite, en deux temps :
- il se décompose d'abord en acide hypochloreux HOCl et cyanurate de sodium
- C3Cl2N3O3Na + 2·H2O → C3H2N3O3Na + 2HOCl
- l'acide hypochloreux, acide faible avec une constante d'acidité de 7,5, est en équilibre avec l'ion hypochlorite (l'équilibre dépendant du pH, il est déplacé vers la droite lorsque le pH est supérieur à 7,5 et vers la gauche lorsqu'il est inférieur. Lorsque l'effet biocide est recherché il faut privilégier un pH de l'ordre de 7,4 (7,2-7,5) favorable à la formation de l'acide hypochloreux, qui est plus puissant que l'ion hypochorite. Par exemple, avec un pH de 8,2, il faudrait 2 mg·L-1 pour avoir le même effet bactéricide que 0,7 mg·L-1 à pH = 7,4[9].)
- HOCl ClO− + H+
Le cyanurate joue un rôle de stabilisant (se décomposant à son tour en partie en acide cyanurique (CNOH)3 ) en protégeant l'acide hypochloreux HOCl et l'ion hypochlorite ClO− d'une décomposition par les ultraviolets.
La décomposition n'a pas d'effet significatif sur le pH de l'eau.
Les mêmes précautions que pour l'eau de javel sont à prendre : l'action d'un acide va libérer du chlore, potentiellement toxique en fonction des quantités, selon la réaction

Sécurité
Ce produit est toxique par ingestion ou par inhalation des gaz qu'il produit[7] et donc à maintenir hors de portée des enfants[7]. Il doit être impérativement stocké dans des locaux bien ventilés, dans des contenants hermétiques, à l'abri de l'humidité et de toute source de chaleur ou d'ignition, et éloigné des aliments et des produits alimentaires et des matières incompatibles[6].
Pour les conditions de stockage et d'utilisation, se reporter à la Circulaire DGS/SD 7 A/DRT/CT 4 n° 2003-47 du 30 janvier 2003 relative aux risques d'incendie ou d'explosion lors du stockage et/ou de l'utilisation de produits de traitement des eaux de piscine.
- En cas d'ingestion, il convient de rincer la bouche, de ne pas faire vomir, mettre au repos et consulter un médecin[6].
- En cas de contact avec les yeux, il convient de rincer d'abord abondamment à l'eau pendant plusieurs minutes (retirer si possible les lentilles de contact), puis de consulter un médecin[6].
- En cas de contact avec la peau, il faut retirer les vêtements contaminés, rincer la peau abondamment à l'eau ou prendre une douche et consulter un médecin[6].
Notes et références
Voir aussi
Wikiwand - on
Seamless Wikipedia browsing. On steroids.






