
Tétrafluorure de soufre
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Tétrafluorure de soufre?
Résumez cet article pour un enfant de 10 ans
AFFICHER TOUTES LES QUESTIONS
Le tétrafluorure de soufre est le composé chimique de formule SF4. C'est un gaz corrosif qui produit de l'acide fluorhydrique HF en présence d'eau ou d'humidité, mais qui est également très utilisé comme réactif dans la préparation de composés organofluorés[6] dont certains sont importants en chimie de spécialité et dans l'industrie pharmaceutique.
Faits en bref Identification, No CAS ...
| Tétrafluorure de soufre | |
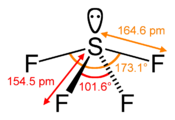   Structure du tétrafluorure de soufre |
|
| Identification | |
|---|---|
| No CAS | 7783-60-0 |
| No ECHA | 100.029.103 |
| No CE | 232-013-4 |
| Propriétés chimiques | |
| Formule | F4SSF4 |
| Masse molaire[1] | 108,059 ± 0,005 g/mol F 70,33 %, S 29,67 %, |
| Moment dipolaire | 0,632 ± 0,003 D [2] |
| Propriétés physiques | |
| T° fusion | −121 °C |
| T° ébullition | −38 °C à 101,3 kPa |
| Masse volumique | 1 950 kg·m-3 à −78 °C |
| Point critique | 90,85 °C [3] |
| Thermochimie | |
| ΔvapH° | 26,44 kJ·mol-1 (1 atm, −40,45 °C)[4] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 12,0 ± 0,3 eV (gaz)[5] |
| Précautions | |
| Directive 67/548/EEC | |
Symboles : T+ : Très toxique C : Corrosif Phrases R : R26 : Très toxique par inhalation. R35 : Provoque de graves brûlures. Phrases S : (S1) : Conserver sous clé. S9 : Conserver le récipient dans un endroit bien ventilé. S26 : En cas de contact avec les yeux, laver immédiatement et abondamment avec de l’eau et consulter un spécialiste. S45 : En cas d’accident ou de malaise, consulter immédiatement un médecin (si possible, lui montrer l’étiquette). S36/37/39 : Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage. |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Fermer

