| Méthylamine |
|
|
Structure de la méthylamine |
| Identification |
| Nom UICPA
|
aminométhane
|
| Synonymes
|
Méthanamine
Monométhylamine
|
| No CAS
|
74-89-5
|
| No ECHA
|
100.000.746 |
| No CE
|
200-820-0
|
| SMILES
|
|
| InChI
|
InChI : vue 3D InChI =1/CH5N/c1-2/h2H2,1H3 |
| Apparence
|
gaz comprimé liquéfié incolore, d'odeur caractéristique. (anhydre)
Ou solution incolore dans l'eau, d'odeur âcre. (solution aqueuse à 40 %)[1]
|
| Propriétés chimiques |
| Formule
|
CH5N [Isomères]
|
| Masse molaire[2]
|
31,057 1 ± 0,001 4 g/mol
C 38,67 %, H 16,23 %, N 45,1 %,
|
| pKa
|
10,63
|
| Moment dipolaire
|
1,31 ± 0,03 D [3]
|
| Propriétés physiques |
| T° fusion
|
−93 °C (anhydre)[1],
−39 °C (solution à 40 %)[1]
|
| T° ébullition
|
−6 °C (anhydre)[1],
48 °C (solution à 40 %)[1]
|
| Solubilité
|
1 080 g·l-1 (20 °C)
|
| Paramètre de solubilité δ
|
22,9 MPa1/2 (25 °C)[4]
|
| Masse volumique
|
0,89 g·cm-3 (solution à 40 %)[1],
0,699 g·cm-3 (−10,8 °C)[5]
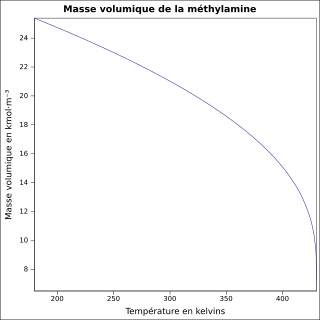
équation[6] : 
Masse volumique du liquide en kmol·m-3 et température en kelvins, de 179,69 à 430,05 K.
Valeurs calculées :
0,6551 g·cm-3 à 25 °C.
| T (K) |
T (°C) |
ρ (kmol·m-3) |
ρ (g·cm-3) |
|---|
| 179,69 |
−93,46 |
25,378 |
0,78816 |
| 196,38 |
−76,77 |
24,84482 |
0,77161 |
| 204,73 |
−68,42 |
24,57165 |
0,76312 |
| 213,07 |
−60,08 |
24,29369 |
0,75449 |
| 221,42 |
−51,73 |
24,01063 |
0,7457 |
| 229,76 |
−43,39 |
23,72214 |
0,73674 |
| 238,11 |
−35,04 |
23,42785 |
0,7276 |
| 246,45 |
−26,7 |
23,12733 |
0,71827 |
| 254,8 |
−18,35 |
22,82014 |
0,70873 |
| 263,14 |
−10,01 |
22,50574 |
0,69896 |
| 271,49 |
−1,66 |
22,18355 |
0,68895 |
| 279,83 |
6,68 |
21,85288 |
0,67868 |
| 288,18 |
15,03 |
21,51295 |
0,66813 |
| 296,52 |
23,37 |
21,16287 |
0,65726 |
| 304,87 |
31,72 |
20,80158 |
0,64603 |
|
| T (K) |
T (°C) |
ρ (kmol·m-3) |
ρ (g·cm-3) |
|---|
| 313,22 |
40,07 |
20,42785 |
0,63443 |
| 321,56 |
48,41 |
20,04018 |
0,62239 |
| 329,91 |
56,76 |
19,63678 |
0,60986 |
| 338,25 |
65,1 |
19,21546 |
0,59677 |
| 346,6 |
73,45 |
18,77348 |
0,58305 |
| 354,94 |
81,79 |
18,30734 |
0,56857 |
| 363,29 |
90,14 |
17,81246 |
0,5532 |
| 371,63 |
98,48 |
17,2827 |
0,53675 |
| 379,98 |
106,83 |
16,70943 |
0,51894 |
| 388,32 |
115,17 |
16,07995 |
0,49939 |
| 396,67 |
123,52 |
15,37422 |
0,47748 |
| 405,01 |
131,86 |
14,5573 |
0,45211 |
| 413,36 |
140,21 |
13,55778 |
0,42106 |
| 421,7 |
148,55 |
12,17728 |
0,37819 |
| 430,05 |
156,9 |
6,494 |
0,20168 |
|
|
| T° d'auto-inflammation
|
430 °C[1]
|
| Point d’éclair
|
−10 °C[1]
|
| Limites d’explosivité dans l’air
|
4,9–20,7 % vol[1]
|
| Pression de vapeur saturante
|
à 20 °C : 304 kPa[1]
équation[6] : 
Pression en pascals et température en kelvins, de 179,69 à 430,05 K.
Valeurs calculées :
353 279,48 Pa à 25 °C.
| T (K) |
T (°C) |
P (Pa) |
|---|
| 179,69 |
−93,46 |
176,71 |
| 196,38 |
−76,77 |
1 003,07 |
| 204,73 |
−68,42 |
2 113,85 |
| 213,07 |
−60,08 |
4 161,6 |
| 221,42 |
−51,73 |
7 717,87 |
| 229,76 |
−43,39 |
13 578,62 |
| 238,11 |
−35,04 |
22 801,38 |
| 246,45 |
−26,7 |
36 734,36 |
| 254,8 |
−18,35 |
57 035,16 |
| 263,14 |
−10,01 |
85 677,8 |
| 271,49 |
−1,66 |
124 948,13 |
| 279,83 |
6,68 |
177 428,76 |
| 288,18 |
15,03 |
245 975,57 |
| 296,52 |
23,37 |
333 688,21 |
| 304,87 |
31,72 |
443 877,25 |
|
| T (K) |
T (°C) |
P (Pa) |
|---|
| 313,22 |
40,07 |
580 030,75 |
| 321,56 |
48,41 |
745 782,46 |
| 329,91 |
56,76 |
944 883,61 |
| 338,25 |
65,1 |
1 181 179,97 |
| 346,6 |
73,45 |
1 458 595 |
| 354,94 |
81,79 |
1 781 119,91 |
| 363,29 |
90,14 |
2 152 810,81 |
| 371,63 |
98,48 |
2 577 792,99 |
| 379,98 |
106,83 |
3 060 272,07 |
| 388,32 |
115,17 |
3 604 551,65 |
| 396,67 |
123,52 |
4 215 057,18 |
| 405,01 |
131,86 |
4 896 365,31 |
| 413,36 |
140,21 |
5 653 238,56 |
| 421,7 |
148,55 |
6 490 664,86 |
| 430,05 |
156,9 |
7 413 900
|
|
 |
| Point critique
|
74,3 bar, 156,85 °C [7]
|
| Thermochimie |
| S0liquide, 1 bar
|
150 J/mol.K
|
| ΔfH0liquide
|
-47 kJ/mol
|
| Cp
|
101,8 J/mol.K (−14 °C)
équation[6] : 
Capacité thermique du liquide en J·kmol-1·K-1 et température en kelvins, de 179,69 à 266,82 K.
Valeurs calculées :
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 179,69 |
−93,46 |
99 250 |
3 196 |
| 185 |
−88,15 |
99 448 |
3 202 |
| 188 |
−85,15 |
99 561 |
3 206 |
| 191 |
−82,15 |
99 673 |
3 209 |
| 194 |
−79,15 |
99 785 |
3 213 |
| 197 |
−76,15 |
99 898 |
3 217 |
| 200 |
−73,15 |
100 010 |
3 220 |
| 202 |
−71,15 |
100 085 |
3 223 |
| 205 |
−68,15 |
100 197 |
3 226 |
| 208 |
−65,15 |
100 310 |
3 230 |
| 211 |
−62,15 |
100 422 |
3 233 |
| 214 |
−59,15 |
100 534 |
3 237 |
| 217 |
−56,15 |
100 647 |
3 241 |
| 220 |
−53,15 |
100 759 |
3 244 |
| 223 |
−50,15 |
100 871 |
3 248 |
|
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 226 |
−47,15 |
100 984 |
3 252 |
| 229 |
−44,15 |
101 096 |
3 255 |
| 231 |
−42,15 |
101 171 |
3 258 |
| 234 |
−39,15 |
101 283 |
3 261 |
| 237 |
−36,15 |
101 396 |
3 265 |
| 240 |
−33,15 |
101 508 |
3 268 |
| 243 |
−30,15 |
101 620 |
3 272 |
| 246 |
−27,15 |
101 733 |
3 276 |
| 249 |
−24,15 |
101 845 |
3 279 |
| 252 |
−21,15 |
101 957 |
3 283 |
| 255 |
−18,15 |
102 070 |
3 287 |
| 258 |
−15,15 |
102 182 |
3 290 |
| 261 |
−12,15 |
102 294 |
3 294 |
| 263 |
−10,15 |
102 369 |
3 296 |
| 266,82 |
−6,33 |
102 510 |
3 301 |
|

équation[8] : 
Capacité thermique du gaz en J·mol-1·K-1 et température en kelvins, de 100 à 1 500 K.
Valeurs calculées :
52,102 J·mol-1·K-1 à 25 °C.
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 100 |
−173,15 |
40 803 |
1 314 |
| 193 |
−80,15 |
44 853 |
1 444 |
| 240 |
−33,15 |
47 812 |
1 539 |
| 286 |
12,85 |
51 157 |
1 647 |
| 333 |
59,85 |
54 933 |
1 769 |
| 380 |
106,85 |
58 978 |
1 899 |
| 426 |
152,85 |
63 113 |
2 032 |
| 473 |
199,85 |
67 440 |
2 171 |
| 520 |
246,85 |
71 798 |
2 312 |
| 566 |
292,85 |
76 033 |
2 448 |
| 613 |
339,85 |
80 272 |
2 585 |
| 660 |
386,85 |
84 374 |
2 717 |
| 706 |
432,85 |
88 216 |
2 840 |
| 753 |
479,85 |
91 933 |
2 960 |
| 800 |
526,85 |
95 411 |
3 072 |
|
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 846 |
572,85 |
98 568 |
3 174 |
| 893 |
619,85 |
101 530 |
3 269 |
| 940 |
666,85 |
104 222 |
3 356 |
| 986 |
712,85 |
106 599 |
3 432 |
| 1 033 |
759,85 |
108 776 |
3 502 |
| 1 080 |
806,85 |
110 720 |
3 565 |
| 1 126 |
852,85 |
112 421 |
3 620 |
| 1 173 |
899,85 |
113 988 |
3 670 |
| 1 220 |
946,85 |
115 426 |
3 717 |
| 1 266 |
992,85 |
116 754 |
3 759 |
| 1 313 |
1 039,85 |
118 089 |
3 802 |
| 1 360 |
1 086,85 |
119 465 |
3 847 |
| 1 406 |
1 132,85 |
120 922 |
3 894 |
| 1 453 |
1 179,85 |
122 603 |
3 948 |
| 1 500 |
1 226,85 |
124 566 |
4 011 |
|
|
| Précautions |
| SGH[9] |
H220, H315, H318, H332 et H335H220 : Gaz extrêmement inflammable
H315 : Provoque une irritation cutanée
H318 : Provoque des lésions oculaires graves
H332 : Nocif par inhalation
H335 : Peut irriter les voies respiratoires
H224, H302, H314 et H332H224 : Liquide et vapeurs extrêmement inflammables
H302 : Nocif en cas d'ingestion
H314 : Provoque de graves brûlures de la peau et des lésions oculaires
H332 : Nocif par inhalation
|
| SIMDUT[10] |
   
A, B1, D1A, E, A : Gaz comprimé tension de vapeur absolue à 50 °C = 700 kPaB1 : Gaz inflammable limite inférieure d'inflammabilité = 4,9 % D1A : Matière très toxique ayant des effets immédiats graves létalité aiguë : CL50 inhalation/4 heures (rat, femelle) = 354 ppmE : Matière corrosive nécrose de la peau chez l'animal Divulgation à 0,1 % selon la liste de divulgation des ingrédients |
| NFPA 704 |
|
| Transport |
|
| Écotoxicologie |
| LogP
|
-0,71 (anhydre)[1],
-0.6 (solution à 40 %)[1]
|
| Seuil de l’odorat
|
bas : 0,000 9 ppm
haut : 4,68 ppm[11]
|
|
| Unités du SI et CNTP, sauf indication contraire. |
modifier  |




















