Loading AI tools
composé chimique De Wikipédia, l'encyclopédie libre
Le bromure de fer(II) est un composé inorganique de formule chimique FeBr2. Le composé anhydre est un solide paramagnétique de couleur jaune ou brunâtre. Plusieurs hydrates de FeBr2 sont également connus, tous étant des solides de couleur pâle. C'est un précurseur commun à d'autres composés du fer en laboratoire de recherche, mais aucune application n'existe pour ce composé.
| Bromure de fer(II) | |
| |
| Identification | |
|---|---|
| Nom UICPA | Bromure de fer(II) |
| No CAS | |
| No ECHA | 100.029.244 |
| PubChem | |
| Apparence | solide jaune-marron |
| Propriétés chimiques | |
| Formule | FeBr2 |
| Masse molaire[1] | 215,653 ± 0,004 g/mol Br 74,1 %, Fe 25,9 %, |
| Propriétés physiques | |
| T° fusion | 684 °C[réf. souhaitée] |
| T° ébullition | 934 °C[réf. souhaitée] |
| Solubilité | 117 g/100 ml d'eau[réf. souhaitée] |
| Masse volumique | 4,63 g cm−3, solide[réf. souhaitée] |
| Cristallographie | |
| Système cristallin | Rhomboédrique |
| Symbole de Pearson | hP3 |
| Classe cristalline ou groupe d’espace | P3m1, (no 164) |
| Structure type | CdI2 |
| Composés apparentés | |
| Autres cations | Bromure de fer(III) |
| Autres anions | Chlorure de fer(II) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
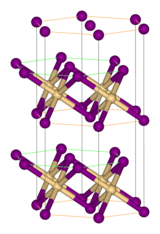
Comme la plupart des halogénures métalliques, FeBr2 adopte une structure polymérique composée de centres métalliques isolés réticulés avec des halogénures. Il cristallise avec la structure CdI2, comportant des couches serrées d'ions bromure, entre lesquelles se trouvent des ions Fe(II) dans des trous octaédriques[2]. L'emballage des halogénures est légèrement différent de celui du FeCl2, qui adopte le motif CdCl2.
Ce composé est synthétisé à l'aide d'une solution d'acide bromhydrique concentré et de poudre de fer dans du méthanol. On additionne du dihydrogène gazeux sur le complexe [Fe(MeOH)6]Br2. Le chauffage du complexe de méthanol sous vide donne du FeBr2 pur[3].
FeBr2 réagit avec deux équivalents de bromure de tétraéthylammonium pour donner [(C2H5)4N]2FeBr4[4]. FeBr2 réagit avec le bromure et le brome pour former les espèces à valence mixte de couleur intense [FeBr3Br9]−[5].
FeBr2 possède un fort métamagnétisme à 4,2 K et a longtemps été étudié comme un composé métamagnétique prototypique[6],[7].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.