
Bicarbonate de sodium
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Bicarbonate de sodium?
Résumez cet article pour un enfant de 10 ans
Le bicarbonate de sodium Écouter (ou carbonate monosodique ou carbonate acide de sodium, anciennement bicarbonate de soude[alpha 1]), l'hydrogénocarbonate de sodium en nomenclature moderne, est un composé inorganique décrit par la formule brute NaHCO3.
| Bicarbonate de sodium | ||
 | ||
 | ||
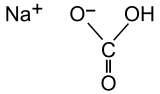
| Structure et poudre de bicarbonate de sodium | ||
| Identification | ||
|---|---|---|
| Nom UICPA | hydrogénocarbonate de sodium | |
| Synonymes |
bicarbonate de soude, carbonate acide de sodium (ancienne appellation en pharmacie) |
|
| No CAS | 144-55-8 | |
| No ECHA | 100.005.122 | |
| No CE | 205-633-8 | |
| Code ATC | B05CB04 B05XA02 « QG04BQ01 » | |
| No E | E500(ii) | |
| SMILES | ||
| InChI | ||
| Apparence | solide blanc en prisme (pur), mais aussi en pratique de formes variables[1] | |
| Propriétés chimiques | ||
| Formule | CHNaO3NaHCO3 | |
| Masse molaire[2] | 84,006 6 ± 0,001 8 g/mol C 14,3 %, H 1,2 %, Na 27,37 %, O 57,14 %, 84,01 g/mol |
|
| pKa | pKa1=10,33, pKa2=6,33 (couples HCO3− / CO32− et CO2 dissous / HCO3−) | |
| Propriétés physiques | ||
| T° fusion | 270 °C (décomposition en NaOH par perte de CO2) mais bicarbonate avec traces d'acides se décompose lentement dès 50 °C en solide Na2CO3, gaz CO2 et vapeur d'eau[3] | |
| Solubilité | 87 g l−1 (eau, 20 °C)[1] |
|
| Masse volumique | 2,22 g cm−3 à 20 °C[4] | |
| Thermochimie | ||
| ΔfH0solide | −947 kJ mol−1(24,85 °C)[5] | |
| ΔfusH° | 136 J mol−1 K−1(24,85 °C) | |
| Cp | 87,7 kJ K−1 mol−1 (25 °C)[3] | |
| Cristallographie | ||
| Système cristallin | monoclinique | |
| Propriétés optiques | ||
| Indice de réfraction | 1,500 | |
| Précautions | ||
| SIMDUT[6] | ||
Produit non contrôlé Ce produit n'est pas contrôlé selon les critères de classification du SIMDUT. |
||
| Considérations thérapeutiques | ||
| Classe thérapeutique | Antiacide | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
C'est un composé ionique blanc de l'anion hydrogénocarbonate et du cation sodium, qui se présente sous forme de poudre. La forme ultra pure, très rare, est constituée de cristaux prismatiques blancs.
Ce corps minéral anhydre, sous l'appellation minéralogique de nahcolite, apparaît néanmoins dans la nature sous la forme d'agrégats de cristaux prismatiques, le plus souvent en veines fibreuses ou en concrétions. Au laboratoire, l'hydrogénocarbonate de sodium apparaît sous la forme de fins cristaux blancs, solubles dans l'eau.