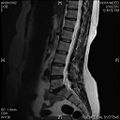
تصویربرداری تشدید مغناطیسی
نوعی تصویربرداری تشخیصی که در آن از تشدید مغناطیسی هستهها استفاده میشود از ویکیپدیا، دانشنامه آزاد
امآرآی (به انگلیسی: MRI) که سرواژه عبارت Magnetic Resonance Imaging بهمعنای تصویربرداری تشدید مغناطیسی[۱] است، روشی پرتونگارانه در تصویربرداری تشخیصی پزشکی و دامپزشکی است که در دهههای اخیر بسیار فراگیر شدهاست و بر اساس پدیده تشدید مغناطیسی هستهای عمل میکند.[۲]
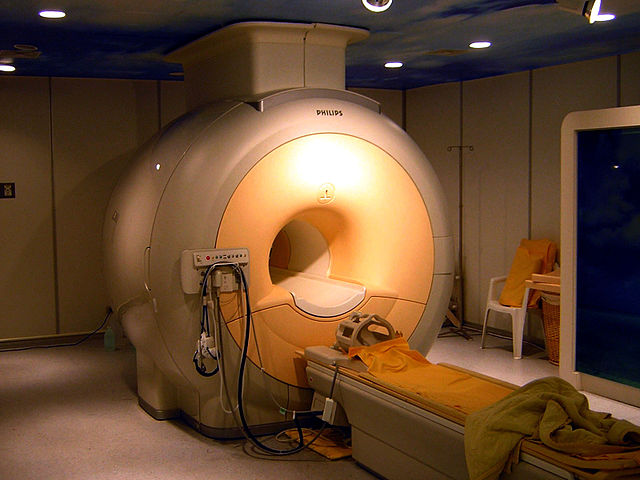
تشریح
خلاصه
دیدگاه

اساس امآرآی مبتنی بر حرکت اسپینی هستههای اتمی موجود در بدن است. این اسپینها از اسپینهای فردی پروتونها و نوترونهای درون هسته، ناشی میشود. با توجه با اینکه در اتم هیدروژن فقط یک پروتون وجود دارد، خود هسته یک اسپین خالص یا گشتاور زاویهای دارد. اسپینها هنگام قرار گرفتن در میدان مغناطیسی خارجی مرتب میشوند. برخی با میدان هم راستا میشوند، و تعداد کمتری از اسپینها پاد موازی با میدان مغناطیسی هم راستا میشوند. سپس، اعمال یک پالس الکترومغناطیسی کوتاهمدت با بسامد در محدوده رادیویی (RF pulse) سبب ایجاد پدیده تشدید مغناطیسی هستهای در اسپینها شده، آنها را نسبت به میدان مغناطیسی اصلی خارجی منحرف کرده، و به حرکت تقدیمی وامیدارد. به زاویهای که بین اسپینها و میدان مغناطیسی خارجی ایجاد میشود، زاویه تکان (Flip angle) گفته میشود. در نهایت، حرکت تقدیمی اسپینها باعث ایجاد یک میدان مغناطیسی متناوب میشود و طبق قانون القاء فارادی اگر یک سیمپیچ گیرنده در نزدیکی این میدان مغناطیسی قرار گیرد، ولتاژ در سیمپیچ القاء شده و سیگنال امآرآی تولید میشود.
با امآرآی میتوان در جهات فوقانی-تحتانی (اگزیال)، چپراستی (ساژیتال) و پسوپیش (کورونال) و حتّی در جهات اُریب و مایل تصویربرداری کرد. یک سیستم امآرآی از سه گروه میدان مغناطیسی استفاده میکند:
- میدان خارجی ثابت و قوی (B0)
- میدان ضعیف گرادیانی متغیر
- میدان حاصل از پالس رادیویی (B۱)

قدرت سیگنالی که در MRI بهوجود میآید به دو عامل دانسیته پروتونها و زمانهای استراحت T۱ و T۲ بستگی دارد. T۱ مدت زمانی است که ۶۳٪ ممان مغناطیسی طولی یک پروتون پس از برانگیختگی، از راستای عمود بر میدان به راستای موازات میدان مغناطیسی بازمیگردد. همچنین T۲ مدت زمانیست که ممان مغناطیسی عرضی یک پروتون پس از برانگیختگی، به ۳۷٪ مقدار اولیه خود تنزل مییابد. اکثر فرایندهای پاتولوژیک، موجب افزایش زمان استراحتِ T۱ و T۲ یا همان Relaxation time آنها میشوند و لذا در مقایسه با بافتهای طبیعی اطراف، در تصاویر T1-weighted سیگنال پایینتر (تیره رنگ تر) و در تصاویر T2-wighted سیگنال بالاتر (روشنتر یا سفیدتر) خواهند داشت.[۳]
خطرهای امآرآی
برخلاف سایر دستگاههای تصویربرداری مثل اشعه ایکس و سیتی اسکن، ام آر آی از تشعشع یونیزه استفاده نمیکند. از این ابزار میتوان برای تصویربرداری از جنین در دوران بارداری استفاده کرد بدون آن که اثری روی آن داشته باشد. از آنجایی که در فرایند ام آر آی از مغناطیس قوی استفاده میشود هر قطعه فلزی که در بدن وجود داشته باشد مثل ضربان ساز قلب، مفصل مصنوعی، دریچه مصنوعی قلب، حلزون مصنوعی گوش یا هر نوع صفحه و پیچ و مهره فلزی در بدن ممکن است خطرساز باشد، چون میدان مغناطیسی میتواند باعث جابجایی یا گرم شدن آن قطعه شود.
بنابراین لازم است تکنولوژیست امآرآی سوالات لازم را قبل از انجام این فرایند از بیمار بپرسد. البته بیشتر قطعات فلزی که امروز در ایمپلنتهای بدن استفاده قرار میشوند تحت تأثیر میدانهای مغناطیسی قرار نمیگیرند و به اصطلاح MR-Safe هستند. علاوه بر این، هنگام اسکن، دستگاه ام آر آی صداهای بلندی تولید میکند که ممکن است باعث ناراحتی فرد شود، بنابراین استفاده از حفاظ گوش در طول این فرایند ضروری است.
سیستمهای امروزی
سیستمهای ام آرآی تشخیصی امروزه غالباً دارای قدرت میدانهای ۰/۲، ۱، ۱/۵، و ۳ تسلا میباشند. سیستمهای پژوهشی گستره بزرگتری را شامل شده و از ۰٫۰۵ تسلا تا ۱۴ تسلا را شامل میشوند.
در ایالات متحده آمریکا بیمارستانها و مراکز خدمات بهداشتی اجازه استفاده از سیستمهای تا ۴ تسلا را نیز برای یک بیمار دارند. اما از چهار تسلا به بالا صرفاً جنبه و کاربردهای تحقیقاتی دارد.
بزرگترین تولیدکنندههای سیستمهای ام آر آی امروزه شرکتهای زیمنس (آلمان)، جنرال الکتریک (آمریکا)، توشیبا (ژاپن)، و فیلیپس (هلند) میباشند.
تاریخچه
خلاصه
دیدگاه
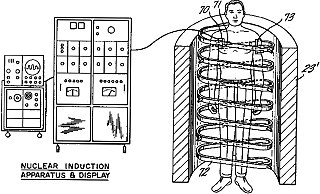
در سال ۱۹۵۰، حصول تصویر یک بعدی تشدید مغناطیسی توسط هرمن کار (Herman Carr) گزارش گردید. پال لاتربر، شیمیدان آمریکایی با کار بر روی تحقیقات پیشین، موفق به ابداع روشهایی برای تولید تصاویر دو بعدی و سه بعدی تشدید مغناطیسی گردید.[۴] سرانجام وی در سال ۱۹۷۳ اولین تصویر گرفته شده بر اساس تشدید مغناطیس هستهای (NMR) خود را منتشر نمود.[۵] اولین تصویر مقطع نگاری از یک موش زنده در ژانویه ۱۹۷۴ منتشر گردید.
از سوی دیگر تحقیقات و پیشرفتهای مهمی در زمینهٔ تصویر برداری بر اساس تشدید مغناطیسی هسته برای نخستین بار در دانشگاه ناتینگهام انگلستان صورت پذیرفت، جایی که پیتر منسفیلد فیزیکدان برجستهٔ آن مؤسسه با گسترش یک روش ریاضی موفق به کاهش زمان تصویربرداری و افزایش کیفیت تصاویر نسبت به روش بکارگرفته شده توسط لاتربر گردید. در همان زمان در سال ۱۹۷۱ دانشمند آمریکایی ارمنیتبار ریموند دامادیان استاد دانشگاه ایالتی نیویورک در مقالهای که در مجلهٔ Science منتشر گردید،[۶] اعلام نمود که امکان تشخیص تومور از بافتهای عادی به کمک تصویر برداری NMR میسر میباشد.
سرانجام جایزهٔ نوبل پزشکی سال ۲۰۰۳ به خاطر اختراع ام آر آی به پال لاتربر از دانشگاه ایلینوی در اوربانا شامپاین[۷] و پیتر منسفیلد از انگلستان اعطا گردید.
طرز کار
خلاصه
دیدگاه
چگونگی تولید تصویر ام آر آی فرایند بس پیچیدهایست. در این روش از خاصیت ویژهٔ اسپینهای هستههای هیدروژنی در میدان مغناطیسی (B0) استفاده میشود. اسپینها تحت تأثیر میدان مغناطیسی پالسهای الکترومغناطیسی (B۱) قرار گرفته و سپس از این حالت برانگیختگی به مرور به حالت اولیه خود بازمیگردند و در حین این فرایند انرژی خود را به شکل امواج متناوب مغناطیسی در مدت زمان مشخصی (T1 و T2) ساطع میکنند. در هر بافتی این مدت زمان متفاوت است. بهطور مثال در ۱/۵ تسلا ثابت T1 برای بافت چربی ۲۶۰ میلیثانیه و برای بافت ماده خاکستری مغز ۹۲۰ میلیثانیه میباشد. بسته به اینکه چه نوع دنباله پالسیای انتخاب شود، و پارامترهایی مثل زمان اکو و زمان تکرار چگونه تعیین شوند، با استفاده از تفاوت این مقادیر بین بافتهای مختلف میتوان کنتراست دلخواه را به تصویر کشید و توانایی یکتای امآرآی در همین خاصیت ویژه نهفتهاست.
هر برش تصویری توسط فاز امواج دریافت شده به ترتیب در محورهای y و x کدگذاری میگردد. برای انجام کدگذاری فضایی احتیاج به میدانها مغناطیسی متغیر میباشد که به کمک سیمپیچهای گرادیانی در هر لحظه تولید میگردد. اطلاعات دریافتی در فضای بسامد مکانی دریافت شده و نهایتاً به کمک تبدیلات فوریه ای به شکل تصویر درآورده میشوند.
کیفیت تصویری ام آر آی
معمولاً بهبود کیفیت تصویری در ام آر آی را با مقیاسهایی همانند قدرت تفکیک میسنجند و معمولاً نیز بهبود قدرت تفکیک با خود عواقبی همانند کاهش سیگنال مفید (SNR) به همراه دارد. اما میتوان این مشکلات را با راه حلهایی همانند استفاده از سیستمهای با قدرت میدان Bo بالاتر،[۸] ویا استفاده از ماده حاجب (contrast agents) مناسب[۹] تصحیح نمود.
مقایسه

ام آر آی از بعضی نقاط برتری و از بعضی جهات دیگر نسبت به ابزار دیگر در فیزیک پزشکی ضعف دارد. در قیاس با سی تی اسکن این موارد عبارتند از:[۱۰]
برتریهای امآرآی در مقایسه با سی تی اسکن
- تضاد تصویری (سایهروشن) بالاتر از سی تی اسکن.
- تهیه مقاطع تصویری از جهات مختلف (از جمله اریب).
- عدم استفاده از پرتوهای یونیزهکننده.
- مانند سیتیاسکن موجب سخت شدن باریکه پرتوها (آرتیفکت سخت، beam hardening) نمیشود.
نقاط ضعف ام آر آی در مقایسه با سیتیاسکن
- پر هزینه تر از سیتیاسکن، کمیابتر، و کار با آن مشکلتر است.
- تصویرگیری زمان بیشتری میبرد.
- در میدانهای معناطیسی پایین وضوح تصویری کمتری دارد.
- به دلیل طولانیتر بودن اسکنها عوارض حرکتی بیشتری دارد.
- موجب مشکلات برای بیماران دارای اجسام فلزی در بدن خود میباشد.
- بیمار باید در حین انجام اسکن (ام آر آی) بی حرکت باشد. حرکات غیرقابل پیشگیری مانند تنفس، ضربان قلب و پریستالسیسم اغلب تصویر را مخدوش میسازند.
- برای بیماران دارای مشکلات تنفسی و کسانی که از محیطهای بسته میترسند، عبور از تونل تنگ دستگاه MRI مشکل است.
اسکنهای پایه MRI
خلاصه
دیدگاه

سیگنالهای دریافتی توسط سیستمهای MRI، حاوی اطلاعات بسیار زیادی بوده که میتواند در استخراج اطلاعات فیزیکی و شیمیایی جسم یا بافت مورد نظر، به کار گرفته شود. با توجه به اطلاعات مطلوب، سیستم MRI برنامهریزی میگردد و در نهایت تصویرسازی به یکی از روشهای زیر یا روشهای ترکیبی نمایش داده میشود.
MRI با وزندهی T1
اثر اصلی: زمان استراحت اسپین-لاتیس
این یک روش پایه در اسکن MRI میباشد، برای مثال، در این روش تصویر سازی، تفاوت دو بافت چربی و آب، به صورت تیرهتر بودن آب نسبت به بافت چربی در عکسبرداری به کمک دنباله اکو گردایان (GRE) با TE کوتاه و TR کوتاه میباشد.
MRI با وزندهی T2
اثر اصلی: زمان استراحت اسپین-اسپین
این روش نیز یکی از روشهای اصلی تصویرسازی MRI میباشد. در این روش نیز مانند وزندهی T1، چربی و آب قابل تفکیک بوده با این تفاوت که چربی تیرهتر و آب روشنتر در تصویر ظاهر میگردد. برای مثال در مطالعه مغز و ستون فقرات، مایع مغزی نخاعی به صورت روشنتر در تصویر ظاهر میگردد. این روش برای شرایطی با TE و TR طولانی مناسب میباشد.
در این روش، از توالی اکو گرادیان (GRE) با TE و TR طولانی استفاده میگردد.
MRI با وزندهی چگالی اسپین ها-چگالی پروتون
این روش به نام چگالی پروتون نیز شناخته میشود. کنترست در تصاویر حاصل از این روش تصویر سازی، حاصل از مقادیر T1 وT2 نبوده و تنها به اختلاف چگالی اسپینهای اتم هیدروژن موجود در بافتها وابسته میباشد. در این روش TE کوتاه و TR طولانی میباشد.[۱۱]
روشها و کاربردهای دیگر
تصویربرداری مولکولی و fMRI

این روش برای اولین بار در بهار سال ۱۹۹۱ در مرکز بیمارستان massachusetts در بوستون آمریکا به منظور نقشهبرداری از فعالیتهای مغزی مورد آزمایش قرار گرفت. در این روش غیر تهاجمی تصاویری بر اساس تغییرات محلی در جریان خون مغز گرفته میشود. در روزهای که
طیفنگاری (MRS)
آنژیوگرافی (MRA)
تصویر برداری تشدید مغناطیسی موازی (PMRI)
جستارهای وابسته

- افکنش شدت بیشینه
- دنبالههای پالسی
- کدگذاری فضایی
- آرتیفکت در تصویرسازی تشدید مغناطیسی
- تصویرگیری با تنسور پخش
منابع
پیوند به بیرون
Wikiwand - on
Seamless Wikipedia browsing. On steroids.