Top Qs
Línea de tiempo
Chat
Contexto
Ácido nítrico
compuesto químico De Wikipedia, la enciclopedia libre
Remove ads
El compuesto químico ácido nítrico (HNO3)[2] es un líquido viscoso y corrosivo que puede ocasionar graves quemaduras en los seres vivos.[3] Se utiliza como reactivo de laboratorio y para fabricar explosivos como la nitroglicerina y trinitrotolueno (TNT), así como fertilizantes como el nitrato de amonio. Tiene usos adicionales en metalurgia y en refinado, ya que reacciona con la mayoría de los metales y en la síntesis química. Cuando se mezcla con el ácido clorhídrico forma el agua regia, un raro reactivo capaz de disolver el oro y el platino. El ácido nítrico también es un componente de la lluvia ácida.
Remove ads
El compuesto es incoloro, pero las muestras más antiguas tienden a tener un tinte amarillo debido a la descomposición en óxido de nitrógeno. La mayor parte del ácido nítrico comercial tiene una concentración del 68% en agua. Cuando la solución contiene más del 86% de HNO
3, se denomina ácido nítrico fumante. Dependiendo de la cantidad de dióxido de nitrógeno presente, el ácido nítrico fumante se caracteriza además como ácido nítrico fumante rojo en concentraciones superiores al 86%, o ácido nítrico fumante blanco en concentraciones superiores al 95%.
El ácido nítrico es el principal reactivo utilizado para la nitración - la adición de un grupo nitro, normalmente a una molécula orgánica. Aunque algunos nitroderivados resultantes son explosivos sensibles a los golpes y al calor, unos pocos son lo suficientemente estables como para utilizarse en municiones y demoliciones, mientras que otros son aún más estables y se utilizan como pigmentos en tintas y tintes. El ácido nítrico también suele utilizarse como agente oxidante fuerte.
Remove ads
Síntesis
El ácido nítrico se obtiene mezclando pentóxido de dinitrógeno (N2O5) y agua. Sintetizar ácido nítrico puro impone habitualmente la destilación con ácido sulfúrico, ya que el ácido nítrico forma un azeótropo con el agua en una composición del 68 % de ácido nítrico y 32 % de agua. Las soluciones comerciales incluyen entre un 52 % y un 68 % de ácido nítrico. Si la solución incluye más de un 86 % de ácido nítrico se nombra como ácido nítrico fumante y viene en dos variedades, blanco y rojo. El ácido nítrico blanco fumante también se llama 100 % ya que casi no tiene agua (menos de un 1 %) según el proceso.
A nivel industrial, se fabrica mediante la síntesis del amoníaco y oxígeno. Ambos elementos se combinan en un reactor de grandes proporciones ante la presencia de un catalizador metálico. Debido a las altas temperaturas que se soportan (700-900 °C), se utilizan metales que mantengan sus características físicas a estas temperaturas, siendo el más apropiado el platino, en combinación con rodio (5-10 %) que le aporta más rigidez.
Remove ads
Propiedades
Resumir
Contexto
Propiedades físicas
El ácido nítrico puro es un líquido viscoso, incoloro e inodoro. A menudo, distintas impurezas lo colorean de amarillo-marrón. A temperatura ambiente libera humos amarillos. El ácido nítrico concentrado tiñe la piel humana de amarillo al contacto, debido a la presencia de grupos aromáticos presentes en la queratina de la piel.
- Punto de ebullición: 83 °C
- Punto de fusión: −41,6 °C
- Densidad relativa (agua = 1): 1,4
- Solubilidad en agua: miscible
- Presión de vapor a 20 °C: 6,4 kPa
- Densidad relativa de vapor (aire = 1): 2,2
Propiedades químicas
El ácido nítrico es un agente oxidante potente; sus reacciones con compuestos como los cianuros, carburos, y polvos metálicos pueden ser explosivas. Las reacciones del ácido nítrico con muchos compuestos orgánicos, como de la trementina, son violentas, la mezcla siendo hipergólica (es decir, autoinflamable). Es un oxácido fuerte: en solución acuosa se disocia completamente en un ion nitrato NO3- y un protón hídrico. Las sales del ácido nítrico (que contienen el ion nitrato) se llaman nitratos.
Contaminación con dióxido de nitrógeno

El ácido nítrico está sujeto a la termal o descomposición por la luz y por esta razón a menudo se almacenaba en botellas de vidrio marrón:
- 4 HNO
3 → 2 H
2O + 4 NO
2 + O
2
Esta reacción puede dar lugar a algunas variaciones no despreciables de la presión de vapor sobre el líquido porque los óxidos de nitrógeno producidos se disuelven parcial o totalmente en el ácido.
El dióxido de nitrógeno (NO
2) y/o el tetróxido de dinitrógeno (N
2O
4) permanecen disueltos en el ácido nítrico coloreándolo de amarillo o incluso de rojo a temperaturas más elevadas. Mientras que el ácido puro tiende a desprender vapores blancos cuando se expone al aire, el ácido con dióxido de nitrógeno disuelto desprende vapores de color marrón rojizo, lo que da lugar a los nombres comunes de "ácido nítrico fumante rojo" y "ácido nítrico fumante blanco". Los óxidos de nitrógeno (NO
x) son solubles en ácido nítrico.
Ácido nítrico fumante
El ácido nítrico fumante de calidad comercial contiene un 98% de HNO
3 y tiene una densidad de 1,50 g/cm3. Este grado se utiliza a menudo en la industria de explosivos. No es tan volátil ni tan corrosivo como el ácido anhidro y tiene una concentración aproximada de 21,4 M.
El ácido nítrico fumante rojo, o RFNA, contiene cantidades sustanciales de dióxido de nitrógeno disuelto (NO
2) dejando la solución con un color marrón rojizo. Debido al dióxido de nitrógeno disuelto, la densidad del ácido nítrico fumante rojo es menor, de 1,490 g/cm3.
El ácido nítrico fumante inhibido, ya sea el ácido nítrico fumante blanco inhibido (IWFNA) o el ácido nítrico fumante rojo inhibido (IRFNA), puede fabricarse añadiendo entre un 0,6 y un 0,7% de fluoruro de hidrógeno (HF). Este fluoruro se añade para resistencia a la corrosión en depósitos metálicos. El fluoruro crea una capa de fluoruro metálico que protege el metal.
Ácido nítrico anhidro
El ácido nítrico fumante blanco, ácido nítrico puro o WFNA, es muy parecido al ácido nítrico anhidro. Está disponible como ácido nítrico al 99,9% por ensayo. Una especificación para el ácido nítrico fumante blanco es que tiene un máximo de 2% de agua y un máximo de 0,5% de NO
2 disuelto. El ácido nítrico anhidro tiene una densidad de 1,513 g/cm3 y una concentración aproximada de 24 molar. El ácido nítrico anhidro es un líquido móvil incoloro con una densidad de 1,512 g/cm3 que se solidifica a −42 grados Celsius (−43,6 °F) para formar cristales blancos[aclaración requerida]. Al descomponerse en NO
2 y agua, adquiere un tinte amarillo. Hierve a 83 grados Celsius (181,4 °F). Suele almacenarse en una botella de vidrio de color ámbar inastillable con el doble de volumen de espacio libre para permitir la acumulación de presión, pero incluso con esas precauciones la botella debe ventilarse mensualmente para liberar la presión.
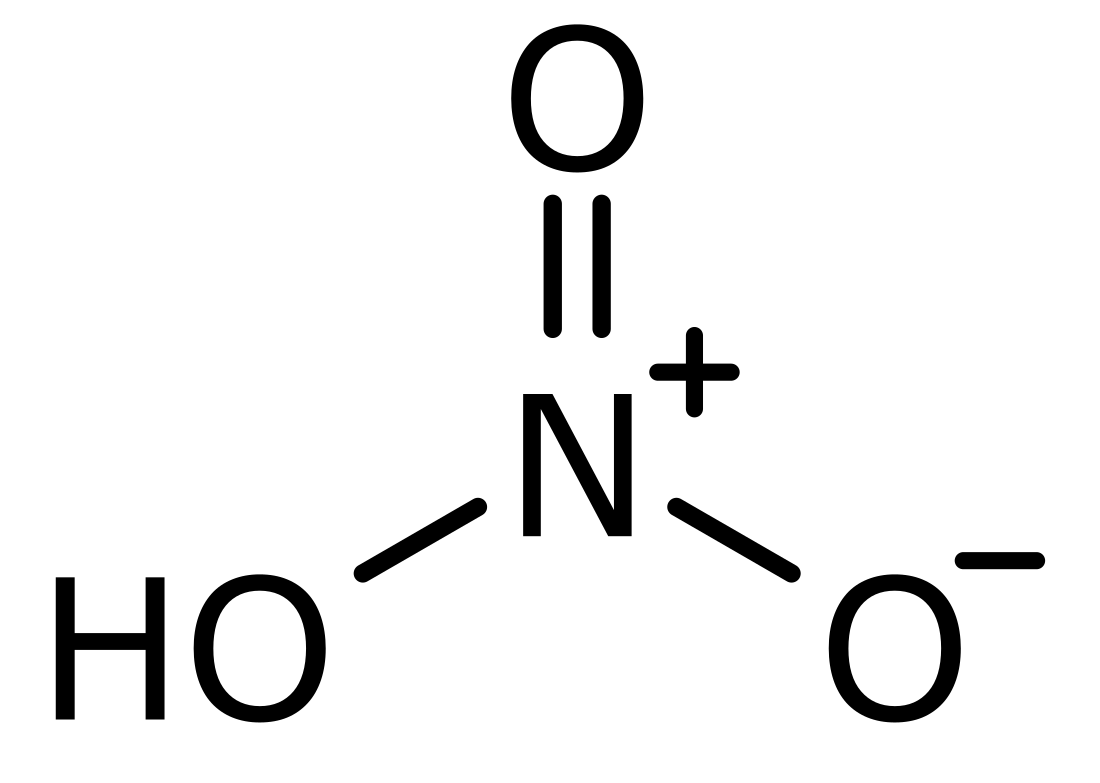
Estructura y enlace

3
Los dos enlaces terminales N-O son casi equivalentes y relativamente cortos, a 1,20 y 1,21 Å.[4] Esto puede explicarse por las teorías de resonancia; las dos principales formas canónicas muestran algún carácter de doble enlace en estos dos enlaces, haciendo que sean más cortos que los de N-O enlace simple. El tercer enlace N-O es alargado porque su átomo de O está unido a un átomo de H,[5][6] con una longitud de enlace de 1,41 Å en la fase gaseosa.[4] La molécula es ligeramente aplanar (los planos del NO
2 y del NOH están inclinados 2° uno respecto al otro) y existe rotación restringida alrededor del enlace sencillo N-OH.[3][7]
Remove ads
Reacciones
Propiedades ácido-base
El ácido nítrico se considera normalmente un ácido fuerte a temperatura ambiente. Existe cierto desacuerdo sobre el valor de la constante de disociación del ácido, aunque el valor de la pKa suele ser inferior a -1. Esto significa que el ácido nítrico en solución diluida se disocia totalmente, excepto en soluciones extremadamente ácidas. El valor pKa se eleva a 1 a una temperatura de 250 °C.[8]
El ácido nítrico puede actuar como base con respecto a un ácido como el ácido sulfúrico:
- HNO
3 + 2 H
2SO
4 ⇌ [NO
2]+
+ [H
3O]+
+ 2 HSO−
4; Constante de equilibrio: K ≈ 22
El ion nitronio, [NO
2]+
, es el reactivo activo en las reacciones de nitración aromática. Dado que el ácido nítrico tiene propiedades tanto ácidas como básicas, puede sufrir una reacción de autoprotolisis, similar a la autoionización del agua:
- 2 HNO
3 ⇌ [NO
2]+
+ NO−
3 + H
2O
Aplicaciones
- Como agente nitrante en la fabricación de explosivos.
- En la fabricación de abonos. El nitrosulfato amónico es un abono nitrogenado simple obtenido químicamente de la reacción del ácido nítrico y sulfúrico con amoniaco.[9]
- El ácido nítrico es empleado en algunos casos en el proceso de pasivación.
- El ácido nítrico es utilizado en grabado artístico (aguafuerte), también se usa para comprobar el oro y el platino.
- En la industria electrónica, es empleado en la elaboración de placas de circuito impreso (PCBs).
- En la industria farmacéutica se usa como agente separador de compuestos altamente básicos en medios orgánicos.
Remove ads
Historia
Resumir
Contexto
Generalmente se cree que el descubrimiento de ácidos minerales como el ácido nítrico se remonta a la alquimia europea del siglo XIII.[10][11][12][13][14] A veces se ha afirmado que el ácido nítrico aparece en varias obras árabes anteriores, como el Ṣundūq al-ḥikma ("Cofre de la sabiduría") atribuida a Jabir ibn Hayyan o el Taʿwīdh al-Ḥākim atribuido al califa fatimí al-Hakim bi-Amr Allah,[15][16] pero la opinión convencional es que el ácido nítrico se describió por primera vez en la obra de pseudo-Geber De inventione veritatis ("Sobre el descubrimiento de la verdad", posterior a c. 1300).Karpenko y Norris, 2002, p. 1002. Como señalan Karpenko y Norris, la datación incierta del corpus pseudo-Geber (que probablemente fue escrito por más de un autor) hace que la fecha de su descripción del ácido nítrico sea igualmente incierta.
Según Al-Hassan, 2001, p. 62, las recetas para la preparación del ácido nítrico también aparecen en el Liber Luminis luminum, un tratado latino atribuido generalmente a Michael Scot (fallecido antes de 1236) pero quizá traducido por él del árabe. Uno de los manuscritos del Liber Luminis luminum menciona que fue traducido por Michael Scot; véase[17] También se encuentran descripciones del ácido nítrico en obras falsamente atribuidas a Alberto Magno y Ramon Llull, que lo preparaban destilando una mezcla que contenía niter y Vitriolo verde y la llamaban "eau forte" (aqua fortis).[18][19]
En el siglo XVII, Johann Rudolf Glauber ideó un proceso para obtener ácido nítrico destilando nitrato potásico con ácido sulfúrico. En 1776 Antoine Lavoisier citó el trabajo de Joseph Priestley para señalar que se puede convertir a partir del óxido nítrico (al que llama "aire nitroso"), "combinado con un volumen aproximadamente igual de la parte más pura del aire común, y con una cantidad considerable de agua."[20][21] En 1785 Henry Cavendish determinó su composición precisa y demostró que podía sintetizarse haciendo pasar una corriente de chispas eléctricas a través de aire húmedo.[18] En 1806, Humphry Davy informó de los resultados de extensos experimentos de electrólisis de agua destilada concluyendo que el ácido nítrico se producía en el ánodo a partir de gas nitrógeno atmosférico disuelto. Utilizó una batería de alto voltaje y electrodos y recipientes no reactivos, como conos de electrodos de oro que hacían las veces de recipientes con puentes de amianto húmedo.[22]
La producción industrial de ácido nítrico a partir del aire atmosférico comenzó en 1905 con el proceso Birkeland-Eyde, también conocido como proceso de arco.[23] Este proceso se basa en la oxidación del nitrógeno atmosférico por el oxígeno atmosférico a óxido nítrico con un arco eléctrico a muy alta temperatura. Se obtuvieron rendimientos de hasta aproximadamente un 4-5% de óxido nítrico a 3000 °C, y menores a temperaturas más bajas.[23][24] El óxido nítrico se enfriaba y se oxidaba con el oxígeno atmosférico restante hasta convertirse en dióxido de nitrógeno, que posteriormente se absorbía en agua en una serie de torres de absorción de columna de relleno o columna de placas para producir ácido nítrico diluido. Las primeras torres hacían burbujear el dióxido de nitrógeno a través de agua y fragmentos de cuarzo no reactivos. Alrededor del 20% de los óxidos de nitrógeno producidos quedaban sin reaccionar, por lo que las torres finales contenían una solución alcalina para neutralizar el resto.[25] El proceso era muy intensivo en energía y fue rápidamente desplazado por el proceso Ostwald una vez que el amoníaco barato estuvo disponible.
Otro de los primeros métodos de producción fue inventado por el ingeniero francés Albert Nodon hacia 1913. Su método producía ácido nítrico a partir de la electrólisis del nitrato de calcio convertido por bacterias a partir de la materia nitrogenada de las turberas. Se hundía en la turba una vasija de barro rodeada de piedra caliza y se fijaba con madera alquitranada para crear un compartimento para el ánodo de carbono alrededor del cual se formaba el ácido nítrico. El ácido nítrico se bombeaba desde una vasija de barro[26] que se hundía hasta el fondo de la vasija. En la parte superior se bombeaba agua fresca a través de otra tubería de barro para reemplazar el líquido extraído. El interior se llenaba con coque. Los cátodos de hierro fundido se hundían en la turba que lo rodeaba. La resistencia era de unos 3 ohmios por metro cúbico y la potencia suministrada era de unos 10 voltios. La producción de un depósito era de 800 toneladas al año.[26][27]
Una vez introducido el proceso Haber para la producción eficiente de amoníaco en 1913, la producción de ácido nítrico a partir de amoníaco mediante el proceso Ostwald superó a la producción a partir del proceso Birkeland-Eyde. Este método de producción sigue utilizándose en la actualidad.
Véase también: Aqua fortis
Remove ads
Referencias
Enlaces externos
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads