
Sulfito
sal de ácido sulfuroso / De Wikipedia, la enciclopedia encyclopedia
Los sulfitos son las sales o ésteres del hipotético ácido sulfuroso H2SO3. Las sales de sulfito contienen el anión SO32-, siendo los más importantes el sulfito de sodio y el sulfito de magnesio. Se forman al poner en contacto el óxido de azufre (IV) (SO2) con disoluciones alcalinas. Se trata de sustancias reductoras[1] pasando el azufre del estado de oxidación +IV a + VI. En disoluciones ácidas se descomponen liberando de nuevo óxido de azufre (IV).
Los sulfitos orgánicos del tipo R-O-S(=O)-O-R'(donde R y R' son grupos orgánicos) se obtienen convenientemente a partir de cloruro de tionilo (SOCl2) y alcoholes.
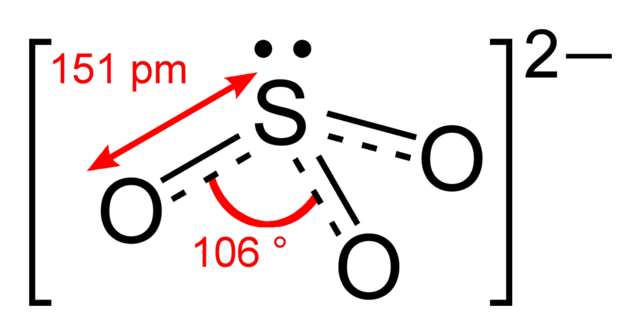
El ion del sulfito tiene forma de pirámide trigonal con el átomo de azufre en el centro y los tres átomos de oxígeno y un par de electrones apuntando a las esquinas.