Ciclobutadieno
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
El ciclobutadieno es un compuesto orgánico cíclico con dos dobles enlaces (dieno) conjugados de fórmula C4H4. Es muy reactivo debido a su tendencia a dimerizarse. Aunque el compuesto original no se ha aislado, algunos derivados sustituidos son robustos y una sola molécula de ciclobutadieno es bastante estable. Como el compuesto se degrada por un proceso bimolecular a 1,3-butadieno, la especie solo se puede observar mediante técnicas de aislamiento en matrices inertes de gases inertes a bajas temperaturas (temperaturas inferiores a 35 K) quedando atrapada sin poder dimerizarse. A temperaturas superiores tiende a dimerizar por medio de la reacción de Diels-Alder, incluso a -78 °C. El isómero endo se forma preferentemente, mientras que el isómero exo se forma solo como un subproducto:[2][3][4]
 | ||
 | ||
| Nombre IUPAC | ||
| 1,3-Ciclobutadieno | ||
| General | ||
| Fórmula molecular | C4H4 | |
| Identificadores | ||
| Número CAS | 1120-53-2[1] | |
| ChEBI | CHEBI:33657 | |
| ChemSpider | 120626 | |
| PubChem | 136879 | |
| Propiedades físicas | ||
| Masa molar | 52 076 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
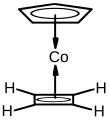
El ciclobutadieno es un ligando estable en muchos complejos metálicos. La razón de esto es que dos electrones se desplazan del metal a los orbitales del ligando, lo que da como resultado un sistema de 6 electrones-π aromáticos. Luego generalmente se puede separar del centro metálico oxidativamente (por ejemplo, por nitrato de cerio (IV)).[5][6]