Top-Fragen
Zeitleiste
Chat
Kontext
Tripeptide
Aus Wikipedia, der freien Enzyklopädie
Remove ads
Tripeptide sind aus drei Aminosäure-Resten aufgebaute Peptide und zählen zur Gruppe der Oligopeptide. Wie andere Oligopeptide besitzen Tripeptide häufig eine sehr spezifische physiologische Wirkung, z. B. in der Neurochemie, im Stoffwechsel und als Releasing-Hormone.[2] Proteine werden im Zuge der Verdauung durch Peptidasen in Aminosäuren, Dipeptide und Tripeptide zerlegt.[3] Tripeptide werden im Dünndarm und der Niere über den Peptidtransporter 1 aufgenommen.[4] Tripeptidyl-Peptidasen sind Peptidasen, die Tripeptide abspalten.
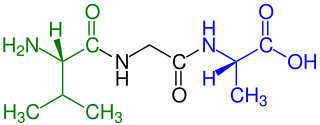
grün markiertem N-terminalen α-Aminosäure-Rest (im Beispiel: L-Valin) und blau markiertem C-terminalen α-Aminosäure-Rest (im Beispiel: L-Alanin)


Remove ads
Beispiele
Beispiele für natürlich vorkommende Tripeptide sind unter anderem die Antioxidantien Glutathion, die Ophthalminsäure, den Proteaseinhibitor Leupeptin, das Melanotropin-Release-Inhibiting-Hormon, die Lactotripeptide, GHK-Cu und das Herbizid Bialaphos. Einige natürliche Tripeptide besitzen eine Amidgruppe am C-Terminus, wie Thyreoliberin und das Melanotropin-Release-Inhibiting-Hormon. Die Peptidalkaloide unter den Mutterkornalkaloiden enthalten unter anderem ein Tripeptid. Ein nichtribosomal erzeugtes Peptid ist das ACV-Tripeptid. Synthetische Tripeptide sind die ACE-Hemmer Lisinopril, Enalapril und Ramipril sowie neuroprotektive Analoga des Thyreoliberins.[5]
Natürliche Tripeptide aus Milch (Casein) werden intakt resorbiert und wirken u. a. als schwache ACE-Hemmer.[6][7] Eine Wirkung an Opioidrezeptoren wird für Beta-Casomorphin beschrieben.[8]
Remove ads
Literatur
- S. Santos, I. Torcato, M. A. Castanho: Biomedical applications of dipeptides and tripeptides. In: Biopolymers. Band 98, Nr. 4, 2012, S. 288–293, PMID 23193593 (englisch).
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads
