Loading AI tools
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Benzolboronsäure, auch bekannt als Phenylboronsäure, ist eine chemische Verbindung aus der Gruppe der Boronsäuren.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
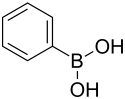 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Benzolboronsäure | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C6H7BO2 | |||||||||||||||||||||
| Kurzbeschreibung | ||||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 121,93 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
8,83[4] | |||||||||||||||||||||
| Löslichkeit |
löslich in Wasser (10 g·l−1 bei 20 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Es gibt zahlreiche Methoden, um Benzolboronsäure zu synthetisieren. Eine verbreitete Synthese verwendet Phenylmagnesiumbromid und Borsäuretrimethylester zur Bildung des entsprechenden Esters, der dann durch Hydrolyse in Phenylboronsäure umgesetzt wird.[5]
Eine analoge Synthese kann auch ausgehend vom Phenyllithium erfolgen.[6]
Benzolboronsäure ist ein farbloser bis gelblicher geruchloser Feststoff.[1][2] Der Feststoff bildet ein orthorhombisches Kristallgitter mit der Raumgruppe Iba2 (Raumgruppen-Nr. 45).[7] Im Festkörper liegen Dimere vor.[7] Durch trockenes Erhitzen kann die Verbindung unter Wasserabspaltung zum Anhydrat Triphenylboroxin trimerisiert werden.[5][8] Die Reaktion verläuft aus der festen Phase mit einer molaren Reaktionsenthalpie von 41 kJ·mol−1 endotherm.[8]
In Gegenwart von Carbonsäure kann eine säurekatalysierte Deboronierung (Protodeboronierung) erfolgen, wobei ein 6-gliedriger Übergangszustand zusätzlich noch über einen Lewis-Säure-Base Komplex zwischen dem Bor-Atom und dem Sauerstoff der Carboxylfunktion stabilisiert wird. Dieser Mechanismus setzt das Vorhandensein von stöchiometrischen Mengen an Carbonsäure voraus. Allerdings ist zu beachten, dass durch Kondensationsprozesse des als Nebenprodukt resultierenden Borsäurederivates die Essigsäure wieder freigesetzt werden kann und somit auch unterstöchiometrische Mengen für eine quantitative Deboronierung ausreichen können.[9][10]
Benzolboronsäure wird bei zahlreichen Kreuz-Kupplungsreaktionen verwendet. Im Jahr 1979 fanden Miyarura und Suzuki eine Bildungsreaktion für Kohlenstoff-Kohlenstoff-Bindungen (heute als Suzuki-Kupplung bezeichnet) welche Arylboronsäuren mit Halogenaromaten unter katalytischer Verwendung von Palladium-Phosphan-Komplexen zu Biphenylderivaten oder Vinylaromaten umsetzen.[11]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.