
Glycosyltransferasen
Enzymfamilie / aus Wikipedia, der freien encyclopedia
Glycosyltransferasen (lat. transferre ‚hinübertragen‘) sind Enzyme vom Typ der Transferasen, die als Katalysatoren Monosaccharid-Einheiten eines aktivierten Kohlenhydrats, sogenannte Glycosylreste, auf ein Akzeptor-Molekül, üblicherweise einen Alkohol, übertragen (Donator-Akzeptor-Prinzip). Diese Reaktionen laufen normalerweise als posttranslationale Modifikationen bei der Proteinbiosynthese von Glycoproteinen entweder als N-Glycosylierung im endoplasmatischen Retikulum oder als O-Glycosylierung im Golgi-Apparat ab.
| Glycosyltransferasen | ||
|---|---|---|
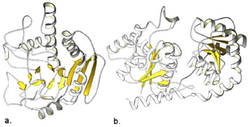 | ||
| (a) Enzym GTA (produziert das Blutgruppen A-Antigen) (b) Enzym GtfB (glycosyliert Vancomycin) | ||
| Enzymklassifikation | ||
| EC, Kategorie | 2.4.-.- | |
| Reaktionsart | Übertragung einer Monosaccharid-Einheit (Donator-Akzeptor-Prinzip) | |
| Substrat | 
| |
| Produkte |  | |
| Vorkommen | ||
| Übergeordnetes Taxon | Lebewesen | |
Auch die Glycosylierung von Glycolipiden (beispielsweise von Cerebrosiden und Gangliosiden) wird durch Glycosyltransferasen katalysiert.
Das menschliche Genom beherbergt Gene für mindestens 250 verschiedene Glycosyltransferasen.[1] In der Mehrzahl sind diese in drei Enzymfamilien beheimatet.[2] Mit der Enzymausstattung zur Glycosylierung, deren Funktionen und ihren Produkten beschäftigt sich die Glykomik.