Oxid sodný
chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
Oxid sodný (Na2O) je jediný oxid sodíku.
Remove ads
Remove ads
Vlastnosti
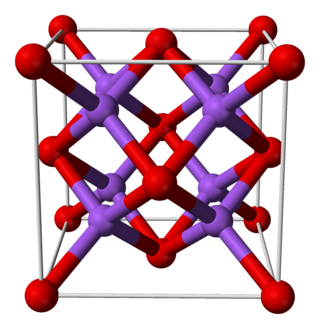
Je to za normálních podmínek bílá krystalická látka.[2] Její krystaly, podobně jako krystaly všech oxidů alkalických kovů, mají tzv. antifluoritovou strukturu, což znamená, že pozice aniontů a kationtů v krystalové mřížce jsou zcela obrácené, než je tomu u fluoridu vápenatého (CaF2). Sodíkové kationty tvoří středy tetraedrů, neboť jsou připojeny na 4 atomy kyslíku, zatímco kyslíkové atomy tvoří středy krychle, neboť jsou navázány na 8 sodíkových iontů.[3][4] Za vysokých teplot se rozkládá na peroxid sodný a sodík.[5]
S vodou bouřlivě reaguje za vzniku hydroxidu sodného[5] (je to vlastně jeho anhydrid):
Na2O + H2O → 2 NaOH |
|
Při kontaktu s očima, pokožkou a sliznicí dýchací soustavy je silně dráždivý a zejména prášková forma může snadno způsobit zdravotní potíže. Vdechnutí většího množství dokonce může vyvolat plicní edém.[5]
Remove ads
Příprava
Tento oxid je možné připravit např. reakcí oxidu dusného se sodíkem:[6]
N2O + 2Na → Na2O + N2 |
|
Taktéž je možné jej připravit tepelným rozkladem uhličitanu sodného:
Na2CO3 → Na2O + CO2 |
|
Použití
Oxid sodný se používá jako přísada při výrobě skla pro snížení teploty tavení oxidu křemičitého, který je hlavní složkou skla.
Reference
Literatura
Externí odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads