Chlorid ruthenitý je anorganická sloučenina se vzorcem RuCl3, která často vytváří hydráty, RuCl3·xH2O; v bezvodé i hydratované podobě jde o hnědou až černou pevnou látku. Hydrát, jehož složení se může lišit, ale často bývá uváděno jako trihydrát, se používá na přípravu dalších sloučenin ruthenia.
| Chlorid ruthenitý | |
|---|---|
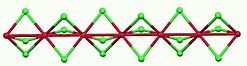 Model struktury | |
| Obecné | |
| Systematický název | chlorid ruthenitý |
| Sumární vzorec | RuCl3 |
| Identifikace | |
| Registrační číslo CAS | 10049-08-8 |
| PubChem | 82323 |
| SMILES | Cl[Ru](Cl)Cl |
| InChI | InChI=1S/3ClH.Ru/h3*1H;/q;;;+3/p-3 |
| Vlastnosti | |
| Molární hmotnost | 207,43 g/mol |
| Teplota rozkladu | >500 °C (>770 K) |
| Rozpustnost ve vodě | rozpustný hydrát, bezvodý nerozpustný |
Některá data mohou pocházet z datové položky. | |
Bezvodý chlorid ruthenitý se připravuje zahříváním práškového ruthenia za přítomnosti chloru. Chlorace může probíhat v prostředí obsahujícím oxid uhelnatý, kdy je produkt odnášen proudem plynu a po ochlazení krystalizuje.[1][2]
RuCl3 vytváří dva známé alotropy. Černý α-RuCl3 má strukturu podobnou chloridu chromitému (CrCl3), kde vzdálenosti mezi atomy Ru činí 346 pm. Tento alotrop obsahuje vrstvy Ru3+ obklopené oktaedrickými klecemi z aniontů Cl−. Základní stav je nízkospinový s úhlovým momentem L=1.[3][4]
Vrstvy α-RuCl3 jsou drženy Van der Waalsovými silami.[5]
Tmavě hnědý metastabilní β-RuCl3 vytváří hexagonální krystaly; ty se skládají z řetězců osmistěnů propojených vrcholy, kde mají vzdálenosti Ru-Ru hodnotu 283 pm, se strukturou podobající se chloridu zirkonitému. β-RuCl3 lze zahřátím na 450–600 °C nevratně převést na α-formu. β-forma je oproti paramagnetickému α-RuCl3 diamagnetická.[6]
Páry RuCl3 se za vysokých teplot rozkládají na prvky; změna entalpie při 750 °C (1020 K), ΔdissH1020, se odhaduje na +240 kJ/mol.
Protože je RuCl3·xH2O nejběžnější sloučeninou ruthenia, tak se používá na přípravu mnoha dalších. Komplexy ruthenia, například chloridové, mohou mít více různých oxidačních čísel, přičemž v některých jsou nereaktivní. Ruthenium se vyznačuje stabilitou komplexů obsahujících Ru2+, Ru3+ (jako je RuCl3·xH2O) a Ru4+.
Příklady komplexů připravených z RuCl3
- RuCl2(PPh3)3, hnědě zbarvená sloučenina rozpustná, v benzenu, také použitelná na přípravu dalších sloučenin. Vzniká touto reakcí:[7]
- 2 RuCl3·xH2O + 7 PPh3 → 2 RuCl2(PPh3)3 + OPPh3 + 5 H2O + 2 HCl
- Octan-chlorid ruthenato-ruthenitý, připravovaný redukcí chloridu ruthenitého v kyselině octové
- [RuCl2(C6H6)]2 se získává z cyklohexa-1,3-dienu nebo cyklohexa-1,4-dienu:[8][9]
- 2 RuCl3·xH2O + 2 C6H8 → [RuCl2(C6H6)]2 + 6 H2O + 2 HCl + H2
- Ru(bipy)3Cl2, luminescentní sůl, připravovaná podle této rovnice:[10]
- 2 RuCl3·xH2O + 6 bipy + CH3CH2OH → 2 [Ru(bipy)3]Cl2 + 6 H2O + CH3CHO + 2 HCl
Meziproduktem je cis-Ru(bipy)2Cl2.[10]
- 2 RuCl3·xH2O + 2 C5Me5H → [RuCl2(C5Me5)]2 + 6 H2O + 2 HCl
[RuCl2(C5Me5)]2 lze dále redukovat na [RuCl(C5Me5)]4.
- RuCl3·xH2O + 3 C5H8O2 → Ru(C5H7O2)3 + 3 H2O + 3 HCl
Některé z těchto sloučenin byly využity při výzkumech, za které byly uděleny dvě Nobelovy ceny; v roce 2001 získal Rjódži Nojori Nobelovu cenu za rozvoj [rutheniových katalyzátorů a roku 2005 obdržel Robert Grubbs Nobelovu cenu za rozvoj metatezí alkenů katalyzovaných alkylideny ruthenia.
Reakce s oxidem uhelnatým
RuCl3(H2O)x reaguje s oxidem uhelnatým, a to i za mírných podmínek;[13] chlorid železitý oproti tomu s CO nereaguje. CO redukuje červenohnědé Ru3+ na světle žluté sloučeniny Ru2+; například vystavení ethanolového roztoku RuCl3(H2O)x oxidu uhelnatému o tlaku 100 kPa může, v závislosti na podmínkách, vést k [Ru2Cl4(CO)4], [Ru2Cl4(CO)4]2−, nebo [RuCl3(CO)3]−. Přidáním ligandů (L) k těmto roztokům vznikají sloučeniny typu Ru-Cl-CO-L (L = PR3). Jejich redukcemi zinkem se tvoří oranžový dodekakarbonyl triruthenia (Ru3(CO)12).
- 6 RuCl3·xH2O + 9 Zn + 24 CO → 2 Ru3(CO)12 + 6x H2O + 9 ZnCl2
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.