Pila Leclanché
From Wikipedia, the free encyclopedia
From Wikipedia, the free encyclopedia
La pila Leclanché o cel·la Leclanché és una cel·la electroquímica primària que va ser inventada i patentada per Georges Leclanché el 1866. Contenia una dissolució conductora (electròlit) de clorur d'amoni, un càtode (pol positiu) de carboni, un despolaritzador de diòxid de manganès i un ànode (terminal negatiu) de zinc.[1] La pila Leclanché era essencialment una versió independent d'una bateria de vas de terrissa porosa, i el seu disseny va ser bastant copiat.[2] La química d'aquesta pila va ser, més tard, adaptada amb èxit per a la fabricació de piles seques.
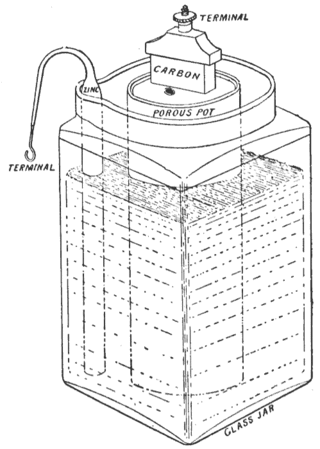
El disseny original d'aquesta cel·la feia servir un atuell porós. Això li proporcionava una resistència interna relativament alta i es van fer diverses modificacions per reduir-la. Aquestes modificacions inclouen la "cel·la de blocs d'aglomerat" i la "cel·la de tela de sac".
A la cel·la Leclanché original, el despolaritzador, fet de diòxid de manganès atapeït, estava empaquetat dins d'un vas porós, i una barra de carboni s'introduïa en el centre perquè actués com càtode. L'ànode, que era una barra de zinc, estava submergit juntament amb el vas anterior en una dissolució de clorur d'amoni. La dissolució líquida actuava com l'electròlit, que penetrava a través del vas porós per fer contacte amb el càtode.

El 1871, Leclanché va prescindir del vas porosa i la va reemplaçar per un parell de "blocs d'aglomerat", adjunts a la placa de carboni per bandes de goma. Aquests blocs estaven fets d'una barreja de diòxid de manganès amb aglutinants i pressionant la barreja en els motlles.
Aquesta cel·la de vas porosa va ser reemplaçada per un embolcall de tela de sac o arpillera. A més, la barra de zinc va ser substituïda per un cilindre de zinc per aconseguir una major àrea superficial. Tenia una menor resistència interna que qualsevol dels anteriors (atuell porosa i blocs d'aglomerat).
El procés químic que produeix electricitat en una pila Leclanché comença quan els àtoms de zinc en la superfície de l'ànode s'oxiden, és a dir, perden dos dels seus electrons i queden carregats positivament com ions Zn 2+. Com els ions zinc (II) són solubles en l'electròlit, difonen i s'allunyen de l'ànode, deixant els seus electrons a la superfície, de manera que l'ànode adquireix una càrrega més negativa que el càtode.[4] Quan la cèl·lula es connecta a un circuit elèctric extern, l'excés d'electrons de l'ànode de zinc flueix pel circuit fins a la barra de carboni que actua de càtode: aquest moviment o flux dels electrons forma el corrent elèctric extern, capaç de ser usat per a diferents aplicacions.
Quan els electrons arriben a la barra de carboni, es combinen amb el diòxid de manganès i l'aigua, que reaccionen entre si per produir òxid de manganès (III) i ions hidròxid amb càrrega negativa. Això va acompanyat d'una reacció secundària en la qual els ions d'hidròxid negatius reaccionen amb els ions positius d'amoni, presents en l'electròlit de clorur d'amoni per produir molècules d'amoníac i aigua:
Les semirreaciones d'aquesta reacció redox són les següents:
| Elèctrode (signe) | Procés químic | semireaccions | Potencial (V) |
|---|---|---|---|
| Ànode (elèctrode negatiu) | Oxidació del Zn | Zn (s) → Zn 2+ (aq)+2 i - | E º =- 0,76 V |
| Càtode (elèctrode positiu) | Reducció del MnO 2+ | 2 Mn O 2 (s)+H 2 O+2 i - → Mn 2 O 3 (s)+2 OH - | E º =+0,95 V |
| Reacció en l'electròlit | Hidròlisi dels ions amoni | 2 OH - +2 NH 4 Cl (s) → 2 H 2 O+2 NH 3 (aq) +2 Cl - (aq) |
La força electromotriu (fem) produïda per una cel·la Leclanché està al voltant d'1,5 volts amb una resistència de diversos ohms, quan es fa servir el disseny original amb vas porós. Es va aplicar molt extensament en els començaments de la telegrafia, per a aplicacions de senyalització, timbres elèctrics i altres usos similars en els quals era necessària un corrent intermitent i era desitjable que la bateria requerís poc manteniment.
La pila Leclanché (o cel humida com també se l'anomena) va ser la precursora de la moderna pila seca de zinc-carboni.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.