
Amoníac
compost químic la qual molècula està formada per un àtom de nitrogen unit a tres àtoms d'hidrogen. / From Wikipedia, the free encyclopedia
L'amoníac, de noms sistemàtics trihidrur de nitrogen o azà, és un compost químic molecular, la molècula del qual consta d'un àtom de nitrogen enllaçat mitjançant enllaços simples covalents a tres àtoms d'hidrogen d'acord amb la fórmula 
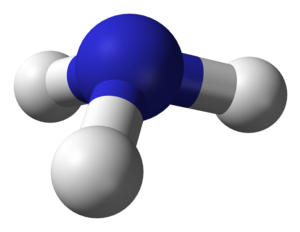 | |
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 17,026549096 Da |
| Epònim | Zeus Ammon |
| Descobridor o inventor | Joseph Priestley |
| Trobat en el tàxon | |
| Rol | metabòlit primari |
| Estructura química | |
| Fórmula química | NH₃ |
 | |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| Propietat | |
| Densitat | 0,7625 kg/m³ (a 0 °C, gas) |
| Velocitat del so | 415 m/s (0 °C, gas) |
| PKa | 9,21 |
| Solubilitat | 34 g/100 g (aigua, 20 °C) |
| Moment dipolar elèctric | 1,471 D |
| Punt de fusió | −77,74 °C −78 °C |
| Punt d'ebullició | −33,4 °C −33 °C (a 760 Torr) −33,33 °C (a 101,325 kPa) |
| Entropia molar estàndard | 192,5 J/(mol K) |
| Moment dipolar elèctric | 1,471 D |
| Entalpia estàndard de formació | −45,94 kJ/mol |
| Pressió de vapor | 8,5 atm (a 20 °C) |
| Perill | |
| Límit inferior d'explosivitat | 15 vol% |
| Límit superior d'explosivitat | 28 vol% |
| Dosi letal mínima | 5.000 ppm (ésser humà, mamífers, inhalació, 5 min) 1.500 mg/m³ (ésser humà, inhalació, 30 min) 5.000 ppm (mamífers, inhalació, 5 min) 3.317 ppm (ratolí de laboratori, inhalació, 1 h) 132 mg/kg (ésser humà) |
| Dosi letal mediana | 7 g/m³ (gat, conill, inhalació, 1 h) 4.600 mg/m³ (ratolí de laboratori, inhalació, 2 h) 4.500 ppm (ratolí de laboratori, inhalació, 1 h) 4.230 ppm (ratolí de laboratori, inhalació, 1 h) 21.430 ppm (ratolí de laboratori, inhalació, 30 min) 7 g/m³ (conill, inhalació, 1 h) 18.600 mg/m³ (rata de laboratori, inhalació, 5 min) 7.040 mg/m³ (rata de laboratori, inhalació, 30 min) 2.000 ppm (rata de laboratori, inhalació, 4 h) 17.401 ppm (rata de laboratori, inhalació, 15 min) 9.500 ppm (rata de laboratori, inhalació, 1 h) 40.300 ppm (rata de laboratori, inhalació, 10 min) 28.595 ppm (rata de laboratori, inhalació, 20 min) 20.300 ppm (rata de laboratori, inhalació, 40 min) 11.590 ppm (rata de laboratori, inhalació, 1 h) 7.338 ppm (rata de laboratori, inhalació, 1 h) 4.837 ppm (ratolí de laboratori, inhalació, 1 h) 9.859 ppm (conill, gat, inhalació, 1 h) 2.000 ppm (rata de laboratori, inhalació, 1 h) |
| Temperatura d'autoignició | 651 °C |
| Límit d'exposició mitjana ponderada en el temps | 18 mg/m³ (10 h, cap valor) 35 mg/m³ (8 h, Estats Units d'Amèrica) 25 ppm (, Egipte, Austràlia, Índia, Japó, Corea del Sud, Mèxic, Nova Zelanda, Noruega, Perú, Suècia, Turquia, Regne Unit) 20 ppm (, Àustria, Bèlgica, Dinamarca, Finlàndia, Alemanya, Islàndia) 14 mg/m³ (, Comissió Europea, Hongria, Països Baixos) 10 ppm (, França) 20 mg/m³ (, Polònia) 50 ppm (, Tailàndia, Filipines) |
| Límit d'exposició a curt termini | 27 mg/m³ (Polònia) 35 ppm (Austràlia, Índia, Corea del Sud, Mèxic, Nova Zelanda, Perú) 50 ppm (Bèlgica, Finlàndia, Islàndia, Suècia) 36 mg/m³ (Comissió Europea, Hongria) 20 ppm (França) 20 mg/m³ (Rússia) |
| IDLH | 210 mg/m³ i 300 ppm |
| Potencial d'escalfament global | 0 |
| NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response () | |