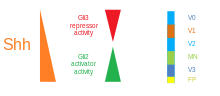
Zvučni jež ponekad i nadzvučni jež, najčešće sonični jež (eng. sonic hedgehog) jest protein koji je kod ljudi kodiran genom SHH sa hromosoma 7.[5] Ova signalna molekula je ključna u regulaciji embrionske morfogeneze kod svih ispitivanih, različitih vrsta životinja. SHH kontrolira organogenezu i organizaciju centralnog nervnog sistema, udova, prstiju i mnogih drugih dijelova tela. Zvučni jež je morfogen koji oblikuje embrion u razvoju koristeći gradijent koncentracije koji karakteriše model francuske zastave.[6] Ovaj model ima neujednačenu distribuciju SHH molekula koja upravlja različitim sudbinama ćelija prema koncentraciji. Mutacije ovog gena mogu uzrokovati prozencefalopatiju, neuspjeh podjele u moždanim hemisferama,[7] kao što je pokazano u eksperimentu koji koristi SHH nokaut-miševe u kojem se srednja linija prednjeg mozga nije uspjela razviti i umjesto toga nastala je samo jedna spojena telencefalonska vezikula.[8] Još uvijek ima ulogu u diferencijaciji, proliferaciji i održavanju tkiva i kod odraslih. Abnormalna aktivacija SHH signalizacije u tkivima odraslih uključena je u različite tipove karcinoma uključujući dojke, kožu, mozak, jetru, žučnu kesu i mnoge druge.[9]
Kratke činjenice Dostupne strukture, PDB ...
| Zvučni jež |
|---|
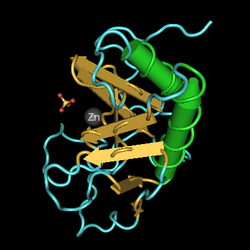 |
|
| Identifikatori |
|---|
| Aliasi | SHH |
|---|
| Vanjski ID-jevi | OMIM: 600725 MGI: 98297 HomoloGene: 30961 GeneCards: SHH |
|---|
|
|
|
| Ontologija gena |
|---|
| Molekularna funkcija | • calcium ion binding
• vezivanje iona metala
• patched binding
• GO:0070122 peptidase activity
• vezivanje iona cinka
• laminin-1 binding
• glycosaminoglycan binding
• morphogen activity
• hydrolase activity
• GO:0001948, GO:0016582 vezivanje za proteine
• endopeptidase activity
|
|---|
| Ćelijska komponenta | • citosol
• endoplasmic reticulum lumen
• membrana
• cell surface
• Lipidni splav
• ćelijska membrana
• Vanćelijsko
• extracellular region
• GO:0005578 Vanćelijski matriks
|
|---|
| Biološki proces | • positive regulation of skeletal muscle cell proliferation
• pattern specification process
• myotube differentiation
• mesenchymal cell proliferation
• male genitalia development
• bud outgrowth involved in lung branching
• limb bud formation
• T cell differentiation in thymus
• embryonic pattern specification
• positive regulation of skeletal muscle tissue development
• positive regulation of immature T cell proliferation in thymus
• positive regulation of kidney smooth muscle cell differentiation
• negative regulation of Wnt signaling pathway
• anatomical structure formation involved in morphogenesis
• ectoderm development
• hindgut morphogenesis
• spinal cord dorsal/ventral patterning
• GO:0007364, GO:0007361, GO:0007358 formation of anatomical boundary
• oligodendrocyte differentiation
• trachea development
• prostate gland development
• negative regulation of transcription elongation from RNA polymerase II promoter
• limb development
• Vaskulogeneza
• primary prostatic bud elongation
• heart looping
• telencephalon regionalization
• odontogenesis of dentin-containing tooth
• positive regulation of mesenchymal cell proliferation
• Angiogeneza
• positive regulation of epithelial cell proliferation involved in prostate gland development
• positive regulation of striated muscle cell differentiation
• negative regulation of proteasomal ubiquitin-dependent protein catabolic process
• embryonic digestive tract morphogenesis
• apoptotic signaling pathway
• inner ear development
• hair follicle morphogenesis
• Ćelijska proliferacija
• metanephros development
• lung epithelium development
• negative regulation of canonical Wnt signaling pathway
• regulation of proteolysis
• branching involved in salivary gland morphogenesis
• negative regulation of mesenchymal cell apoptotic process
• positive regulation of neuroblast proliferation
• dopaminergic neuron differentiation
• intermediate filament organization
• renal system development
• cell fate commitment
• GO:0009373 regulation of transcription, DNA-templated
• positive regulation of smoothened signaling pathway
• androgen metabolic process
• Nefrogeneza
• lung development
• GO:1903363 negative regulation of protein catabolic process
• thymus development
• embryonic organ development
• negative regulation of cell differentiation
• negative regulation of dopaminergic neuron differentiation
• embryonic digit morphogenesis
• negative regulation of alpha-beta T cell differentiation
• positive regulation of sclerotome development
• epithelial-mesenchymal cell signaling
• negative regulation of gene expression
• lymphoid progenitor cell differentiation
• negative thymic T cell selection
• GO:0060469, GO:0009371 positive regulation of transcription, DNA-templated
• positive regulation of Wnt signaling pathway
• ventral midline development
• central nervous system development
• heart development
• branching involved in ureteric bud morphogenesis
• negative regulation of T cell proliferation
• embryonic limb morphogenesis
• positive regulation of cell differentiation
• branching involved in prostate gland morphogenesis
• positive regulation of mesenchymal cell proliferation involved in ureter development
• establishment of cell polarity
• branching involved in blood vessel morphogenesis
• positive regulation of cerebellar granule cell precursor proliferation
• neuroblast proliferation
• pancreas development
• positive regulation of protein import into nucleus
• Ježev signalni put
• oligodendrocyte development
• camera-type eye development
• spinal cord motor neuron differentiation
• positive regulation of alpha-beta T cell differentiation
• digestive tract morphogenesis
• hair follicle development
• positive regulation of oligodendrocyte differentiation
• roof of mouth development
• left lung development
• striated muscle tissue development
• positive regulation of T cell differentiation in thymus
• cellular response to lithium ion
• embryonic foregut morphogenesis
• GO:1903374 anatomical structure development
• thalamus development
• stem cell development
• smoothened signaling pathway involved in regulation of cerebellar granule cell precursor cell proliferation
• cell fate specification
• negative regulation of apoptotic process
• GO:1901227 negative regulation of transcription by RNA polymerase II
• regulation of nodal signaling pathway involved in determination of lateral mesoderm left/right asymmetry
• Proteoliza
• embryonic skeletal system development
• regulation of protein localization to nucleus
• odontogenesis
• respiratory tube development
• regulation of prostatic bud formation
• thyroid gland development
• negative regulation of cell migration
• developmental growth
• right lung development
• determination of left/right asymmetry in lateral mesoderm
• positive thymic T cell selection
• mesenchymal smoothened signaling pathway involved in prostate gland development
• canonical Wnt signaling pathway
• Regulacija ekspresije gena
• osteoblast development
• negative regulation of cholesterol efflux
• dorsal/ventral neural tube patterning
• regulation of epithelial cell proliferation involved in prostate gland development
• epithelial-mesenchymal signaling involved in prostate gland development
• dorsal/ventral pattern formation
• branching morphogenesis of an epithelial tube
• lung lobe morphogenesis
• embryonic forelimb morphogenesis
• midbrain development
• skin development
• regulation of odontogenesis
• regulation of mesenchymal cell proliferation involved in prostate gland development
• mesenchymal cell proliferation involved in lung development
• positive regulation of hh target transcription factor activity
• prostate epithelial cord elongation
• metanephric mesenchymal cell proliferation involved in metanephros development
• Endocitoza
• lung morphogenesis
• cell development
• trachea morphogenesis
• epithelial cell proliferation involved in salivary gland morphogenesis
• cell-cell signaling
• salivary gland cavitation
• hindbrain development
• Koagulacija (krv)
• negative regulation of kidney smooth muscle cell differentiation
• somite development
• cerebellar granule cell precursor proliferation
• axon guidance
• negative regulation of ureter smooth muscle cell differentiation
• positive regulation of ureter smooth muscle cell differentiation
• multicellular organism development
• animal organ formation
• intein-mediated protein splicing
• determination of left/right symmetry
• vasculature development
• GO:1901313 positive regulation of gene expression
• regulation of cell population proliferation
• embryonic morphogenesis
• neural crest cell migration
• polarity specification of anterior/posterior axis
• positive regulation of cell population proliferation
• artery development
• protein localization to nucleus
• Bergmann glial cell differentiation
• forebrain development
• neuron fate commitment
• CD4-positive or CD8-positive, alpha-beta T cell lineage commitment
• striated muscle cell differentiation
• myoblast differentiation
• lung-associated mesenchyme development
• epithelial tube branching involved in lung morphogenesis
• positive regulation of cell division
• GO:0003257, GO:0010735, GO:1901228, GO:1900622, GO:1904488 positive regulation of transcription by RNA polymerase II
• anterior/posterior pattern specification
• embryonic hindlimb morphogenesis
• forebrain regionalization
• cell proliferation in external granule layer
• tracheoesophageal septum formation
• regulation of signaling receptor activity
|
|---|
| Izvori:Amigo / QuickGO |
|
| Ortolozi |
|---|
| Vrste | Čovjek | Miš |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (mRNK) | | |
|---|
| RefSeq (bjelančevina) | | |
|---|
| Lokacija (UCSC) | Chr 7: 155.8 – 155.81 Mb | Chr 5: 28.66 – 28.67 Mb |
|---|
| PubMed pretraga | [3] | [4] |
|---|
| Wikipodaci |
|
Zatvori
Gen ježa (hh) je prvi put identificiran kod Drosophila melanogaster, u klasičnim snimcima koje su uradili Christiane Nüsslein-Volhard i Eric Wieschaus, objavljenim u 1980.[10] Ovi snimci — koji su osvojili Nobelovu nagradu za fiziologiju ili medicinu 1995., zajedno sa razvojnim genetičarom Edwardom B. Lewisom — za identifikaiju gena koji kontroliraju segmentacija u ebrionu Drosophila. Gubitak funkcije hh uzrokuje mutantni fenotip, kada embrioni budu prekriveni zubcimima, tj. malim šiljastim izbočinama koje liče na bodljee ježa. Istraživanja Philipa Inghama, Andrew P. McMahon i Clifforda Tabina, s ciljem pronalaska ekvivalenta ježa kod kičmenjaka otkrila su tri homologna gena.[11][12][13][14]
Dva od ovih gena—„pustinjski jež“ i „indijski jež“— nazvani su po vrstama ježa, dok je „sonični jež“ dobio ime po Sonic the Hedgehog , naslovnom protagonisti istoimene franšize video igara.[15][16] Gen je tako nazvao Robert Riddle, koji je bio postdoktorski saradnik Laboratorije Clifford Tabin, nakon što se njegova supruga Betsy Wilder vratila kući sa časopisom o igricama koji sadrži reklamu za "Sonic the Hedgehog" video igrica.[17][18][19] Kod zebrica nađena su dva od tri duplirana gena kod kičmenjaka: hh i SHH[20] i SHH b[21] (ranije opisan kao tiggywinkle hedgehog, nazvan po The Tale of Mrs. Tiggy-Winkle, liku iz knjiga za djecu Beatrix Potter) i ihha i ihhb[22] ranije opisan kao tiggywinkle hedgehog, nazvan po Mrs. Tiggy-Winkle, liku iz Beatrix Potter, knjiga za djecu) i ranije opisan kao tiggywinkle hedgehog. knjiga za djecu) i ranije opisan kao tiggywinkle hedgehog, nazvan po Mrs. Tiggy-Winkle, liku iz Beatrix Potter, knjiga za djecu) i ranije opisan kao tiggywinkle hedgehog, nazvan po Mrs. Tiggy-Winkle, liku iz Beatrix Potter, knjiga za djecu, i ranije opisan kao tiggywinkle hedgehog,
Utvrđeno je da od homologa hh, SHH ima najkritičniju ulogu u razvoju, djelujući kao morfogen uključen u oblikovanje mnogih sistema—uključujući hormone prednjeg režnja hipofize,[23] moždani neopalij,[24] kičmenu moždinu,[25] pluća,[26] zube [27] i talamus preko zona limitans intrathalamica.[28][29] Kod kičmenjaka, razvoj udova i prstiju zavisi od lučenja zona polarizirajuće aktivnosti zvučnog ježa, koje se nalaze na zadnjoj strani embrionskog ekstremitetnog pupoljka.[13] Mutacije u genu SHH ljudskog soničnoog ježa uzrokuju holoprozencefaliju tip 3 HPE3, kao posljeicu gubitka ventralne srednje linije. Put transkripcije zvučnog ježa je također povezan sa formiranjem specifičnih tipova kancerogenih tumora, uključujući embrionski cerebellumski tumor.[30] i meduloblastom,[31] a kao i napredovanje tumora karcinom prostate.[32]
Da bi se SHH eksprimirao u udovima embriona u razvoju, morfogen koji se zove faktor rasta fibroblasta mora se izlučiti iz apikalnog ektodermnog grebena.[33]
Također se pokazalo da zvučni jež djeluje kao aksonska replika. |Pokazano je da SHH privlači komisurne aksone na ventralnoj srednjoj liniji kičmene moždine u razvoju.[34] Konkretno, SHH privlači retinske ganglijske ćelije (RGC) aksona u niskim koncentracijama i odbija ih u višim koncentracijama.[35] Pokazalo se da odsustvo (neekspresija) SHH kontrolira rast zadnjih udova u nastajanju kod kitova[36] (kitovi i delfini).
Gen SHH je član porodice ježevih gena s pet varijacija prerade DNK sekvence ili varijanti transkripta.[37] SHH se nalazi na hromosomu 7 i pokreće proizvodnju proteina zvučnog ježa.[37] Ovaj protein šalje signale kratkog i dugog dometa embrionskim tkivima da regulira razvoj.[38] Ako je gen SHH mutiran ili odsutan, protein zvučnog ježa ne može djelovati kako treba. Zvučni jež doprinosi rastu ćelija, diferencijaciji i formiranju ćelija, strukturiranju i organizaciji tjelesnog plana građe.[39] Ovaj protein funkcionira kao vitalna morfogena signalna molekula i ima važnu ulogu u formiranju mnogih različitih struktura u razvoju embriona. "SHH" gen utiče na nekoliko glavnih sistema organa, kao što su nervni, kardiovaskularni, respiratorni i mišićno-koštani sistem. Mutacije gena SHH mogu uzrokovati malformaciju komponenti ovih sistema, što može rezultirati velikim problemima u razvoju embriona. Na mozak i oči, naprimjer, mogu značajno uticati mutacije ovog gena i uzrokovati poremećaje kao što su mikroftalmija i holoprozencefalija. Mikroftalmija je stanje koje utiče na oči, što rezultira malim, nerazvijenim tkivima na jednom ili oba oka. To može dovesti do problema u rasponu od koloboma jednog oka do potpunog odsustva očiju. Holoprozencefalija je stanje koje je najčešće uzrokovano mutacijom gena SHH koja uzrokuje nepravilno razdvajanje lijeve i desne hemisfere mozga i dismorfiju lica. Mnogi sistemi i strukture se u velikoj mjeri oslanjaju na ispravnu ekspresiju gena SHH i naknadnog proteina zvučnog ježa, čime se izdvaja kao esencijalni gen za razvoj.
Da bi se SHH eksprimirao u udovima embrija u razvoju, morfogen zvan faktor rasta fibroblasta mora biti izlučen iz apikalnog dijela ektodermnog grebena.[33]
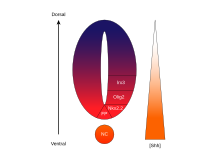
Morfogeni sa obrascima dorzoventralne osovine
nervne cijevi: Gradijenti SHH i BMP nervne cijevi
kičmenjakaFormiranje ektopijskog poda nervne cijevi u prisustvu
notohordaVentralni domeni
nervne cijevi: Tipovi ventralnih ćelija nervne cijevi
SHH prolazi kroz niz koraka obrade prije nego što se izluči iz ćelije. Novosintetizovani SHH teži 45 kDa i naziva se preprotein. Kao izlučeni protein, sadrži kratku signalnu sekvencu na svom N-kraju, koji prepoznaje čestica prepoznavanja signala tokom translokacije u endoplazmatski retikulum (ER) , prvi korak u lučenju. Proteina. Kada se translokacija završi, signalnu sekvencu uklanja signalna peptidaza u ER. Tamo se SHH podvrgava autoprocesiranju za generiranje 20 kDa N-terminalnog signalnog domena (SHH-N) i 25 kDa C-terminalnog domena bez poznate signalne uloge.[40] Cijepanje je katalizirano proteazama unutar C-terminalnog domena. Tokom reakcije, na C-terminal dodaje se molekula holesterola SHH-N.[41][42] Dakle, C-terminalni domen djeluje kao intein i holesterolska transferaza. Još jedan hidrofobni dio, palmitat, dodaje se u alfa-amin N-terminalni cistein SHH-N. Ova modifikacija je potrebna za efikasnu signalizaciju, što rezultira 30-strukim povećanjem potencije u odnosu na nepalmitilirani oblik, a provodi je član membranski vezana O-aciltransferaza porodice protein-cistein N-palmitoiltransferaza HHAT.[43]
Marigo, Valeria; Roberts, Drucilla J.; Lee, Scott M. K.; Tsukurov, Olga; Levi, Tatjana; Gastier, Julie M.; Epstein, Douglas J.; Gilbert, Debra J.; Copeland, Neal G.; Seidman, Christine E.; Jenkins, Nancy A. (1. 7. 1995). "Cloning, Expression, and Chromosomal Location of SHH and IHH: Two Human Homologues of the Drosophila Segment Polarity Gene Hedgehog". Genomics (jezik: engleski). 28 (1): 44–51. doi:10.1006/geno.1995.1104. ISSN 0888-7543. PMID 7590746. Nanni, Luisa; Ming, Jeffrey E.; Bocian, Maureen; Steinhaus, Kathryn; Bianchi, Diana W.; de Die-Smulders, Christine; Giannotti, Aldo; Imaizumi, Kiyoshi; Jones, Kenneth L.; Del Campo, Miguel; Martin, Rick A. (1. 12. 1999). "The Mutational Spectrum of the Sonic Hedgehog Gene in Holoprosencephaly: SHH Mutations Cause a Significant Proportion of Autosomal Dominant Holoprosencephaly". Human Molecular Genetics. 8 (13): 2479–2488. doi:10.1093/hmg/8.13.2479. ISSN 0964-6906. PMID 10556296. Krauss S, Concordet JP, Ingham PW (decembar 1993). "A functionally conserved homolog of the Drosophila segment polarity gene hh is expressed in tissues with polarizing activity in zebrafish embryos". Cell. 75 (7): 1431–44. doi:10.1016/0092-8674(93)90628-4. PMID 8269519. S2CID 46266627. Echelard Y, Epstein DJ, St-Jacques B, Shen L, Mohler J, McMahon JA, McMahon AP (decembar 1993). "Sonic hedgehog, a member of a family of putative signaling molecules, is implicated in the regulation of CNS polarity". Cell. 75 (7): 1417–30. doi:10.1016/0092-8674(93)90627-3. PMID 7916661. S2CID 6732599. Herzog W, Zeng X, Lele Z, Sonntag C, Ting JW, Chang CY, Hammerschmidt M (februar 2003). "Adenohypophysis formation in the zebrafish and its dependence on sonic hedgehog". Dev. Biol. 254 (1): 36–49. doi:10.1016/S0012-1606(02)00124-0. PMID 12606280. Lewis KE, Eisen JS (septembar 2001). "Hedgehog signaling is required for primary motoneuron induction in zebrafish". Development. 128 (18): 3485–95. doi:10.1242/dev.128.18.3485. PMID 11566854. Wolpert L (2015). Principles of Development (5th izd.). Oxford University Press. str. 500.
Taylor MD, Northcott PA, Korshunov A, Remke M, Cho YJ, Clifford SC, Eberhart CG, Parsons DW, Rutkowski S, Gajjar A, Ellison DW, Lichter P, Gilbertson RJ, Pomeroy SL, Kool M, Pfister SM (april 2012). "Molecular subgroups of medulloblastoma: the current consensus". Acta Neuropathologica. 123 (4): 465–72. doi:10.1007/s00401-011-0922-z. PMC 3306779. PMID 22134537. Lubik AA, Nouri M, Truong S, Ghaffari M, Adomat HH, Corey E, Cox ME, Li N, Guns ES, Yenki P, Pham S, Buttyan R (2016). "Paracrine Sonic Hedgehog Signaling Contributes Significantly to Acquired Steroidogenesis in the Prostate Tumor Microenvironment". International Journal of Cancer. 140 (2): 358–369. doi:10.1002/ijc.30450. PMID 27672740. S2CID 2354209. "SHH gene". Genetics Home Reference. U.S. National Library of Medicine. Pristupljeno 9. 4. 2020. Stanton BZ, Peng LF, Maloof N, Nakai K, Wang X, Duffner JL, Taveras KM, Hyman JM, Lee SW, Koehler AN, Chen JK, Fox JL, Mandinova A, Schreiber SL (mart 2009). "A small molecule that binds Hedgehog and blocks its signaling in human cells". Nat. Chem. Biol. 5 (3): 154–6. doi:10.1038/nchembio.142. PMC 2770933. PMID 19151731.
- Dorus S, Anderson JR, Vallender EJ, Gilbert SL, Zhang L, Chemnick LG, Ryder OA, Li W, Lahn BT (2006). "Sonic Hedgehog, a key development gene, experienced intensified molecular evolution in primates". Human Molecular Genetics. 15 (13): 2031–7. doi:10.1093/hmg/ddl123. PMID 16687440.
- Gilbert, Scott F. (2000). Developmental biology (6th izd.). Sunderland, Mass: Sinauer Associates. ISBN 978-0-87893-243-6.
- Kim J, Kim P, Hui CC (2001). "The VACTERL association: lessons from the Sonic hedgehog pathway". Clinical Genetics. 59 (5): 306–15. doi:10.1034/j.1399-0004.2001.590503.x. PMID 11359461. S2CID 34304310.
- Morton JP, Lewis BC (2007). "SHH signaling and pancreatic cancer: implications for therapy?". Cell Cycle. 6 (13): 1553–7. doi:10.4161/cc.6.13.4467. PMID 17611415. S2CID 4670615.
- Mullor JL, Sánchez P, Ruiz i Altaba A (2003). "Pathways and consequences: Hedgehog signaling in human disease". Trends Cell Biol. 12 (12): 562–9. doi:10.1016/S0962-8924(02)02405-4. PMID 12495844.
- Nanni L, Ming JE, Du Y, Hall RK, Aldred M, Bankier A, Muenke M (2001). "SHH mutation is associated with solitary median maxillary central incisor: a study of 13 patients and review of the literature". American Journal of Medical Genetics. 102 (1): 1–10. doi:10.1002/1096-8628(20010722)102:1<1::AID-AJMG1336>3.0.CO;2-U. PMID 11471164.
- Williams JA (2006). "Hedgehog and spinal cord injury". Expert Opinion on Therapeutic Targets. 9 (6): 1137–45. doi:10.1517/14728222.9.6.1137. PMID 16300466. S2CID 5548531.
Šablon:Ježev signalni put